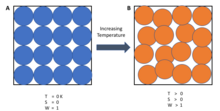
Třetí zákon zjednodušeně řečeno říká, že entropie dokonalého krystalu čisté látky se s teplotou blížící se nule blíží nule. Uspořádání dokonalého krystalu neponechává žádné nejasnosti ohledně umístění a orientace jednotlivých částí krystalu. Se snižováním energie krystalu se vibrace jednotlivých atomů redukují na nulu a krystal se stává všude stejným.
Třetí zákon poskytuje absolutní referenční bod pro určení entropie při jakékoli jiné teplotě. Entropie uzavřené soustavy určená vzhledem k tomuto nulovému bodu je pak absolutní entropií této soustavy. Matematicky je absolutní entropie libovolného systému při nulové teplotě přirozený logaritmus počtu základních stavů krát Boltzmannova konstanta kB = 1,38×10-23 J K-1.
Entropie dokonalé krystalové mřížky definované Nernstovou větou je nulová za předpokladu, že její základní stav je jedinečný, protože ln(1)=0. Jestliže se soustava skládá z jedné miliardy atomů, které jsou všechny stejné a leží v matrici dokonalého krystalu, počet kombinací jedné miliardy stejných věcí vzatých po jedné miliardě je Ω = 1. Proto:
S – S 0 = k B ln Ω = k B ln 1 = 0 {\displaystyle S-S_{0}=k_{\text{B}}\ln \Omega =k_{{text{B}}\ln {1}=0}

Rozdíl je nulový, proto počáteční entropie S0 může být libovolná zvolená hodnota, pokud ji všechny ostatní takové výpočty zahrnují jako počáteční entropii. V důsledku toho je pro pohodlí zvolena nulová hodnota počáteční entropie S0 = 0.
S – S 0 = S – 0 = 0 {\displaystyle S-S_{0}=S-0=0}.

S = 0 {\displaystyle S=0}

Příklad : Změna entropie krystalové mřížky ohřáté přicházejícím fotonemEdit
Předpokládejme soustavu tvořenou krystalovou mřížkou o objemu V s N stejnými atomy při teplotě T = 0 K a přicházejícím fotonem o vlnové délce λ a energii ε.
Počátečně existuje pouze jeden přístupný mikrostav :
S 0 = k B ln Ω = k B ln 1 = 0 {\displaystyle S_{0}=k_{\text{B}}\ln \Omega =k_{\text{B}}\ln {1}=0}

.
Předpokládejme, že krystalová mřížka pohlcuje příchozí foton. V mřížce je jedinečný atom, který interaguje a absorbuje tento foton. Po absorpci tedy existuje N možných mikrostavů přístupných systému, přičemž každému z mikrostavů odpovídá jeden excitovaný atom a ostatní atomy zůstávají v základním stavu.
Entropie, energie a teplota uzavřeného systému vzroste a lze ji vypočítat. Změna entropie je:
Δ S = S – S 0 = k B ln Ω {\displaystyle \Delta S=S-S_{0}=k_{\text{B}}\ln {\Omega }}

Z druhého termodynamického zákona:
Δ S = S – S 0 = δ Q T {\displaystyle \Delta S=S-S_{0}={\frac {\delta Q}{T}}}.

Tudíž:
Δ S = S – S 0 = k B ln ( Ω ) = δ Q T {\displaystyle \Delta S=S-S_{0}=k_{\text{B}}\ln(\Omega )={\frac {\delta Q}{T}}}.

Výpočet změny entropie:
S – 0 = k B ln N = 1.38 × 10 – 23 × ln ( 3 × 10 22 ) = 70 × 10 – 23 J K – 1 {\displaystyle S-0=k_{\text{B}}\ln {N}=1,38\krát 10^{-23}\krát \ln {(3\krát 10^{22})}=70\krát 10^{-23}\,\mathrm {J} \,\mathrm {K} ^{-1}}

Předpokládáme N = 3 – 1022 a λ = 1 cm . Změna energie systému v důsledku pohlcení jediného fotonu, jehož energie je ε:
δ Q = ϵ = h c λ = 6 .62 × 10 – 34 J ⋅ s × 3 × 10 8 m s – 1 0,01 m = 2 × 10 – 23 J {\displaystyle \delta Q=\epsilon ={\frac {hc}{\lambda }}={\frac {6,62\krát 10^{-34}\,\mathrm {J} \cdot \mathrm {s} \krát 3\krát 10^{8}\,\mathrm {m} \,\mathrm {s} ^{-1}}{0,01\,\mathrm {m} }}=2\krát 10^{-23}\,\mathrm {J} }

Teplota uzavřené soustavy vzroste o:
T = ϵ Δ S = 2 × 10 – 23 J 70 × 10 – 23 J K – 1 = 0,02857 K {\displaystyle T={\frac {\epsilon }{\Delta S}}={\frac {2\krát 10^{-23}\,\mathrm {J}} }{70\krát 10^{-23}\,\mathrm {J} \,\mathrm {K} ^{-1}}=0,02857\,\mathrm {K} }

To lze interpretovat jako průměrnou teplotu systému v rozsahu od 0 < S < 70 × 10 – 23 J K – 1 {\displaystyle 0<S<70\times 10^{-23}\,\mathrm {J} \,\mathrm {K} ^{-1}}

. Předpokládalo se, že foton absorbuje jediný atom, ale změna teploty a entropie charakterizuje celý systém.
Systémy s nenulovou entropií při absolutní nuleEdit
Příkladem systému, který nemá jedinečný základní stav, je systém, jehož čistý spin je poloviční celé číslo, pro které časová symetrie dává dva degenerované základní stavy. Pro takové systémy je entropie při nulové teplotě alespoň kB ln(2) (což je v makroskopickém měřítku zanedbatelné). Některé krystalické systémy vykazují geometrickou frustraci, kdy struktura krystalové mřížky brání vzniku jedinečného základního stavu. Hélium v základním stavu (pokud není pod tlakem) zůstává kapalné.
Skla a pevné roztoky si navíc při teplotě 0 K zachovávají velkou entropii, protože se jedná o velké soubory téměř degenerovaných stavů, ve kterých se dostávají do pasti mimo rovnováhu. Dalším příkladem pevné látky s mnoha téměř degenerovanými základními stavy, které jsou uvězněny mimo rovnováhu, je led Ih, který má „protonový nepořádek“.
Aby byla entropie při absolutní nule nulová, musí být magnetické momenty dokonale uspořádaného krystalu samy dokonale uspořádané; z entropického hlediska to lze považovat za součást definice „dokonalého krystalu“. Tuto podmínku mohou splňovat pouze feromagnetické, antiferomagnetické a diamagnetické materiály. Feromagnetické materiály však ve skutečnosti nemají nulovou entropii při nulové teplotě, protože spiny nepárových elektronů jsou všechny vyrovnány, a tím vzniká spinová degenerace v základním stavu. Naproti tomu materiály, které zůstávají při teplotě 0 K paramagnetické, mohou mít mnoho téměř degenerovaných základních stavů (například ve spinovém skle) nebo si mohou zachovat dynamickou neuspořádanost (kvantová spinová kapalina).
.