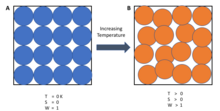
Den tredje lov siger i enkle vendinger, at entropien for en perfekt krystal af et rent stof nærmer sig nul, når temperaturen nærmer sig nul. Justeringen af en perfekt krystal efterlader ingen tvetydighed med hensyn til placeringen og orienteringen af hver enkelt del af krystallen. Efterhånden som krystallens energi reduceres, reduceres de enkelte atomers vibrationer til ingenting, og krystallen bliver den samme overalt.
Den tredje lov giver et absolut referencepunkt for bestemmelse af entropien ved enhver anden temperatur. Entropien i et lukket system, bestemt i forhold til dette nulpunkt, er derefter dette systems absolutte entropi. Matematisk set er den absolutte entropi for ethvert system ved nulpunktstemperatur den naturlige logaritme af antallet af grundtilstande gange Boltzmanns konstant kB = 1,38×10-23 J K-1.
Entropien for et perfekt krystalgitter som defineret ved Nernsts sætning er nul, forudsat at dets grundtilstand er unik, fordi ln(1)=0. Hvis systemet består af en milliard atomer, der alle er ens, og ligger inden for matricen af en perfekt krystal, er antallet af kombinationer af en milliard identiske ting taget en milliard ad gangen Ω = 1. Derfor:
S – S 0 = k B ln Ω = k B ln 1 = 0 {\displaystyle S-S_{0}=k_{\text{B}}}\ln \Omega =k_{\text{B}}}\ln {1}=0}

Differencen er nul, og derfor kan den oprindelige entropi S0 være en hvilken som helst valgt værdi, så længe alle andre sådanne beregninger omfatter denne som den oprindelige entropi. Som følge heraf vælges for nemheds skyld den indledende entropiværdi nul S0 = 0.
S – S 0 = S – 0 = 0 {\displaystyle S-S_{0}=S-0=0}

S = 0 {\displaystyle S=0}

Eksempel : Entropiændring af et krystalgitter opvarmet af en indkommende fotonRediger
Sæt et system bestående af et krystalgitter med volumen V af N identiske atomer ved T = 0 K, og en indkommende foton med bølgelængde λ og energi ε.
Initialt er der kun én tilgængelig mikrotilstand :
S 0 = k B ln Ω = k B ln 1 = 0 {\displaystyle S_{0}=k_{\text{B}}}\ln \Omega =k_{\text{B}}\ln {1}=0}

.
Lad os antage, at krystalgitteret absorberer den indkommende foton. Der er et unikt atom i gitteret, som interagerer og absorberer denne foton. Så efter absorptionen er der N mulige mikrotilstande tilgængelige for systemet, idet hver af mikrotilstandene svarer til et exciteret atom, og de andre atomer forbliver i grundtilstand.
Den entropi, energi og temperatur i det lukkede system stiger og kan beregnes. Entropiforandringen er:
Δ S = S – S 0 = k B ln Ω {\displaystyle \Delta S=S-S_{0}=k_{\text{B}}}\ln {\Omega }}

Fra den anden termodynamiske lov:
Δ S = S – S 0 = δ Q T {\displaystyle \Delta S=S-S_{0}={\frac {\delta Q}{T}}}}

Hence:
Δ S = S – S 0 = k B ln ( Ω ) = δ Q T {\displaystyle \Delta S=S-S_{0}=k_{\text{B}}}\ln(\Omega )={\frac {\delta Q}{T}}}}

Beregning af entropiændring:
S – 0 = k B ln N = 1.38 × 10 – 23 × ln ( 3 × 10 22 ) = 70 × 10 – 23 J K – 1 {\displaystyle S-0=k_{\text{B}}}\ln {N}=1.38\times 10^{-23}\times \ln {(3\times 10^{22})}=70\times 10^{-23}\,\mathrm {J} \,\mathrm {K} ^{-1}}

Vi antager N = 3 – 1022 og λ = 1 cm . Systemets energiforandring som følge af absorption af den enkelte foton, hvis energi er ε:
δ Q = ϵ = h c λ = 6.62 × 10 – 34 J ⋅ s × 3 × 10 8 m s – 1 0,01 m = 2 × 10 – 23 J {\displaystyle \delta Q=\epsilon ={\frac {hc}{\lambda }}={\frac {6,62\ gange 10^{-34}\,\mathrm {J} \cdot \mathrm {s} \times 3\times 10^{8}\,\mathrm {m} \,\mathrm {s} ^{-1}}}{0.01\,\mathrm {m} }}}=2\ gange 10^{-23}\,\mathrm {J} }

Temperaturen i det lukkede system stiger med:
T = ϵ Δ S = 2 × 10 – 23 J 70 × 10 – 23 J K – 1 = 0,02857 K {\displaystyle T={{\frac {\epsilon }{\Delta S}}={\frac {\frac {2\times 10^{-23}\,\mathrm {J} }{70\times 10^{-23}\,\mathrm {J} \,\mathrm {K} ^{-1}}}}=0.02857\,\mathrm {K}} }

Dette kan fortolkes som systemets gennemsnitlige temperatur over området fra 0 < S < 70 × 10 – 23 J K – 1 {\displaystyle 0<S<70\times 10^{-23}\,\mathrm {J} \,\mathrm {K} ^{-1}}

. Et enkelt atom blev antaget at absorbere fotonen, men temperatur- og entropiændringen karakteriserer hele systemet.
Systemer med ikke-nul entropi ved det absolutte nulpunktRediger
Et eksempel på et system, der ikke har en unik grundtilstand, er et system, hvis nettospin er et halvt heltal, for hvilket tidsomvendt symmetri giver to degenererede grundtilstande. For sådanne systemer er entropien ved nulpunktstemperatur mindst kB ln(2) (hvilket er ubetydeligt på en makroskopisk skala). Nogle krystallinske systemer udviser geometrisk frustration, hvor krystalgitterets struktur forhindrer fremkomsten af en entydig grundtilstand. Helium i grundtilstand forbliver flydende (medmindre det er under tryk).
Dertil kommer, at glas og faste opløsninger bevarer en stor entropi ved 0 K, fordi de er store samlinger af næsten degenererede tilstande, hvori de bliver fanget uden for ligevægt. Et andet eksempel på et fast stof med mange næsten degenererede grundtilstande, der er fanget uden for ligevægt, er is Ih, som har “proton uorden”.
For at entropien ved det absolutte nulpunkt skal være nul, skal de magnetiske momenter i en perfekt ordnet krystal selv være perfekt ordnede; ud fra et entropisk perspektiv kan dette betragtes som en del af definitionen af en “perfekt krystal”. Kun ferromagnetiske, antiferromagnetiske og diamagnetiske materialer kan opfylde denne betingelse. Ferromagnetiske materialer har imidlertid ikke rent faktisk nul entropi ved nul temperatur, fordi de uparrede elektroners spins alle er rettet ind efter hinanden, og dette giver en spindegeneration i grundtilstanden. Materialer, der forbliver paramagnetiske ved 0 K, kan derimod have mange næsten degenererede grundtilstande (f.eks. i et spinglas), eller de kan bevare dynamisk uorden (en kvantespinvæske).