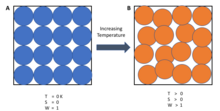
Enklare uttryckt säger den tredje lagen att entropin hos en perfekt kristall av ett rent ämne närmar sig noll när temperaturen närmar sig noll. Justeringen av en perfekt kristall lämnar ingen tvetydighet om var och hur varje del av kristallen är placerad och orienterad. När kristallens energi minskar reduceras de enskilda atomernas vibrationer till ingenting och kristallen blir densamma överallt.
Den tredje lagen ger en absolut referenspunkt för bestämning av entropin vid alla andra temperaturer. Entropin i ett slutet system, bestämd i förhållande till denna nollpunkt, är då systemets absoluta entropi. Matematiskt sett är den absoluta entropin för ett system vid nolltemperatur den naturliga loggen av antalet grundtillstånd gånger Boltzmanns konstant kB = 1,38×10-23 J K-1.
Entropen för ett perfekt kristallgitter enligt Nernsts sats är noll under förutsättning att dess grundtillstånd är unikt, eftersom ln(1)=0. Om systemet består av en miljard atomer, alla likadana, och ligger inom matrisen för en perfekt kristall, är antalet kombinationer av en miljard identiska saker som tas en miljard åt gången Ω = 1. Därav:
S – S 0 = k B ln Ω = k B ln 1 = 0 {\displaystyle S-S_{0}=k_{\text{B}}}\ln \Omega =k_{\text{B}}}\ln {1}=0}

Differensen är noll, och därför kan den initiala entropin S0 vara vilket valfritt värde som helst så länge som alla andra sådana beräkningar inkluderar detta som initial entropi. Som ett resultat av detta väljs det initiala entropivärdet noll S0 = 0 används för enkelhetens skull.
S – S 0 = S – 0 = 0 {\displaystyle S-S_{0}=S-0=0}

S = 0 {\displaystyle S=0}

Exempel : Entropiförändring av ett kristallgitter som värms upp av en inkommande fotonRedigera
Anta ett system som består av ett kristallgitter med volymen V av N identiska atomer vid T = 0 K, och en inkommande foton med våglängd λ och energi ε.
Initialt finns det bara ett tillgängligt mikrotillstånd :
S 0 = k B ln Ω = k B ln 1 = 0 {\displaystyle S_{0}=k_{\text{B}}\ln \Omega =k_{\text{B}}\ln {1}=0}

.
Låt oss anta att kristallgitteret absorberar den inkommande fotonen. Det finns en unik atom i gallret som interagerar och absorberar denna foton. Så efter absorptionen finns det N möjliga mikrotillstånd som är tillgängliga för systemet, var och en av mikrotillstånden motsvarar en exciterad atom, och de andra atomerna stannar kvar i grundtillstånd.
Entropen, energin och temperaturen i det slutna systemet stiger och kan beräknas. Entropiförändringen är:
Δ S = S – S 0 = k B ln Ω {\displaystyle \Delta S=S-S_{0}=k_{\text{B}}\ln {\Omega }}

Från termodynamikens andra lag:
Δ S = S – S 0 = δ Q T {\displaystyle \Delta S=S-S_{0}={\frac {\delta Q}{T}}}}

Hence:
Δ S = S – S 0 = k B ln ( Ω ) = δ Q T {\displaystyle \Delta S=S-S_{0}=k_{\text{B}}\ln(\Omega )={\frac {\delta Q}{T}}}

Beräkning av entropiförändring:
S – 0 = k B ln N = 1.38 × 10 – 23 × ln ( 3 × 10 22 ) = 70 × 10 – 23 J K – 1 {\displaystyle S-0=k_{\text{B}}\ln {N}=1.38\times 10^{-23}\times \ln {(3\times 10^{22})}=70\times 10^{-23}\,\mathrm {J} \,\mathrm {K} ^{-1}}

Vi antar att N = 3 – 1022 och λ = 1 cm . Systemets energiförändring till följd av absorptionen av den enda fotonen vars energi är ε:
δ Q = ϵ = h c λ = 6.62 × 10 – 34 J ⋅ s × 3 × 10 8 m s – 1 0,01 m = 2 × 10 – 23 J {\displaystyle \delta Q=\epsilon ={\frac {hc}{\lambda }}={\frac {6.62\times 10^{-34}\,\mathrm {J} \cdot \mathrm {s} \times 3\times 10^{8}\,\mathrm {m} \,\mathrm {s} ^{-1}}}{0.01\,\mathrm {m} }}=2\times 10^{-23}\,\mathrm {J} }

Temperaturen i det slutna systemet stiger med:
T = ϵ Δ S = 2 × 10 – 23 J 70 × 10 – 23 J K – 1 = 0,02857 K {\displaystyle T={\frac {\epsilon }{\Delta S}}={\frac {2\times 10^{-23}\,\mathrm {J} }{70\times 10^{-23}\,\mathrm {J} \,\mathrm {K} ^{-1}}}}=0.02857\,\mathrm {K}} }

Detta kan tolkas som systemets medeltemperatur över området från 0 < S < 70 × 10 – 23 J K – 1 {\displaystyle 0<S<70\times 10^{-23}\,\mathrm {J} \,\mathrm {K} ^{-1}}

. En enda atom antogs absorbera fotonen, men temperatur- och entropiförändringen karakteriserar hela systemet.
System med icke-noll entropi vid absolut nollEdit
Ett exempel på ett system som inte har ett unikt grundtillstånd är ett system vars nettospin är ett halvt heltal, för vilket tidsomvändningssymmetri ger två degenererade grundtillstånd. För sådana system är entropin vid nolltemperatur minst kB ln(2) (vilket är försumbart på en makroskopisk skala). Vissa kristallina system uppvisar geometrisk frustration, där kristallgitterets struktur förhindrar uppkomsten av ett unikt grundtillstånd. Helium i grundtillstånd förblir flytande (såvida det inte är under tryck).
Det är dessutom så att glasögon och fasta lösningar behåller en stor entropi vid 0 K, eftersom de är stora samlingar av nästan degenererade tillstånd, i vilka de blir instängda utanför jämvikten. Ett annat exempel på ett fast ämne med många nästan degenererade grundtillstånd, som är fångade utanför jämvikt, är is Ih, som har ”protonstörning”.
För att entropin vid den absoluta nollpunkten ska vara noll måste de magnetiska momenten i en perfekt ordnad kristall i sig själva vara perfekt ordnade; ur ett entropiskt perspektiv kan detta anses vara en del av definitionen av en ”perfekt kristall”. Endast ferromagnetiska, antiferromagnetiska och diamagnetiska material kan uppfylla detta villkor. Ferromagnetiska material har dock i själva verket inte noll entropi vid noll temperatur, eftersom de oparade elektronernas spinn är alla likriktade och detta ger en spinndegeneration i grundtillståndet. Material som förblir paramagnetiska vid 0 K kan däremot ha många nästan degenererade grundtillstånd (t.ex. i ett spinnglas) eller kan behålla dynamisk oordning (en kvantspinnvätska).