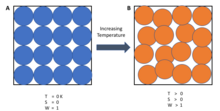
En términos simples, la tercera ley establece que la entropía de un cristal perfecto de una sustancia pura se aproxima a cero a medida que la temperatura se acerca a cero. La alineación de un cristal perfecto no deja ninguna ambigüedad en cuanto a la ubicación y orientación de cada parte del cristal. Al reducirse la energía del cristal, las vibraciones de los átomos individuales se reducen a la nada, y el cristal se vuelve igual en todas partes.
La tercera ley proporciona un punto de referencia absoluto para la determinación de la entropía a cualquier otra temperatura. La entropía de un sistema cerrado, determinada en relación con este punto cero, es entonces la entropía absoluta de ese sistema. Matemáticamente, la entropía absoluta de cualquier sistema a temperatura cero es el logaritmo natural del número de estados básicos multiplicado por la constante de Boltzmann kB = 1,38×10-23 J K-1.
La entropía de una red cristalina perfecta definida por el teorema de Nernst es cero siempre que su estado básico sea único, porque ln(1)=0. Si el sistema está compuesto por un billón de átomos, todos iguales, y se encuentran dentro de la matriz de un cristal perfecto, el número de combinaciones de un billón de cosas idénticas tomadas un billón a la vez es Ω = 1. Por lo tanto:
S – S 0 = k B ln Ω = k B ln 1 = 0 {\displaystyle S-S_{0}=k_{text{B}}ln \Omega =k_{text{B}}ln {1}=0}

La diferencia es cero, por lo que la entropía inicial S0 puede ser cualquier valor seleccionado siempre que todos los demás cálculos de este tipo lo incluyan como entropía inicial. Como resultado, el valor de entropía inicial de cero se selecciona S0 = 0 se utiliza para la conveniencia.
S – S 0 = S – 0 = 0 {\displaystyle S-S_{0}=S-0=0}

S = 0 {\displaystyle S=0}

Ejemplo : Cambio de entropía de una red cristalina calentada por un fotón entranteEditar
Supongamos un sistema formado por una red cristalina con volumen V de N átomos idénticos a T = 0 K, y un fotón entrante de longitud de onda λ y energía ε.
Inicialmente, sólo hay un microestado accesible :
S 0 = k B ln Ω = k B ln 1 = 0 {\displaystyle S_{0}=k_{text{B}}ln \Omega =k_{text{B}}ln {1}=0}

.
Supongamos que la red cristalina absorbe el fotón entrante. Hay un único átomo en la red que interactúa y absorbe este fotón. Así que después de la absorción, hay N posibles microestados accesibles por el sistema, cada uno de los microestados correspondientes a un átomo excitado, y los otros átomos que permanecen en el estado de tierra.
La entropía, la energía y la temperatura del sistema cerrado aumentan y se pueden calcular. El cambio de entropía es:
Δ S = S – S 0 = k B ln Ω {\displaystyle \Delta S=S-S_{0}=k_{text{B}}ln {\Omega }}

De la segunda ley de la termodinámica:
Δ S = S – S 0 = δ Q T {\displaystyle \Delta S=S-S_{0}={frac {\delta Q}{T}}

Por lo tanto:
Δ S = S – S 0 = k B ln ( Ω ) = δ Q T {\displaystyle \Delta S=S-S_{0}=k_{text{B}}ln(\mega )={\frac {\delta Q}{T}}

Calculando el cambio de entropía:
S – 0 = k B ln N = 1.38 × 10 – 23 × ln ( 3 × 10 22 ) = 70 × 10 – 23 J K – 1 {\displaystyle S-0=k_{texto{B}}ln {N}=1,38 veces 10^{-23} {ln {(3 veces 10^{22})}=70 veces 10^{-23},\mathrm {J} \…y el de la matriz K. ^{-1}}

Suponemos N = 3 – 1022 y λ = 1 cm . El cambio de energía del sistema como resultado de absorber el único fotón cuya energía es ε:
δ Q = ϵ = h c λ = 6.62 × 10 – 34 J ⋅ s × 3 × 10 8 m s – 1 0,01 m = 2 × 10 – 23 J {\displaystyle \delta Q=\epsilon ={frac {hc}{\lambda }}={frac {6,62\times 10^{-34}\,\mathrm {J} \3 veces 10^8},mathrm {m} \^{-1} {0,01} {mathrm}} = 2 veces 10^23}, «Matriz». }

La temperatura del sistema cerrado aumenta en:
T = ϵ Δ S = 2 × 10 – 23 J 70 × 10 – 23 J K – 1 = 0,02857 K {\displaystyle T={frac {\epsilon }{Delta S}}={frac {2\times 10^{-23},\mathrm {J} 70 veces 10^23},\Nmathrm {J} \…de la matriz K. ^{-1}}=0,02857,\Nmathrm {K} }

Esto puede interpretarse como la temperatura media del sistema en el rango de 0 < S < 70 × 10 – 23 J K – 1 {\displaystyle 0<S<70\times 10^{-23}\mathrm {J} \N – Matriz {K} ^{-1}}

. Se ha supuesto que un solo átomo absorbe el fotón, pero la temperatura y el cambio de entropía caracterizan a todo el sistema.
Sistemas con entropía no nula en el cero absolutoEditar
Un ejemplo de un sistema que no tiene un único estado básico es uno cuyo espín neto es un semi-integro, para el que la simetría de inversión del tiempo da dos estados básicos degenerados. Para tales sistemas, la entropía a temperatura cero es al menos kB ln(2) (que es despreciable a escala macroscópica). Algunos sistemas cristalinos presentan frustración geométrica, en la que la estructura de la red cristalina impide la aparición de un único estado básico. El helio en estado básico (a menos que esté bajo presión) permanece líquido.
Además, los vidrios y las soluciones sólidas retienen una gran entropía a 0 K, porque son grandes colecciones de estados casi degenerados, en los que quedan atrapados fuera del equilibrio. Otro ejemplo de un sólido con muchos estados básicos casi degenerados, atrapados fuera del equilibrio, es el hielo Ih, que tiene «desorden de protones».
Para que la entropía en el cero absoluto sea cero, los momentos magnéticos de un cristal perfectamente ordenado deben estar ellos mismos perfectamente ordenados; desde una perspectiva entrópica, esto puede considerarse parte de la definición de un «cristal perfecto». Sólo los materiales ferromagnéticos, antiferromagnéticos y diamagnéticos pueden satisfacer esta condición. Sin embargo, los materiales ferromagnéticos no tienen, de hecho, entropía cero a temperatura cero, porque los espines de los electrones no apareados están todos alineados y esto da una degeneración del espín en estado básico. Los materiales que permanecen paramagnéticos a 0 K, por el contrario, pueden tener muchos estados básicos casi degenerados (por ejemplo, en un cristal de espín), o pueden conservar el desorden dinámico (un líquido de espín cuántico).