Viskoelasticitet er en egenskab ved menneskeligt blod, der primært skyldes den elastiske energi, der er lagret i deformationen af de røde blodlegemer, når hjertet pumper blodet gennem kroppen. Den energi, der overføres til blodet af hjertet, lagres delvist i den elastiske struktur, en anden del spredes af viskositeten, og den resterende energi lagres i blodets kinetiske bevægelse. Når der tages hensyn til hjertets pulsation, bliver et elastisk regime klart tydeligt. Det er blevet vist, at den tidligere opfattelse af blodet som en rent viskos væske var utilstrækkelig, da blodet ikke er en almindelig væske. Blod kan mere præcist beskrives som en fluidiseret suspension af elastiske celler (eller en sol).
De røde blodlegemer optager omkring halvdelen af blodets volumen og besidder elastiske egenskaber. Denne elastiske egenskab er den største bidragende faktor til blodets viskoelastiske opførsel. Den store volumenprocent af røde blodlegemer ved et normalt hæmatokritniveau giver kun lidt plads til cellens bevægelse og deformation uden at interagere med en nabocelle. Beregninger har vist, at den maksimale volumenprocent af røde blodlegemer uden deformation er 58 %, hvilket ligger inden for de normalt forekommende niveauer. På grund af det begrænsede rum mellem de røde blodlegemer er det indlysende, at for at blodet kan flyde, vil en betydelig interaktion mellem cellerne spille en afgørende rolle. Denne interaktion og tendensen til, at cellerne aggregerer, er en vigtig faktor, der bidrager til blodets viskoelastiske adfærd. Deformation og aggregering af røde blodlegemer er også koblet sammen med strømningsinducerede ændringer i arrangementet og orienteringen som en tredje vigtig faktor for blodets viskoelastiske opførsel. Andre faktorer, der bidrager til blodets viskositetsegenskaber, er plasmaviskositeten, plasmasammensætningen, temperaturen og strømningshastigheden eller forskydningshastigheden. Tilsammen gør disse faktorer det menneskelige blod viskoelastisk, ikke-newtonsk og thixotropisk.
Når de røde blodlegemer er i hvile eller ved meget små forskydningshastigheder, har de en tendens til at aggregere og stable sig sammen på en energimæssigt gunstig måde. Tiltrækningen tilskrives ladede grupper på cellernes overflade og tilstedeværelsen af fibrinogen og globuliner. Denne aggregerede konfiguration er et arrangement af celler med den mindste mængde deformation. Ved meget lave forskydningshastigheder domineres blodets viskoelastiske egenskaber af aggregeringen, og cellernes deformerbarhed er relativt ubetydelig. Efterhånden som forskydningshastigheden øges, begynder aggregaternes størrelse at falde. Ved en yderligere stigning i forskydningshastigheden vil cellerne omarrangere og orientere sig for at skabe kanaler, som plasmaet kan passere igennem, og som cellerne kan glide igennem. I dette område med lav til middelhøj skubhastighed bevæger cellerne sig i forhold til nabocellerne, hvilket muliggør flow. Aggregationsegenskabernes indflydelse på viskoelasticiteten mindskes, og de røde cellers deformerbarhed begynder at få større indflydelse. Når forskydningshastigheden bliver stor, vil de røde blodlegemer strække eller deformere sig og tilpasse sig strømmen. Der dannes cellelag, der er adskilt af plasma, og strømningen tilskrives nu lag af celler, der glider på lag af plasma. Cellelaget gør det lettere for blodet at strømme, og der er således en reduceret viskositet og en reduceret elasticitet. Blodets viskoelasticitet er domineret af de røde blodlegemers deformerbarhed.
Maxwell-modelRediger
Maxwell-modellen vedrører Maxwell-væsker eller Maxwell-materiale. Materialet i Maxwell-modellen er en væske, hvilket betyder, at det respekterer kontinuitetsegenskaber for konservative ligninger : Fluider er en delmængde af materiens faser og omfatter væsker, gasser, plasmaer og, til en vis grad, plastiske faste stoffer. Maxwell-modellen er lavet til at vurdere lokale konservative værdier af viskoelasticitet ved hjælp af et globalt mål i modellens integralvolumen, der kan overføres til forskellige strømningssituationer. Blod er et komplekst materiale, hvor forskellige celler, f.eks. røde blodlegemer, er diskontinuerlige i plasma. Deres størrelse og form er også uregelmæssig, fordi de ikke er perfekte kugler. De røde blodlegemer er heller ikke identisk fordelt i en blodprøve, fordi de vandrer med hastighedsgradienter i retning af de områder med den højeste hastighed, som kaldes den berømte Fåhræus-Lindqvist-effekt, og de aggregerer eller adskiller sig i kappe- eller proppestrømme, der er beskrevet af Thurston. Typisk betragtes materialet (ensartet blå farve) i den nedenfor beskrevne Maxwell-model ensartet som en perfekt distribueret væske med partikler overalt i volumenet (i blå farve), men Thurston afslører, at pakker af røde blodlegemer, propper, er mere til stede i området med høj hastighed, hvis y er højderetningen i Maxwell-modellens figur (y~H), og der er et frit cellelag i området med lavere hastighed (y~0), hvilket betyder, at plasmavæsken, der deformeres under Maxwell-modellen, er spændt efter indre foringer, der helt undslipper Maxwells analytiske model.
I teorien opfører en væske i en Maxwell-model sig nøjagtigt på samme måde i enhver anden strømningsgeometri som f.eks. rør, roterende celler eller i hviletilstand. Men i praksis varierer blodets egenskaber med geometrien, og blod har vist sig at være et utilstrækkeligt materiale til at blive studeret som en væske i almindelig forstand. Så Maxwell-modellen giver tendenser, der skal suppleres i den virkelige situation, efterfulgt af Thurston-modellen i et kar med hensyn til fordeling af celler i kappe- og propstrømme.
Hvis man betragter et lille kubisk blodvolumen med kræfter, der påvirkes af hjertets pumpekraft og forskydningskræfter fra grænserne. Ændringen i kubens form vil have 2 komponenter:
- Elastisk deformation, som kan genvindes og er lagret i blodets struktur.
- Slipning, som er forbundet med en kontinuerlig tilførsel af viskøs energi.
Når kraften fjernes, vil kuben delvis genvinde sig selv. Den elastiske deformation er vendt, men det er glidningen ikke. Dette forklarer, hvorfor den elastiske del kun er mærkbar i ustadig strømning. I stabil strømning vil glidningen fortsætte med at stige, og målingerne af den ikke tidsvarierende kraft vil negligere bidragene fra elasticiteten.

Figur 1 kan bruges til at beregne følgende parametre, der er nødvendige for vurderingen af blodet, når der udøves en kraft.
Skubspænding: τ = F A {\displaystyle \tau ={\frac {F}{A}}}

Skærespænding: γ = D H {\displaystyle \gamma ={\frac {D}{H}}}}

Forskydningshastighed: γ ˙ = V H {\displaystyle {\dot {\gamma }}}={\frac {V}{H}}}}

En sinusformet tidsvarierende strømning anvendes til at simulere pulseringen af et hjerte. Et viskoelastisk materiale, der udsættes for en tidsvarierende strømning, vil resultere i en fasevariation mellem τ {\displaystyle \tau }

og γ {\displaystyle \gamma }

repræsenteret ved ϕ {\\displaystyle \phi }

. Hvis ϕ = 0 {\displaystyle \phi =0}

, er materialet et rent elastisk materiale, fordi spændinger og deformationer er i fase, således at den ene reaktion forårsaget af den anden er umiddelbar. Hvis ϕ {\displaystyle \phi }

= 90°, er materialet et rent viskøst, fordi deformationen halter 90 grader efter spændingen. Et viskoelastisk materiale vil ligge et sted mellem 0 og 90 grader.
Den sinusformede tidsvariation er proportional med e i ω t {\displaystyle e^{i\omega t}}

. Derfor beskrives størrelses- og faseforholdet mellem spænding, belastning og forskydningshastighed ved hjælp af dette forhold og en radiusfrekvens, ω = 2 π f {\displaystyle \omega =2\pi f}

var f {\displaystyle f}

er frekvensen i hertz. Skubspænding: τ ∗ = τ e – i ϕ {\displaystyle \tau ^{*}=\tau e^{-i\phi }}

Skydespænding: γ ∗ = γ e – i π 2 {\displaystyle \gamma ^{*}=\gamma e^{-i{\frac {\pi }{2}}}}

Forskydningshastighed: γ ˙ ∗ = γ ˙ e – i 0 {\displaystyle {\dot {\gamma }}^{*}={\dot {\gamma }}e^{-i0}}}

Komponenterne af den komplekse forskydningsspænding kan skrives som:
τ ∗ = τ τ ′ – i τ ″ {\displaystyle \tau ^{*}}=\tau ‘-i\tau ”}

Hvor τ ′ {\displaystyle \tau ‘}

er den viskose spænding og τ ″ {\displaystyle \tau ”}

er den elastiske spænding.Den komplekse viskositetskoefficient η ∗ {\displaystyle \eta ^{*}}

kan findes ved at tage forholdet mellem den komplekse forskydningsspænding og den komplekse forskydningshastighed: η ∗ = τ ∗ γ ˙ ˙ ∗ = ( τ ′ γ ˙ + i τ ″ γ ˙ ˙ ) = η ′ + i η ″ {\displaystyle \eta ^{*}={\frac {\tau ^{*}}}{{{\dot {\gamma }}}^{*}}}}}=({\frac {\tau ‘}{\dot {\gamma }}}+i{\frac {\tau ”}{\dot {\gamma }}}})=\eta ‘+i\eta ”}

Det komplekse dynamiske modul G kan ligeledes fås ved at tage forholdet mellem den komplekse forskydningsspænding og den komplekse forskydningsforstrækning.
G = τ ∗ γ ∗ = ( τ ″ γ + i τ ′ γ ) {\displaystyle G={\frac {\tau ^{*}}}{\gamma ^{*}}}}=({\frac {\tau ”}{\gamma }}+i{\frac {\tau ‘}{\gamma }})}

Gennem at relatere ligningerne til almindelige viskoelastiske termer får vi lagringsmodulet G’ og tabsmodulet G”.
G = G ′ + i G ″ {\displaystyle G=G’+iG”}

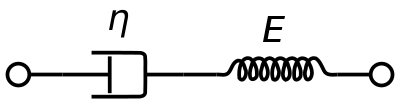
En viskoelastisk Maxwell-materiale-model anvendes almindeligvis til at repræsentere de viskoelastiske egenskaber ved blod. Den anvender en rent viskos dæmper og en rent elastisk fjeder, der er forbundet i serie. Analyse af denne model giver den komplekse viskositet i form af dashpotkonstanten og fjederkonstanten.
η ∗ = η d a s h 1 + i ω ( η d a s h E s p r i n g ) = η ′ – i η ″ {\displaystyle \eta ^{*}={\frac {\eta _{dash}}}{1+i\omega ({\frac {\eta _{dash}}}{E_{fjeder}}}})}}=\eta ‘-i\eta ”}

Oldroyd-B modelEdit
En af de mest anvendte konstitutive modeller for blodets viskoelasticitet er Oldroyd-B modellen. Der findes flere variationer af den ikke-newtonske Oldroyd-B-model, der karakteriserer forskydningsudtyndingsadfærd som følge af aggregering og dispersion af røde blodlegemer ved lav forskydningshastighed. Her betragtes en tredimensionel Oldroyd-B-model koblet med impulsligningen og den samlede spændingstensor. Der anvendes en ikke-newtonsk strømning, som sikrer, at blodets viskositet μ ( h , d ) {\displaystyle \mu (h,d)}

er en funktion af kardiameteren d og hæmatokriten h. I Oldroyd-B-modellen er forholdet mellem forskydningsspændingstensor B og orienteringsspændingstensor A givet ved:
S + γ = μ ( h , d ) – g A + C 1 ( g A – C 2 I μ ( h , d ) 2 ) {\displaystyle S+\gamma \left=\mu (h,d)\left-gA+C_{1}\left(gA-{\frac {C_{2}I}{\mu (h,d)^{2}}}}\right)}

hvor D/Dt er den materielle afledning, V er væskens hastighed, C1, C2, g, γ {\displaystyle \gamma }

er konstanter. S og B er defineret som følger: S = μ B + g A {\displaystyle S=\mu B+gA}

B = Δ V + ( Δ V ) T {\displaystyle B=\Delta V+(\Delta V)^{T}}

Viscoelasticitet af røde blodlegemerRediger
Røde blodlegemer er udsat for intens mekanisk stimulering fra både blodstrømmen og karvæggene, og deres reologiske egenskaber er vigtige for deres effektivitet i udførelsen af deres biologiske funktioner i mikrocirkulationen. Det er blevet påvist, at røde blodlegemer i sig selv udviser viskoelastiske egenskaber. Der er flere metoder, der anvendes til at undersøge de mekaniske egenskaber af røde blodlegemer, f.eks:
- mikropipetteaspiration
- mikroindtrækning
- optiske pincetter
- højfrekvente elektriske deformationstest
Disse metoder arbejdede med at karakterisere de røde blodcellers deformationsmuligheder i form af forskydnings-, bøjnings-, bøjnings-, arealudvidelsesmoduler og afslapningstider. De var imidlertid ikke i stand til at undersøge de viskoelastiske egenskaber. Der er blevet anvendt andre teknikker som f.eks. fotoakustiske målinger. Ved denne teknik anvendes en laserstråle med en enkelt impuls til at generere et fotoakustisk signal i væv, og signalets henfaldstid måles. I henhold til teorien om lineær viskoelasticitet er henfaldstiden lig med viskositets-elasticitetsforholdet, og derfor kunne de røde blodlegemers viskoelastiske egenskaber opnås.
En anden eksperimentel teknik, der blev anvendt til at vurdere viskoelasticiteten, bestod i at anvende ferromagnetiske perler, der var bundet til en celleoverflade. Der påføres derefter kræfter på den magnetiske perle ved hjælp af optisk magnetisk vridningscytometri, hvilket gjorde det muligt for forskerne at undersøge de røde blodlegemers tidsafhængige reaktioner.
T s ( t ) {\displaystyle T_{s}(t)}

er det mekaniske drejningsmoment pr. enhed perlevolumen (enheder af spænding) og er givet ved: T s ( t ) = c H cos θ {\displaystyle T_{s}(t)=cH\cos \theta }

hvor H er det påførte magnetiske drejningsfelt, θ {\displaystyle {\theta }}

er vinklen af perlens magnetiske moment i forhold til den oprindelige magnetiseringsretning, og c er perlekonstanten, som findes ved eksperimenter udført ved at placere perlen i en væske med kendt viskositet og anvende et vridningsfelt.
Det komplekse dynamiske modul G kan anvendes til at repræsentere relationerne mellem svingende spænding og belastning:
G = G ′ + i G ″ {\displaystyle G=G’+iG”}

hvor G ′ {\displaystyle G’}

er lagringsmodulet og G ″ {\displaystyle G”}

er tabsmodulet: G ′ = σ 0 ε 0 ε 0 cos ϕ {\displaystyle G’={{\frac {\sigma _{0}}}{\varepsilon _{0}}}}\cos \phi }

G ″ = σ 0 ε 0 ε 0 sin ϕ {\displaystyle G”={\frac {\sigma _{0}}}{\varepsilon _{0}}}}\sin \phi }

hvor σ 0 {\displaystyle \sigma _{0}}

og ε 0 {\displaystyle \varepsilon _{0}}

er amplituderne af spændinger og deformationer og ϕ {\\displaystyle \phi }

er faseforskydningen mellem dem.

Fra ovenstående relationer bestemmes komponenterne af det komplekse modul ud fra en sløjfe, der dannes ved at sammenligne ændringen i drejningsmomentet med ændringen i tiden, som danner en sløjfe, når den repræsenteres grafisk. Grænserne for T s ( t ) {\displaystyle T_{s}(t)}

– d(t)-sløjfen og det område, A, der er afgrænset af T s ( t ) {\displaystyle T_{s}(t)}

– d(t)-sløjfen, som repræsenterer energispildet pr. cyklus, anvendes i beregningerne. Fasevinklen ϕ {\displaystyle \phi }

, lagermodulet G’ og tabsmodulet G bliver derefter: ϕ = sin – 1 4 A π Δ T s Δ d {\displaystyle \phi =\sin ^{-1}{\frac {4A}{\pi \Delta T_{s}\Delta d}}}}

G ′ = Δ T s Δ d cos ϕ {\displaystyle G’={{\frac {\Delta T_{s}}}{\Delta d}}}\cos \phi }

G ″ = Δ T s Δ d sin ϕ = 4 A π ω Δ d 2 {\displaystyle G”={\frac {\Delta T_{s}}}{\Delta d}}\sin \phi ={\frac {4A}{\pi \omega \Delta d^{2}}}}

hvor d er forskydningen.
Hysteresen vist i figur 3 repræsenterer den viskoelasticitet, der er til stede i røde blodlegemer. Det er uklart, om dette er relateret til molekylære membranfluktuationer eller metabolisk aktivitet, der styres af intracellulære koncentrationer af ATP. Der er behov for yderligere forskning for at udforske denne interaktion fuldt ud og for at kaste lys over de underliggende viskoelastiske deformationsegenskaber i de røde blodlegemer.
Effekter af blodkarRediger
Når man ser på blodets viskoelastiske opførsel in vivo, er det nødvendigt også at overveje virkningerne af arterier, kapillærer og vener. Blodets viskositet har en primær indflydelse på strømningen i de større arterier, mens elasticiteten, som ligger i de røde blodlegemers elastiske deformerbarhed, har primær indflydelse i arteriolerne og kapillærerne. Forståelse af bølgeudbredelsen i arterievæggene, den lokale hæmodynamik og vægskubspændingsgradienten er vigtig for forståelsen af mekanismerne bag den kardiovaskulære funktion. Arterievæggene er anisotrope og heterogene og består af lag med forskellige biomekaniske egenskaber, hvilket gør det meget vanskeligt at forstå de mekaniske påvirkninger, som arterierne bidrager til blodstrømningen.
Medicinske grunde til en bedre forståelseRediger
Fra et medicinsk synspunkt bliver vigtigheden af at studere blodets viskoelastiske egenskaber indlysende. Med udviklingen af kardiovaskulære proteser, såsom hjerteklapper og blodpumper, er det nødvendigt at forstå pulserende blodstrømning i komplekse geometrier. Et par specifikke eksempler er virkningerne af blodets viskoelastiske egenskaber og deres betydning for afprøvning af pulserende blodpumper. Der er dokumenteret stærke korrelationer mellem blodets viskoelasticitet og regional og global cerebral blodgennemstrømning under kardiopulmonal bypass.
Dette har også banet vejen for udvikling af en blodanalog for at studere og afprøve proteser. Den klassiske analog af glycerin og vand giver en god repræsentation af viskositet og inertialeffekter, men mangler de elastiske egenskaber af ægte blod. En sådan blodanalog er en vandig opløsning af xanthangummi og glycerin, der er udviklet til at matche både de viskose og elastiske komponenter i blodets komplekse viskositet.
Normale røde blodlegemer er deformerbare, men mange tilstande, som f.eks. seglcellesygdom, reducerer deres elasticitet, hvilket gør dem mindre deformerbare. Røde blodlegemer med nedsat deformerbarhed har en stigende strømningshindring, hvilket fører til en stigning i aggregering af røde blodlegemer og nedsat iltmætning, hvilket kan føre til yderligere komplikationer. Tilstedeværelsen af celler med nedsat deformerbarhed, som det er tilfældet ved seglcellesygdom, har en tendens til at hæmme dannelsen af plasmalag, og ved at måle viskoelasticiteten kan graden af hæmning kvantificeres.
HistorikRediger
I tidligt teoretisk arbejde blev blod behandlet som en ikke-newtonsk viskøs væske. De første undersøgelser havde evalueret blod under stationær strømning og senere ved hjælp af svingende strømning. Professor George B. Thurston fra University of Texas præsenterede først ideen om, at blod er viskoelastisk, i 1972. De tidligere undersøgelser af blod under stabil strømning viste ubetydelige elastiske egenskaber, fordi det elastiske regime er lagret i blodet under påbegyndelsen af strømningen, og dets tilstedeværelse er derfor skjult, når strømningen når stabil tilstand. De tidlige undersøgelser brugte de egenskaber, der blev fundet ved stabil strømning, til at udlede egenskaber for ustabile strømningssituationer. Udviklingen inden for medicinske procedurer og medicinsk udstyr krævede en bedre forståelse af blodets mekaniske egenskaber.