Cyklopentan Kemiska egenskaper, användning, produktion
Fysikaliska och kemiska egenskaper
Cyklopentan, även känt som ”pentametylen”, är ett slags cykloalkan med formeln C5H10. Den har en molekylvikt på 70,13. Den förekommer som en slags brandfarlig vätska. Den har en smältpunkt på 94,4 °C, en kokpunkt på 49,3 °C, en relativ densitet på 0,7460 och ett brytningsindex på 1,4068. Den är löslig i alkohol, eter och kolväten och är inte löslig i vatten. Cyklopentan är inte en planär ring och har två konformationer: kuvertkonformationer och halvstols-konformationer. Kol-kol-kol-bindningsvinkeln är nära 109 ° 28 ’ med en molekylär spänning som inte är stor och ringen är relativt stabil. Den har liknande kemiska egenskaper som alkaner. Den dödliga koncentrationen i luften för råttorna var 3,8 × 10-2. Den uppvisar en rödgul färg vid reaktion med rykande svavelsyra samtidigt som den genererar nitrocyklopentan och glutarsyra vid reaktion med salpetersyra. Metod: Det kan erhållas från petroleumeterdestillat genom högtryckskrackning av cyklohexan i närvaro av aluminium eller katalytisk hydrering av cyklopenten och cyklopentadien. Användningsområden: används huvudsakligen som lösningsmedel.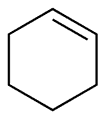
Figur 1 cyklopentans struktur.
Cykloalkan
Cykloalkaner är mättade kolväten där kolatomerna i molekylen är arrangerade i en ring och ett tillräckligt antal väteatomer är kombinerade. Cykloalkaner som förekommer i petroleum är främst cyklopentan och cyklohexan.
Cykloalkaner har en högre smältpunkt, kokpunkt och relativ densitet än motsvarande rätkedjiga alkaner. Vi kan använda den nafteniska aromatiska råoljan för att framställa högoktanig straight-run bensin vars explosionsskydd är bättre än normalt paraffin. Paraffin med låg svavelhalt och naftenisk råolja är inte bara lätt att bearbeta, utan också en utmärkt råvara för produktion av avancerade smörjmedel. Petroleum som innehåller relativt många polycykliska nafteniska föreningar med lång sidokedja är ett idealiskt material för smörjmedel av hög kvalitet.
Vid rumstemperatur och atmosfäriskt tryck är cykloalkan som innehåller fyra eller färre kolatomer i gasform och de som innehåller mer än fyra kolatomer existerar i flytande form. Cyklopropan och cyklobutan uppträder som gas, cyklopentan till cykloundekan uppträder som vätska, cyklododekan och högre uppträder som fast ämne.
Cykloalkans kemiska natur är relaterad till antalet kolatomer som bildar ringen. Det hänvisas till tre- och fyrledad ring, som liten ring; den fem- till sjuledade ringen som normal ring; den åtta-elva ringen som normal ring; den tolvledade ringen och högre som stor ring. Kolkärnornas linjer i små ringar stämmer inte överens med bindningsorbitalens axel. I cyklopropan är den ring som bildas av kolatomernas kärnor en liksidig triangel där varje vinkel är 60° medan vinkeln på axeln för sp3-hybridorbitalets axel för kol-kol enkelbindningar som bildas av varje kol är 104° (se figur 2 nedan). Därför har banan misslyckats med att uppnå den största graden av överlappning, vilket orsakar en stor vinkelspänning. Cyclobutan har också vinkelspänning, men är mindre. Detta leder till den lilla ringens dåliga stabilitet, vilket gör att den har liknande kemiska egenskaper som olefiner som kan ha en ringöppnande additionsreaktion med många reagenser. Den andra ringen har mindre eller ingen vinkelspänning. Cykloalkaner och alkaner har liknande kemiska egenskaper och är mindre benägna att ha en ringöppningsreaktion, t.ex. en reaktion med väte. Cyklohexan och högre cykloalkan är svårare att genomgå hydrogenering.
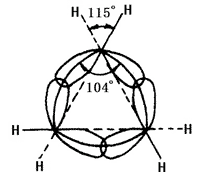
Figur 2 är en schematisk representation av sp3-hybridiseringens orbitalöverlappning i cyklopropan.
Cyklopropan (vid rumstemperatur) och cykllobutan (vid uppvärmningsförhållandena) kan ha additionsreaktion med halogen och vätehalogenid.
Den öppna slingan inträffar mellan de två atomer som förbinder det största och minsta antalet väte. Additionen uppfyller den markovska regeln. Medan den normala ringen, under stimulering av ljuset eller värmen kan ha substitutionsreaktion med halogenen.
Vid rumstemperatur kan cykloalkan inte oxideras av kaliumpermanganat.
Cyklopentan, cyklohexan och dess alkylsubstituerade produkter förekommer i vissa petroleumoljor. Cycloalkaner kan också syntetiseras genom lämpliga metoder, till exempel dihaloalkancyklisering och hydrering av aromatiska kolväten.
Denna information har redigerats av Xiaonan från Chemicalbook (2015-08-17).
Farligt läge
Intag och inandning är måttligt giftigt. (2) Är brandfarlig med större risk för förbränning. Den tillåtna koncentrationen i luft är 600 ppm (1720mg/m3) i USA.
Skadliga effekter och symtom på förgiftning
Inandning av höga koncentrationer av cyklopentan kan orsaka hämning av centrala nervsystemet, även om dess akuta toxicitet är låg. Symtom på akut exponering inkluderar först upphetsning, följt av uppkomsten av balansstörningar och till och med stupor, koma. Det finns sällan fall av dödsfall på grund av andningssvikt. Det har rapporterats att djur som utfodrats med denna vara kan få svår diarré, vilket leder till kärlkollaps i hjärta, lungor och lever samt till degeneration i hjärnan.
Skyddsåtgärder
Det kan användas för att förbättra produktionsutrustningen. Använd hudskyddskrämer eller handskar för att skydda huden.
Medicinsk vård
Vid regelbunden fysisk undersökning, var uppmärksam på potentiell irritationseffekt av hud och luftvägar samt eventuella komplikationer av njurar och lever.
Transportkrav
Brandfarlig vätska av klass I. Code of Hazard Regulations: 61013. Behållaren ska märkas med ett märke för ”brandfarlig vätska” vid transport.
Brandsläckningsmedel
Se ”cyklohexan”.
Rekommenderade metoder för avfallshantering
Förbränning;
Kemiska egenskaper
Den uppträder som färglös vätska med en smältpunkt på-93,9 °C, en kokpunkt på 49,26 °C, en relativ densitet på 0,7460 (20/4 °C), ett brytningsindex på 1,4068 och en flampunkt på-37 °C. Den är blandbar med alkohol, eter och andra organiska lösningsmedel, men är inte lätt att lösa upp i vatten.
Användningar
(1) Den kan användas som lösningsmedel för lösningspolymerisering av polyisoprengummi och cellulosaeter. Det kan användas som ersättning för Freon som isoleringsmaterial i kylskåp och frysar samt som skummedel för andra hårda PU-skum och kromatografiska analysstandarder.
(2) Används som standardsubstans för kromatografisk analys, lösningsmedel, motorbränslen, azeotropa destillationsmedel.
Produktionsmetod
Cyklopentan är en komponent i petroleumeteren i kokpunktsintervallet 30-60 °C med en halt på i allmänhet 5-10 %. Tillämpa atmosfärisk destillation vid ett återflödesförhållande på 60:1 och utför den i ett 8 meter högt torn; destillera först ut isopentan och n-pentan; fortsätt fraktioneringen för att erhålla cyklopentan med en renhet på över 98 %. Cyklopentan kan också erhållas genom reduktion av cyklopentanon eller katalytisk hydrogenering av cyklopentadien.
Faror &Säkerhetsinformation
Kategori Brandfarliga vätskor
Toxicitetsklassning: Låg toxicitet
Akut toxicitet: oral-råtta LD50: 11400 mg/kg; oral-mus LD50: 12800 mg/kg
Farliga egenskaper hos explosiva ämnen: Explosivt vid blandning med luft
Brännbarhet och farliga situationer: Brandfarligt vid brand, hög temperatur och oxidationsmedel med förbränning som frigör irriterande rök
Lagringsegenskaper: Lagringsutrymme: ventilerat, låg temperatur och torrt; lagra den med oxidationsmedel separat
Släckmedel: TWA 1720 mg/m3; STEL 2150 mg/kg
Kemiska egenskaper
Färglös vätska med bensinliknande lukt
Kemiska egenskaper
Cyklopentan är en färglös vätska.
Fysiska egenskaper
Färglös, rörlig, brandfarlig vätska med en lukt som liknar cyklohexan.
Användningar
Cyklopentan är en petroleumprodukt. Den bildas genom katalytisk krackning vid hög temperatur av cyklohexan eller genom reduktion av cyklopentadien. Den förekommer i petroleumeterfraktioner och i många kommersiella lösningsmedel och används som lösningsmedel för färg, vid extraktion av vax och fett samt inom skoindustrin.
Användningar
Som laboratoriereagens; vid tillverkning av läkemedel; förekommer i lösningsmedel och i petroleumeter; drivmedel som tryckmedel.
Produktionsmetoder
Cyklopentan förekommer i petroleumeterfraktioner och framställs genom krackning av cyklohexan i närvaro av aluminiumoxid vid hög temperatur och högt tryck eller genom reduktion av cyklopentadien.
Definition
ChEBI: En cykloalkan som består av fem kolväten som vardera är bundna med två väteämnen ovanför och under planet. Stamformen i klassen av cyklopentaner.
Allmän beskrivning
En klar färglös vätska med en petroleumliknande lukt. Flampunkt på -35°F. Mindre tät än vatten och olöslig i vatten. Ångor är tyngre än luft.
Luft & Vattenreaktioner
Lättantändligt. Olösligt i vatten.
Reaktivitetsprofil
CYKLOPENTAN är oförenligt med starka oxidationsmedel som klor, brom, fluor. .
Hälsofara
Inandning orsakar yrsel, illamående och kräkningar; koncentrerade ångor kan orsaka medvetslöshet och kollaps. Ångor orsakar lätt sveda i ögonen. Kontakt med vätska orsakar irritation i ögonen och kan irritera huden om den får sitta kvar. Intag orsakar irritation i magen. Aspiration ger allvarlig lungirritation och snabbt utvecklande lungödem; spänning i centrala nervsystemet följt av depression.
Hälsofara
Cyklopentan är ett lågakut giftigt ämne. Exponering i höga koncentrationer kan leda till depression av det centrala nervsystemet med symtom på excitabilitet, förlust av jämvikt, stupor och koma. Andningssvårigheter kan uppstå hos råttor efter 30-60 minuters exponering för 100 000-120 000 ppm i luften. Det är irriterande för de övre luftvägarna, huden och ögonen. Det finns ingen information i litteraturen om de kroniska effekterna av långvarig exponering för cyklopentan.
Brandfarlighet
Beteende vid brand: Behållare kan explodera.
Kemisk reaktivitet
Reaktivitet med vatten Ingen reaktion; Reaktivitet med vanliga material: Ingen reaktion; Stabilitet under transport: Stabil; Neutraliserande medel för syror och kaustika: Inte relevant; Polymerisering: Polymerisationshämmare: Inte relevant: Inte relevant: Polymerisationshämmare: Inte relevant.
Säkerhetsprofil
Mildt giftigt vid förtäring och inandning. Höga koncentrationer har narkotisk verkan. En mycket farlig brandrisk när den utsätts för värme eller flammor; kan reagera med oxidationsmedel. För att bekämpa brand, använd skum, CO2, torrkemikalier. Vid upphettning till nedbrytning avger den bitter rök och ångor.
Potentiell exponering
Cyklopentan används som lösningsmedel.
Källa
Beståndsdel i bensin med hög oktanhalt (citerat, Verschueren, 1983). Harley et al. (2000)analyserade headspace-ångorna från tre kvaliteter blyfri bensin där etanol tillsattes för att ersätta metyl-tert-butyleter. Cyclopentan påvisades i en identisk koncentration på 1,4 viktprocent i huvuddimmorna för normal-, medel- och premiumkvaliteterna.
Schauer et al. (1999) rapporterade cyclopentan i avgaserna från en dieseldriven medelstor lastbil med en utsläppshastighet på 410 μg/km.
California Phase II reformulerad bensin innehöll cyclopentan i en koncentration på 4,11 g/kg. Utsläppen från avgasröret i gasfas från bensindrivna bilar med och utan katalytiska omvandlare var 0,78 respektive 85,4 mg/km (Schauer et al., 2002).
Miljöförlopp
Biologiskt. Cyklopentan kan oxideras av mikrober till cyklopentanol, som kan oxideras till cyklopentanon (Dugan, 1972).
Fotolytisk. Följande hastighetskonstanter har rapporterats för reaktionen mellan oktan och OH-radikaler i atmosfären: 3,7 x 10-12 cm3/molekyl?sek vid 300 K (Hendry och Kenley, 1979); 5,40x 10-12 cm3/molekyl?sek (Atkinson, 1979); 4,83 x 10-12 cm3/molekyl?sek vid 298 K (DeMore ochBayes, 1999); 6,20 x 10-12, 5,24 x 10-12, och 4.43 x 10-12 cm3/molekyl?sek vid 298, 299 respektive 300 K (Atkinson, 1985), 5,16 x 10-12 cm3/molekyl?sek vid 298 K (Atkinson, 1990) och 5,02 x 10-12 cm3/mol-sek vid 295 K (Droege och Tilly, 1987).
Kemisk/fysisk. Cyklopentan hydrolyseras inte eftersom det inte har någon hydrolyserbar funktionell grupp. Fullständig förbränning i luft ger koldioxid och vatten.
Vid förhöjda temperaturer bryts ringen och bildar eten och förmodligen allene och väte (Rice och Murphy, 1942).
Skeppning
UN1146 Cyklopentan, faroklass: 3; Etiketter: 3 – Brandfarlig vätska.
Reningsmetoder
Befria den från cyklopenten genom två passager genom en kolonn av noggrant torkad och avgasad aktiverad kiselgel. Den förekommer i petroleum och är MYCKET BRANDFARLIG.
Inkompatibiliteter
Kan bilda en explosiv blandning med luft, kan ackumulera statiska elektriska laddningar och kan orsaka antändning av dess ångor. Kontakt med starka oxidationsmedel kan orsaka brand och explosion.
Avfallshantering
Lös upp eller blanda materialet med ett brännbart lösningsmedel och bränn i en kemisk förbränningsugn utrustad med efterbrännare och skrubber. Alla federala, statliga och lokala miljöbestämmelser måste följas.