INLEIDING
Amyloïdose is een afzettingsziekte die wordt veroorzaakt door extracellulaire ophoping van fibrillen waarvan de bron bestaat uit eiwitten met een onstabiele structuur die zich vouwen, aggregeren en afzetten.1 Dergelijke afzettingen kunnen de weefselstructuur veranderen en de functie van verschillende organen en systemen aantasten.2
Amyloïde fibrillen zijn onoplosbaar en resistent tegen proteolyse en worden meestal gekleurd met Congo rood, waarbij ze een intense geelgroene birefringentie vertonen onder gepolariseerd licht.3 Meer dan 30 eiwitten kunnen amyloïde afzetting veroorzaken, maar slechts 5 veroorzaken significante afzetting in hartweefsel1:
- –
Lichtketens, die primaire amyloïdose (AL) veroorzaken.
- –
Transthyretine (TTR), dat TTR-amyloïdose (ATTR) veroorzaakt.
- –
Apolipoproteïne A.
- –
Fibrinogeen.
- –
Serum amyloïd-eiwit A, dat secundaire amyloïdose veroorzaakt.
Primaire amyloïdose en ATTR zijn de meest voorkomende vormen van cardiale amyloïdose, waarbij de AL-vorm historisch gezien als meer voorkomend in ontwikkelde landen wordt beschouwd.3
De meeste informatie over cardiale amyloïdose is gebaseerd op AL. Maar hoewel het aantal patiënten met AL stabiel is gebleven, is het aantal ATTR-diagnoses de laatste tijd toegenomen en men denkt nu dat ATTR veel vaker voorkomt dan AL.2
Transthyretine amyloïdose is heel vaak het onderwerp geweest van misdiagnose of aanzienlijke vertraging totdat de juiste diagnose werd gesteld. Redenen hiervoor zijn onder meer de heterogeniteit van de vormen, de noodzaak van histologische bevestiging, een tekort aan gespecialiseerde apparatuur en de onjuiste opvatting van sommige cardiologen dat het een zeldzame ziekte is zonder behandelingsmogelijkheden.2,3
Deze aspecten zijn echter aan het veranderen. De diagnose heeft gevolgen voor de behandeling van de patiënt. Er zijn specifieke therapieën ontwikkeld die de afzetting kunnen vertragen of stabiliseren en die doeltreffender zijn in de vroege stadia. Een vroege diagnose is daarom van cruciaal belang. Dit overzicht beschrijft belangrijke recente vorderingen bij de diagnose en behandeling van ATTR, die hoop bieden voor patiënten met deze aandoening.
TRANSTHYRETIN CARDIAC AMYLOIDOSIS
Transthyretine is een tetramerisch plasma-eiwit dat verantwoordelijk is voor het transport van thyroxine en retinol-gebonden eiwit. Het wordt voornamelijk gesynthetiseerd in de lever en in tweede instantie in de plexus choroidea en het pigmentepitheel van het netvlies.4
Transthyretine heeft de neiging te dissociëren tot dimeren en monomeren, die misassembleren tot fibrillen en afzetting ondergaan. Puntmutaties of het effect van leeftijd kunnen deze neiging versterken, waardoor de 2 klinische vormen van ATTR ontstaan: mutant (ATTRm) en wild-type (ATTRwt).
MUTANT TRANSTHYRETINE AMYLOIDOSIS
Meer dan 120 mutaties zijn momenteel bekend die ATTRm veroorzaken. Deze mutaties vertonen een autosomaal dominant overervingspatroon, met variabele penetrantie.4 Door de grote geografische diversiteit is het moeilijk om de prevalentie van ATTR vast te stellen, maar het wordt beschouwd als een zeldzame ziekte met een prevalentie van minder dan 1/100 000 inwoners2 (tabel 1).
De belangrijkste klinische en diagnostische kenmerken van mutant en wildtypeType Transthyretine Cardiale Amyloïdose
| ATTRwt | ATTRm | |
|---|---|---|
| Prevalentie | Onbekend. Blijkbaar zeer frequent | |
| Genetisch onderzoek | Afwezigheid van mutaties in TTR | Mutatie in TTR |
| Typische leeftijd bij presentatie | > 60 jaar | Variabel naar oorzakelijke mutatie |
| Geslacht | Mannelijke overheersing. 80% patiënten | Mannelijk overwegend, met agressiever fenotype |
| Extracardiale manifestaties | – Carpaal tunnel syndroom (33%-49%) – Lumbale spinale stenose – Traumatische bicepspeesruptuur (32%) |
– Ascenderende bilaterale sensomotorische polyneuropathie – Dysautonomie: orthostatische hypotensie, diarree-constipatie, erectiestoornissen – Betrokkenheid van de ogen: glaucoom, intravitreale depositie, gescalpeerde pupillen |
| Hartinsufficiëntie | Constant | Variabel volgens oorzakelijke mutatie |
| Hartoutput | – Hartfalen (53%-86%) – Geleidingsstoornissen – AF (43%-67%) – Degeneratieve AOS |
– Geleidingsstoornissen – Hartfalen – Infrequent AF (10%) |
| Diagnostische technieken | ||
| ECG | – Pseudoinfarctpatroon (63%-66%) – Laag voltage (22%-33%) – Sokolow LVH (6%-13%) |
– Pseudoinfarct patroon (18%-69%) – Laag voltage (2%-25%) – Sokolow LVH (3%-8%) |
| ECHO | – Matig-ernstige hypertrofie – Mild-matig gedeprimeerde LVEF (30%) |
– Matige hypertrofie – LVEF, doorgaans behouden |
| Hart-MRI | – Late versterking – Verhoogde natieve T1 en EV |
|
| 99mTc DPD scintigrafie | – Graad 2-3 | – Graad 0: asymptomatische dragers – Graad 1: initiële cardiale betrokkenheid – Graad 2-3: significante cardiale betrokkenheid |
AF, atriumfibrilleren; AoS, aortastenose; ATTRm, gemuteerde transthyretine-amyloïdose; ATTRwt, wild-type transthyretine-amyloïdose; ECG, elektrocardiogram; ECO, echocardiogram; EV, extracellulair volume; LVEF, linker ventrikel ejectiefractie; LVH, linker ventrikel hypertrofie; TTR, transthyretine.
De eerste TTR-mutaties werden gerapporteerd als familiaire amyloïde polyneuropathie (of de ziekte van Andrade), en bijgevolg werd ATTRm tot voor kort beschouwd als een neurologische aandoening. Recente bevindingen tonen echter cardiale betrokkenheid aan in meer dan de helft van de gevallen.3
Er is een sterke genotype-fenotype correlatie, waarbij mutaties geassocieerd zijn met puur neurologische ziekte of puur cardiale ziekte.3 De verdeling van ATTRm in cardiale of neurologische ziekte kan echter een oversimplificatie zijn, aangezien er aanzienlijke overlap is tussen de 2 klinische vormen in het ziektespectrum.
De Val30Met-mutatie (nu bekend als Val50Met nadat 20 posities werden toegevoegd aan de traditionele mutatienaam in ATTRm) is wereldwijd de meest frequente mutatie en is endemisch in Portugal, Japan en Zweden. De geschatte incidentie in Portugal is 1 per 538 inwoners.2 Mallorca (Spanje) en Valverde del Camino (Huelva, Spanje) worden ook beschouwd als gebieden waar ATTRm endemisch is. De geschatte prevalentie in Mallorca bij symptomatische patiënten is 3/100 000 inwoners.5
De Val30Met-mutatie veroorzaakt een overwegend neurologische aandoening met symmetrische sensomotorische polyneuropathie, die begint in de onderste ledematen en een oplopend patroon volgt. De aandoening kan gepaard gaan met dysautonomie met orthostatische hypotensie, erectiestoornissen, incontinentie voor urine en gastro-intestinale symptomen. De ziekte begint meestal aan het eind van het tweede of derde decennium van het leven, en bij 43% van de patiënten is het hart betrokken, hetgeen een frequente doodsoorzaak is4 (tabel 1).
Van bijzonder belang is de Val122Ile-mutatie (p. Val142Ile), die voorkomt bij 3% tot 4% van de Noord-Amerikaanse zwarte bevolking.3 Hoewel de penetrantie onvolledig is,3 is deze mutatie geassocieerd met een 47% verhoogd risico op het ontwikkelen van hartfalen (HF).6 Een recente studie toonde aan dat Val122Ile amyloïdose de vierde meest voorkomende oorzaak van HF was in de Britse Afro-Caribische bevolking.7 Hoewel tot 30% van de patiënten met deze mutatie kenmerken van milde neuropathie kan vertonen,6 is het klinische fenotype gewoonlijk vergelijkbaar met dat van ATTRwt.4 Val122Ile moet niet worden beschouwd als een mutatie die uitsluitend voorkomt bij de zwarte bevolking, omdat deze ook bij de blanke bevolking kan voorkomen. Wij hebben deze mutatie bijvoorbeeld geïdentificeerd in 4 blanke Spaanse families zonder zwarte voorouders.
WILD-TYPE TRANSTHYRETIN AMYLOIDOSIS
Wild-type transthyretine amyloïdose werd voor het eerst beschreven in 1876. Vroeger werd het seniele amyloïdose genoemd, maar de diagnose bij patiënten tussen 40 en 60 jaar heeft deze term verouderd gemaakt. Interessant is dat het vroegst bekende geval van deze mutatie werd gevonden bij een 47-jarige Amerikaanse patiënt.8
De precieze prevalentie van ATTRwt blijft onbekend. Studies suggereren echter dat het ondergediagnosticeerd is en dat het de meest frequente vorm van cardiale amyloïdose zou kunnen zijn.2,3 De volgende resultaten ondersteunen deze hypothese:
- –
Bij patiënten ouder dan 80 jaar is de prevalentie van TTR-afzetting 25% bij autopsie.3
- –
Bij patiënten met HF met behouden ejectiefractie (HFpEF) bedraagt de matig-ernstige TTR-depositie bij autopsie 5%.9
- –
In patiënten ouder dan 60 jaar opgenomen voor HFpEF en linker ventrikel hypertrofie (LVH) ≥ 12mm, vond onze groep recent een prevalentie van 13%.10
In tegenstelling tot ATTRm, is ATTRwt een sporadische ziekte die typisch begint na de leeftijd van 70 jaar.4 De ziekte wordt voornamelijk bij mannen aangetroffen, en gepubliceerde series hebben percentages tussen 89% en 98% gerapporteerd.11,12 In een recente serie patiënten met de diagnose ATTRwt in 2 ziekenhuizen (Madrid, Spanje en Bologna, Italië) ontdekte onze groep echter dat 20% vrouw was. Bovendien hebben andere autopsiestudies ook gesuggereerd dat ATTRwt bij vrouwen mogelijk wijder verbreid is dan eerder gerapporteerd. Daarom mag het vrouwelijk geslacht de klinische verdenking van ATTRwt niet verminderen (tabel 1).13
Autopsiebevindingen tonen aan dat TTR-depositie verspreid is in verschillende organen bij ATTRwt. De depositie is echter veel groter in het hart als gevolg van het cardiale tropisme van TTR, en cardiale betrokkenheid is de belangrijkste klinische manifestatie.4 Patiënten kunnen zich presenteren met symptomen van extracardiale TTR-depositie, zoals lumbale kanaalstenose, atraumatische ruptuur van de bicepspees of “Popeye sign”, en carpaal tunnel syndroom (CTS)3 (figuur 1). Al deze kenmerken kunnen helpen om de diagnose snel te stellen. CTS kan gepaard gaan met andere amyloïdose subtypes, maar komt vaker voor bij ATTRwt. De afzetting kan enkele jaren voorafgaan aan de cardiale manifestaties.6 Het kan als indicatie worden gebruikt bij oudere patiënten met LVH, vooral als zij bilaterale CTS hebben die niet geassocieerd is met specifieke beroepsactiviteiten en in New York Heart Association functionele klasse ≥ II zijn (ongepubliceerde gegevens).
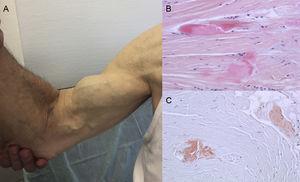
Tekenen en symptomen van transthyretine amyloïdose. A: niet-raumatische ruptuur van de rechter bicepspees (“Popeye-teken”). B en C: kleuring met hematoxyline-eosine (B) en Congo rood (C), beide ×200, van carpaal ligament monster met dichte collageenbundels met niet-cellulair materiaal. Met dank aan Dr Clara Salas Antón.
DIAGNOSIS VAN TRANSTHYRETIN AMYLOIDOSISKlinische presentatie
Amyloïd kan in elke cardiale structuur infiltreren.1 Typisch is dat door depositie de wanddikte van de hartkamers toeneemt, wat een geleidelijke afname van de distensibiliteit veroorzaakt, leidend tot ernstige diastolische disfunctie. ATTR wordt daarom traditioneel beschouwd als een oorzaak van restrictieve cardiomyopathie.
Het klinische spectrum van ATTR is echter veel breder en meer heterogeen. Het meest voorkomende symptoom van ATTR is HF. Zoals vermeld, suggereerde een studie gepubliceerd door onze groep in 2015 dat een protocol gebaseerd op 99mTc-3,3-diphosphono-1,2-propanodicarboxylic acid (99mTc-DPD) scintigrafie nuttig kan zijn voor de diagnose van ATTRwt bij een significant deel (13%) van de patiënten ouder dan 60 jaar opgenomen voor HFpEF.10 Op basis van dit resultaat werd 99mTc-DPD scintigrafie opgenomen in de Europese richtlijnen over HF van 2016 als een nuttig hulpmiddel voor de identificatie van patiënten met ATTR.14 ATTR mag echter niet uitsluitend worden verdacht bij patiënten met HFpEF omdat, naarmate de amyloïdafzetting vordert, de contractiele functie verslechtert en ATTR bijgevolg kan worden geassocieerd met verschillende graden van systolische disfunctie.
Transthyretine amyloïdose is een fenocopie van hypertrofische cardiomyopathie (HCM) en kan daarmee worden verward. Een recent multicenter Frans onderzoek meldde dat 5% van de patiënten met HCM ATTRm hebben.15 Onze resultaten komen echter niet overeen met dit hoge percentage, wat te maken zou kunnen hebben met de grote zwarte populatie in Frankrijk.
Afwijkingen in de hartgeleiding kunnen de eerste manifestatie van ATTR zijn. Amyloïd infiltratie van de sinus en atrioventriculaire knopen1 kan wijzen op de noodzaak van pacemaker implantatie (tabel 1). Uit de eerder genoemde studie in Spanje en Italië bleek dat geleidingsstoornissen de eerste manifestatie van ATTRwt waren bij 7% van de patiënten met deze ziekte.13
Atriale aritmieën komen ook zeer vaak voor bij patiënten met ATTRwt13 (figuur 2A), en de eerste manifestatie van de ziekte kan een beroerte zijn.4 De Mayo Clinic groep heeft onlangs zelfs gesuggereerd dat ATTRwt moet worden uitgesloten bij een diagnose van niet-valvulair atriumfibrilleren (AF) bij oudere patiënten.8 Daarentegen komt AF veel minder vaak voor bij patiënten met ATTRm (tabel 1).
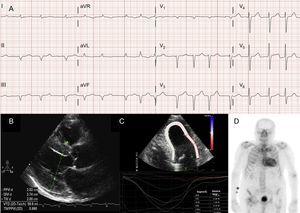
Diagnostische technieken bij transthyretine cardiale amyloïdose (ATTR). A: Elektrocardiogram van een patiënt met wild-type transthyretine-amyloïdose (ATTRwt), met atriumfibrillatie en pseudoinfarctpatroon in de afleidingen in het midden. B: echocardiogram van een patiënt met gemuteerde transthyretine-amyloïdose met Val30Met-mutatie, met duidelijke concentrische linkerventrikelhypertrofie en milde pericardiale effusie. C: longitudinale regionale stam van een patiënt met ATTRwt, met geconserveerde waarden in het apicale segment en gedeprimeerde waarden in het basale en midventriculaire segment. D: 99mTc-DPD (99mTc-3,3-diphosphono-1,2-propanodicarboxylic acid) scan van een patiënt met ATTRwt, waarbij biventriculaire opname superieur aan botopname wordt getoond, overeenkomend met Perugini graad 3.
Ten slotte merken we op dat ATTR en degeneratieve aortastenose bij dezelfde patiënt naast elkaar kunnen voorkomen. In 2016 vestigden verschillende studies de aandacht op deze mogelijkheid, en een prospectieve studie meldde dat ATTRwt een prevalentie van 6% had bij patiënten ouder dan 65 jaar die een aortaklepvervanging ondergingen.16 Deze studie suggereerde dat patiënten met beide entiteiten een veel slechtere postoperatieve prognose hadden dan patiënten zonder ATTRwt (mortaliteit 50% vs 6,9% na een mediane follow-up van 2,3 jaar).16 Een andere recente studie met 99mTc-DPD scintigrafie bij 43 patiënten met low-flow/low-gradient aortastenose identificeerde 5 patiënten met ATTRwt (prevalentie 12%). 17 Patiënten met ernstige aortastenose en ATTRwt hebben hetzelfde demografische profiel, en de geschikte behandeling voor patiënten met beide ziekten moet nog worden vastgesteld.
Gebruik van diagnostische technieken
De diagnose van ATTR is een uitdaging in de dagelijkse klinische praktijk. Hoewel elektrocardiografie en echocardiografie een rol spelen bij de diagnose, hebben nieuwe niet-invasieve technieken een sleutelrol gekregen bij de beoordeling van patiënten met ATTR.
Elektrocardiogram
De associatie tussen laagspanning en cardiale amyloïdose wordt al lang als onbetwistbaar beschouwd.3 De meest gebruikte criteria in de klinische praktijk zijn de QRS-amplitude 1 Hoewel lage elektrocardiografische spanningen in de setting van LVH argwaan zouden moeten wekken, was de prevalentie in een hedendaagse serie van ATTR zo laag als 20% tot 25%.3,4,13 De prevalentie varieert ook naar gelang de toegepaste criteria. Bijvoorbeeld, het gebruik van het Sokolow-criterium (S-golf in afleiding V1 + R-golf in afleiding V5 of V6
1,5 mV) kan de berekende prevalentie verhogen tot 46% à 58%.13 De verhouding van de linker ventrikelwanddikte tot de totale QRS-spanning is aanbevolen om de verschillen tussen de resultaten van de 2 technieken beter te beoordelen.2,3 Tot 20% van de patiënten met ATTR kan echter voldoen aan de elektrocardiografische criteria voor LVH.2,3
In de meeste series van patiënten met cardiale amyloïdose is het pseudoinfarctpatroon de meest voorkomende elektrocardiografische bevinding2,3,13 (figuur 2A). Door mogelijke betrokkenheid van het geleidingssysteem komen ook vaak complete of incomplete bundeltakblokken voor.3
Echocardiografie
Hoewel echocardiografie de hoeksteen is van de initiële diagnose van ATTR, zijn geen bevindingen specifiek.3 Transthyretine amyloïdose is typisch geassocieerd met een normaal of klein linkerventrikel met concentrische hypertrofie.3 Op het 10e Internationale Symposium over Amyloïd en Amyloïdose in 2004 werd als echocardiografisch criterium voor hartziekten door AL zonder andere oorzaken van LVH de aanwezigheid van LVH vastgesteld met een cutoff van 12 mm voor de interventriculaire wanddikte van de septumwand.4 Dit criterium werd later geëxtrapoleerd naar andere vormen van amyloïdose (figuur 2B), wat een hoge specificiteit maar een lage sensitiviteit opleverde.
Hoewel concentrische LVH klassiek beschreven is, suggereren huidige series dat ongeveer 20% asymmetrische LVH heeft.13
Ondanks de klassieke associatie tussen een normale of licht gedaalde linkerventrikel ejectiefractie (LVEF) en cardiale amyloïdose,2 is het LVEF-bereik zeer variabel.8 In een recente studie in de Mayo Clinic was een LVEF 8 terwijl in onze serie een LVEF 13 Bovendien is het gebruik van de LVEF bij de beoordeling van de systolische functie bij cardiale amyloïdose beperkt, omdat licht gedaalde waarden reeds indicatief zijn voor relevante hartziekte. Deze beperking kan worden ondervangen door het gebruik van Doppler-snelheden, strain imaging en myocardiale contractiefractie, die zijn voorgesteld als geschiktere indices om de hartfunctie te beoordelen.2
Andere klassieke echocardiografische tekenen zijn rechterventrikelhypertrofie, biatriale dilatatie, milde pericardiale effusie, verdikking van de atrioventriculaire klep, verdikking van de atriale septale wand, en korrelig glinsterend myocard.3,6 Omdat sommige van deze kenmerken echter werden waargenomen bij een zeer geselecteerde reeks patiënten in gevorderde stadia van de ziekte, hoeven ze niet allemaal aanwezig te zijn om verdenking te doen ontstaan.1
Regional strain imaging is een zeer nuttige techniek voor de vroege diagnose van patiënten met ATTR. Bij patiënten met ATTR is de longitudinale rek verminderd in basale en midventriculaire segmenten, maar behouden in apicale segmenten18 (figuur 2C). Dit typische patroon kan nuttig zijn bij de differentiële diagnose van ATTR van andere hartziekten.4
Biomarkers
Er zijn minder gegevens over de rol van het N-terminale prohormoon van hersennatriuretisch propeptide (NT-proBNP) en troponine bij ATTR dan bij AL.4 De NT-proBNP niveaus in ATTR zijn gewoonlijk lager dan in AL,4 hetgeen 2 verschillende pathofysiologische mechanismen weerspiegelt: directe licht-keten toxiciteit in AL versus geïnduceerde weefselschade door protofibrillen in ATTR.
Onlangs heeft de Mayo Clinic groep een stratificatie systeem voorgesteld gelijkaardig aan dat wat van kracht is voor AL. In een cohort van 360 patiënten met ATTRwt, bleken beide biomarkers voorspellers te zijn van sterfte. Patiënten in stadium III (NT-proBNP > 3000 pg/mL en troponine T > 0,05 ng/mL) hadden een mediane overleving van 20 maanden, terwijl patiënten in stadium I en II een mediane overleving hadden van 66 maanden en 40 maanden (respectievelijk geen biomarker of slechts 1 biomarker boven de vastgestelde afkappunten).
Cardiac Magnetic Resonance Imaging
Cardiale magnetische resonantiebeeldvorming (CMRI) kan worden gebruikt om structurele en functionele informatie te verkrijgen en de samenstelling van het myocardweefsel te karakteriseren.3 CMRI is essentieel voor de vroege identificatie van ATTR, en voor de differentiële diagnose van andere hartziekten.
De karakterisering van weefsel door CMRI is gebaseerd op de volgende kenmerken:
- –
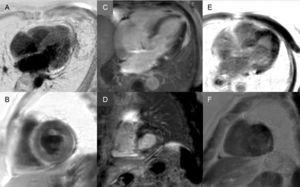
Late enhancement: Een globaal subendocardiaal patroon is vrijwel pathognomonisch voor cardiale amyloïdose, maar is slechts bij ongeveer een kwart van de patiënten aanwezig. Andere patronen, zoals transmuraal (het meest voorkomend) of patching, zijn ook compatibel (figuur 3). Ondanks de hoge sensitiviteit en specificiteit moet rekening worden gehouden met een mogelijke afwezigheid van late enhancement (15% van de patiënten) en, naar onze ervaring, een niet te verwaarlozen percentage fout-negatieven om technische redenen.3 Het transmurale enhancement-patroon wordt geassocieerd met een slechtere prognose en is een onafhankelijke voorspeller van mortaliteit.19
 Figuur 3.
Figuur 3.Diversiteit van late versterkingspatronen bij cardiale magnetische resonantiebeeldvorming bij transthyretine amyloïdose. A en B: late versterkingssequenties, respectievelijk op het vierkamervlak en de korte as op het middenniveau, van een patiënt met gemuteerde transthyretine-amyloïdose (ATTRm), die diffuse pathologische transmurale gadoliniumafzetting laat zien. C en D: late versterkingssequenties, 4-kamer en korte-as basaal niveau, respectievelijk, van patiënten met ATTRm, die pathologische gadoliniumdepositie met een patched patroon vertonen, met lager inferoseptaal en inferolateraal basaal focaal gebied. E en F, late versterkingssequenties, 4-kamer vlak en korte as op apicaal niveau, respectievelijk, van patiënten met ATTRm, die uitgebreide pathologische transmurale depositie laten zien, behalve in basale en middelste anterolaterale segmenten. Met dank aan Dr Jesús González Mirelis.
(0.15MB). - –
Lange T1 tijden: T1 mapping is een techniek waarbij een kwantitatief myocardiaal signaal wordt gemeten vóór (natief T1) of na contrasttoediening. Native T1 tijden zijn zeer lang bij cardiale amyloïdose.3 T1 mapping vereist geen toediening van contrast en kan dus gebruikt worden bij nierfalen. T1 tijden kunnen zelfs abnormaal zijn voordat LVH wordt waargenomen.3 T1 tijden zijn langer bij ATTR dan bij HCM en controles (1097ms ± 43 ms vs 1026ms ± 64 ms vs 9,67ms ± 34ms, respectievelijk; P
ms ± 68 ms; P = 0,01).20
Contrasttoediening kan worden gebruikt om extracellulair volume (ECV) te berekenen en toename van extracellulaire ruimte te beoordelen. ECV-waarden bij cardiale amyloïdose zijn hoger dan bij andere hartziekten, behalve in myocardinfarctzones.21 In 2016 rapporteerde onze groep, in samenwerking met andere nationale centra, dat ECV-kwantificering cardiale betrokkenheid bij ATTRm kan identificeren en, voor het eerst, correleerde met de mate van neurologische stoornissen, wat het gebruik van deze techniek bij vroege diagnose en opsporing van ATTRm ondersteunt.22
Quantitatieve T1 mapping en ECV berekeningstechnieken kunnen zeer nuttig zijn bij ATTR voor vroege diagnose, klinische follow-up, en beoordeling van de respons op behandeling (figuur 4).
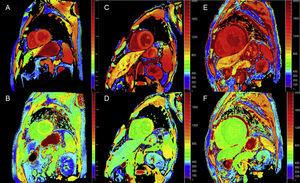
T1 mapping, voor en na contrast, met gemodificeerde look-locker inversie-recovery (MOLLI) in 3T cardiale magnetische resonantie beeldvorming in gezonde controle, patiënt met transthyretine amyloïdose, en patiënt met primaire licht-keten amyloïdose. A en B: Natieve T1 mapping en extracellulair volume (EV), respectievelijk, in een gezonde controle, met normale waarden (EV = 0,214). C en D: Natieve T1 kartering en EV, respectievelijk, bij een patiënt met mutante transthyretine amyloïdose met neurologische schade en beginnende cardiale betrokkenheid, verhoogde natieve T1, en licht verhoogde EV (0.361). E en F: Natieve T1 kartering en EV, respectievelijk, bij een patiënt met wild-type transthyretine cardiale amyloïdose, verhoogde natieve T1, en zeer hoge EV (0,626), wat wijst op massale amyloïd infiltratie. Met dank aan Dr Jesús González Mirelis.
Cardiale scintigrafie
In de jaren tachtig werd de waarneming van cardiale opname van verschillende botdifosfonaat-tracers histologisch gecorreleerd met de aanwezigheid van cardiale amyloïdose.23 Het mechanisme van de opname is niet goed gekarakteriseerd, maar het zou verband kunnen houden met het calciumgehalte van amyloïde afzettingen.
In een vroege studie van de Bologna-groep met 99mTc-DPD werd cardiale opname gevonden bij 15 patiënten met ATTR en de afwezigheid daarvan bij 10 patiënten met AL, waarbij gebruik werd gemaakt van een score gebaseerd op biventriculaire opname die gelijk was aan of hoger dan de botopname (Perugini-score)24 (figuur 2D). Vergelijkbare bevindingen werden vervolgens gerapporteerd door onze groep en anderen.25 Milde uptake (score 1) en matige uptake (score 2) kunnen worden gevonden bij respectievelijk 30% en 10% van de patiënten met AL.24
Gezien de hoge sensitiviteit en specificiteit, is deze techniek uiterst nuttig voor het vaststellen van de diagnose ATTR en kan cardiale betrokkenheid aantonen, zelfs wanneer echocardiografie en MRI-bevindingen nog normaal zijn. In feite zijn incidentele bevindingen van ATTR na scintigrafie voor oncologische of reumatologische indicaties niet ongewoon.26
De Tc-DPD is niet beschikbaar in de Verenigde Staten, maar vergelijkbare resultaten zijn gerapporteerd met behulp van 99mTc-PYP (pyrofosfaat) beeldvorming.27
Andere radiotracers worden momenteel bestudeerd. Zo is 18F-florbetapir, dat reeds is goedgekeurd voor beeldvorming van beta-amyloïd in de hersenen,4 onderzocht bij patiënten met AL en ATTR. De resultaten tonen aan dat 18F-florbetapir myocardiale AL en ATTR afzettingen kan detecteren.28 Hoewel de beschikbare gegevens werden verkregen in case studies29 en de hoge kosten van deze radiotracer het gebruik ervan beperken, zijn er verschillende studies aan de gang naar het potentiële voordeel van het gebruik ervan ten opzichte van dat van Tc-DPD als screeningstechniek voor de 2 meest voorkomende vormen van amyloïdose.
Invasieve diagnose
De definitieve diagnose van ATTR is gebaseerd op het histologisch aantonen van amyloïde fibrillen. Hoewel er extracardiale depositie kan zijn, varieert de kans dat amyloïd door histologie wordt aangetoond per orgaan.2 Er zijn weinig studies over de kosteneffectiviteit van een extracardiale biopsie (bv. abdominaal vet, gingiva, speekselklier, gastro-intestinaal) bij ATTR, die groter is bij ATTRm dan bij ATTRwt. Een negatieve biopsie van een klinisch onaangetast orgaan sluit de diagnose ATTR echter niet uit.4
Zoals bij ATTRwt is een endomyocardiale biopsie geïndiceerd bij patiënten zonder extracardiale betrokkenheid of met alleen hartziekte.3,4 Endomyocardiale biopsie is een procedure met een laag risico (vooral in ervaren centra) en fouten bij de monsterneming zijn onwaarschijnlijk.6
Na histologische bevestiging van amyloïdose, waarvoor soms interpretatie door getraind personeel nodig is,6 is correcte classificatie van het subtype cruciaal.4 Momenteel is classificatie afhankelijk van een combinatie van immunohistochemie, genetische analyse, en proteomics:
- –
Immunohistochemie is gebaseerd op het gebruik van specifieke antilichamen tegen bekende amyloïd eiwitten. Hoewel de resultaten van deze techniek doorgaans definitief zijn, is zij minder gevoelig voor de herkenning van lichte ketens.4
- –
Deze beperking kan worden ondervangen door het gebruik van massaspectrometrie, die definitieve resultaten oplevert en de maatstaf is voor de bevestiging van het amyloïd-subtype.2 Hoewel deze techniek alleen in gespecialiseerde centra beschikbaar is, is zij vooral nuttig in onduidelijke gevallen of in gevallen die positief zijn voor verschillende antilichamen op immunohistochemie, wat in onze ervaring in ongeveer 20% tot 30% van de gevallen voorkomt. 4
- –
Omdat klinische of histologische technieken ATTRm niet kunnen onderscheiden van ATTRwt, wordt genetisch onderzoek aanbevolen in alle gevallen van ATTR. Het vinden van een oorzakelijke mutatie kan van belang zijn voor het aanbieden van genetische counseling en follow-up aan asymptomatische dragers, 4,30 die baat zouden kunnen hebben bij toekomstige therapieën die het begin van de ziekte vertragen of zelfs voorkomen.31
Niet-invasieve diagnose
Tot voor kort werd histologisch onderzoek als essentieel beschouwd in de diagnose van ATTR.3 Om de diagnose te vergemakkelijken, stelde een internationale multicenter studie in 2016 echter een nieuw algoritme voor de niet-invasieve diagnose van ATTR voor.32
De studie analyseerde de resultaten van 1217 patiënten. De aanwezigheid van klassieke tekenen van cardiale amyloïdose met behulp van beeldvormende technieken, graad 2 of 3 Tc-DPD/PYP-uptake op scintigrafie, en de afwezigheid van een monoklonaal eiwit hadden een specificiteit en positief voorspellende waarde voor ATTR van 100%32 (figuur 5).
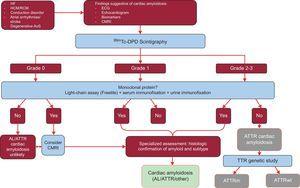
Diagnostisch algoritme voor patiënten met verdenking op cardiale amyloïdose. Beoordelingssysteem voor 99mTc-DPD-scintigrafie: graad 0, geen hartopname; graad 1, licht lagere opname dan bot; graad 2, matige opname gelijk aan botopname; graad 3, ernstige opname hoger dan botopname. ACV, beroerte; AL, primaire lichte keten amyloïdose; AOS, aortastenose; ATTR, transthyretine amyloïdose; ATTRm, mutante transthyretine amyloïdose; ATTRwt, wild-type transthyretine amyloïdose; CMRI, cardiale magnetische resonantie beeldvorming; ECG, elektrocardiogram; HCM, hypertrofische cardiomyopathie; HF, hartfalen; RCM, restrictieve cardiomyopathie; TTR, transthyretine.
Een belangrijk kenmerk van dit algoritme is de afwezigheid van een monoklonaal eiwit dat AL zou kunnen veroorzaken op serum chain assay (Freelite, The Binding Site, UK) en op immunofixatie-elektroforese van bloed en urine. De aanwezigheid van een monoklonaal eiwit is een indicatie voor endomyocardiale biopsie om onderscheid te maken tussen ATTR en AL.32 Tot 5% van de bevolking ouder dan 65 jaar heeft een monoklonale gammopathie van onbepaalde betekenis.2 Bij ouderen zou een matige toename van circulerende lichte ketens niet direct tot de diagnose AL moeten leiden. Er is gerapporteerd dat tot 10% van de oudere patiënten met ATTRwt en monoklonale gammopathie van onbepaalde significantie in referentiecentra eerder een verkeerde diagnose van AL hadden gekregen.3,33 Een juiste diagnose is nodig om ongepaste chemotherapie te vermijden. Van belang is dat ons ziekenhuis 2 gevallen heeft gedocumenteerd van patiënten met multipel myeloom en gelijktijdig ATTRwt op massaspectrometrie.
BEHANDELING VAN TRANSTHYRETIN CARDIAC AMYLOIDOSIS
De behandeling van patiënten met ATTR heeft 2 doelstellingen: medische ondersteuning bieden en, indien mogelijk, de amyloïdafzetting stoppen of vertragen door het gebruik van specifieke behandelingen.
Medische behandeling
In de volgende paragrafen wordt de ondersteunende cardiale zorg voor patiënten met ATTR beschreven.
Behandeling van hartfalen
Euvolemie moet worden gehandhaafd bij patiënten met cardiale amyloïdose. Dieet- en leefstijlmaatregelen zijn zeer belangrijk. Diuretica zijn essentieel voor de behandeling van HF bij ATTR. Omdat overmatig gebruik van diuretica echter kan leiden tot hypotensie (vaak als gevolg van autonome disfunctie) en de klinische situatie kan verergeren, vooral bij ATTRm, moet uiterst voorzichtig te werk worden gegaan.
Bij de behandeling van HF in ATTR moet er rekening mee worden gehouden dat verminderde diastolische disfunctie en verminderd slagvolume leiden tot compensatoire tachycardie om de cardiale output op peil te houden. Daarom moeten bètablokkers met zorg worden gebruikt en voor elke patiënt worden geïndividualiseerd. De standaardpraktijk is ze te verwijderen als er geen problemen zijn met het onder controle houden van de hartfrequentie. Deze aanpak is, indien mogelijk, nog belangrijker bij ATTRwt vanwege de frequente aanwezigheid van geleidingsstoornissen.6 Calciumantagonisten en digoxine kunnen zich binden aan amyloïde fibrillen en zijn daarom gecontra-indiceerd bij ATTR vanwege het risico op toxiciteit, zelfs bij therapeutische doses.6
In tegenstelling tot HF met systolische dysfunctie door andere etiologie is er geen bewijs voor een prognostisch voordeel door het gebruik van bètablokkers, angiotensine-converterende enzymremmers, of angiotensine II receptor antagonisten bij cardiale amyloïdose. In feite kan het gebruik ervan leiden tot klinische verslechtering door hypotensie en lage output: een recente publicatie meldde een slechtere prognose bij ATTRm en een neutraal effect bij ATTRwt.34
Behandeling van atriale aritmieën
De behandeling van AF bij ATTR is een uitdaging. Het handhaven van een sinusritme op lange termijn is moeilijk. Elektrische cardioversie kan echter worden geprobeerd omdat dit tot klinische verbetering kan leiden.
Het risico op trombo-embolie bij patiënten met ATTR is zeer hoog. Bovendien kan chronische amyloïd infiltratie leiden tot mechanische atriale disfunctie, wat de onderliggende oorzaak kan zijn van de ontwikkeling van atriale trombus bij sommige patiënten zonder AF. Anticoagulantiatherapie bij ATTR mag niet gebaseerd zijn op de CHADS2-VASC score en moet standaardtherapie zijn bij AF. Bloedingen komen minder vaak voor dan bij AL, en daarom bevelen sommige ziekenhuizen antistollingstherapie aan bij patiënten in sinusritme als er een slechte atriale functie is volgens de transmitrale Doppler-snelheden. Hoewel er geen vergelijkende studies zijn over de effectiviteit van directe orale anticoagulantia versus vitamine K antagonisten, heeft ons ziekenhuis directe orale anticoagulantia toegediend aan geselecteerde patiënten.
Rol of Devices
De huidige aanbevelingen voor pacemaker implantatie zijn hetzelfde bij ATTR en de algemene bevolking. Sommige groepen zijn echter voorstander van profylactische implantatie, vooral bij patiënten met ATTRm en geleidingsstoornissen.35 Wij zijn geen voorstander van deze preventieve strategie en hebben niet zo’n hoog percentage geleidingsstoornissen gevonden dat profylactische implantatie bij patiënten met ATTRm gerechtvaardigd is.
De rol van implanteerbare cardioverter-defibrillator (ICD) bij ATTR is niet goed vastgesteld. In een kleine serie verbeterde ICD-implantatie de overleving niet significant, hoewel het bij meerdere patiënten gedurende de eerste 2 jaar een passend effect had.36
Harttransplantatie
Harttransplantatie heeft een kleine rol gespeeld bij ATTR omdat ATTRm verschillende organen kan betreffen en ATTRwt typisch oudere patiënten treft. Echter, de afwezigheid van extracardiale betrokkenheid bij patiënten met ATTRwt maakt hen goede kandidaten voor de procedure. De literatuur geeft voorbeelden van succesvolle transplantatie bij patiënten jonger dan 70 jaar met ATTRwt of met ATTRm en overwegend cardiale betrokkenheid.4
Specifieke behandeling van transthyretine cardiale amyloïdose
Op dit moment is er geen goedgekeurde therapie voor de specifieke behandeling van ATTR cardiale amyloïdose, hoewel levertransplantatie (TxH) alleen of in combinatie met harttransplantatie sinds de jaren negentig bij ATTRm wordt gebruikt als een manier om de belangrijkste bron van precursor TTR te elimineren.4
Levertransplantatie
Het Familial Amyloidotic Polyneuropathy World Transplant Registry37 meldde dat meer dan 2000 patiënten met ATTRm een TxH hebben ondergaan in 20 landen.4 Patiënten met de Val30Met mutatie en een overwegend neurologisch ziektebeeld hebben een overlevingskans van meer dan 50% na 20 jaar.3 Deze veelbelovende resultaten zijn gebaseerd op een strenge selectie van patiënten op basis van leeftijd, type mutatie, en stadium van de ziekte. De meest geaccepteerde indicatie voor TxH is de combinatie van jonge leeftijd, de Val30Met mutatie, en vroege stadia van de ziekte.
De belangrijkste beperkingen van deze techniek zijn echter het tekort aan donoren, de noodzaak van chronische immunosuppressie, hoge leeftijd op het moment van presentatie, en slechtere resultaten verkregen bij patiënten met andere mutaties dan de Val30Met mutatie.
Daarnaast wordt de theoretische onderdrukking van de productie van het gemuteerde eiwit tegengegaan door progressieve natieve TTR afzetting na de implantatie,4,6 waarvan het mechanisme niet volledig wordt begrepen. In feite beïnvloedt cardiale TTR afzetting na TxH de morbiditeit en mortaliteit.
De noodzaak om de pathogenese van ATTR en de beperkingen van TxH beter te begrijpen heeft de ontwikkeling van verschillende geneesmiddelen gestimuleerd.
Deze nieuwe verbindingen werken op verschillende punten in de TTR amyloidogenese cascade (Figuur 6). De behandeling zal altijd bestaan uit het verminderen van het precursor eiwit, hoewel het vermijden van afzetting en het elimineren van bestaande afzettingen even belangrijk zullen zijn. Daarom denken wij dat de aanpak van deze ziekte in de toekomst de vorm van een gecombineerde behandeling zal aannemen.
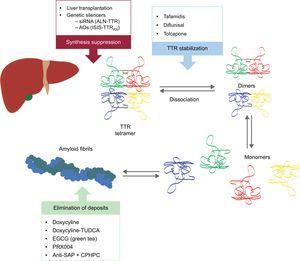
Specifieke therapieën bij transthyretine cardiale amyloïdose en belangrijkste doelwitten. AntiSAP + CPHPC, antiserum amyloïd P-component + (R)-1-6-oxo-hexanoyl]pyrrolidine-2-carboxylzuur; AO’s, antisense oligonucleotiden; EGCG, epigallocatechine-3-gallaat; siRNA, small interfering RNA; TTR, transthyretine; TUDCA, tauroursodeoxycholzuur.
Onderdrukking van Transthyretinesynthese
Twee onderzoekslijnen lopen naar de remming van TTR-lever-expressie: het gebruik van small interfering RNA (siRNA) en het gebruik van antisense oligonucleotide (AO) geneesmiddelen.
- –
De siRNA zijn dubbelstrengs RNA-moleculen die boodschapper-RNA-sequenties het zwijgen opleggen door er specifiek aan te binden, waardoor eiwitvorming wordt verhinderd. Patisiran (ALN-TTR02) blijkt de TTR-productie met 80% te verminderen.38 Bij patiënten met ATTRm bedroeg de TTR-reductie 87%.39 Een fase 2-studie heeft veelbelovende resultaten laten zien, waarbij stabiele echocardiografische, functionele en analytische parameters werden aangetoond na 12 maanden en 24 maanden.40 De resultaten van de fase 3 neurologische studie bij patiënten met ATTRm en een subanalyse van patiënten met cardiale betrokkenheid worden verwacht in 2017 (tabel 2). Een ander geneesmiddel, revusiran (ALN-TTR01), wordt subcutaan toegediend en verschilt van patisiran in de lipide nanodeeltjes die siRNA inkapselen. Dit geneesmiddel was het onderwerp van een fase III klinische studie bij patiënten met ATTRm die hartziekten hebben. De studie werd vorig jaar stopgezet vanwege een onverwachte toename van de mortaliteit in de behandelingsgroep (tabel 2).
Tabel 2.Belangrijkste lopende klinische proeven bij transthyretine cardiale amloïdose
Werkingsmechanisme Compound Trial Opzet Patiënten (N) en ATTR-subtype Interventie Primaire eindpunten Situatie/resultaten TTR-synthese onderdrukking Patisiran (ALN-TTR02) NCT01961921 Phase II studie, multicenter 27
ATTRm (11 hartbetrokkenheid)Patisiran 0.30 mg/kg IV om de 3 weken gedurende 2 jaar Lange-termijn veiligheid. Secundaire eindpunten: effect op neurologische stoornissen en cardiale parameters Goed verdragen geneesmiddel, met vergelijkbaar veiligheidsprofiel in neurologisch en cardiaal fenotype
Troponine I, NT-proBNP en echocardiografische gegevens bleven stabiel na 12 mo en 24 moNCT01960348 (APOLLO) Phase III, gerandomiseerde, dubbelblinde, placebogecontroleerde, multicenter 225
ATTRm met neurologische betrokkenheidPatisiran infusie IV vs placebo 2:1 Veranderingen in mNIS+7 Verwacht november 2017
Subanalyse van patiënten met voorspelde cardiale betrokkenheidNCT02510261 APOLLO-uitbreidingsstudie Patisiran infusie IV vs placebo 2:1 gedurende 52 wk Veiligheid en bijwerkingen op lange termijn Ongaand Revusiran (ALN-TTR01) NCT02319005 (ENDEAVOUR) Phase III, gerandomiseerd, dubbelblind, placebogecontroleerd 206
ATTRm met hartbetrokkenheidRevusiran 500mg 5 d, vervolgens wekelijks gedurende 2 jaar versus placebo Veranderingen in 6-m looptest en in plasma TTR waarden Gediscontinueerd vanwege verhoogde mortaliteit in de revusiran arm ISIS-TTRRX NCT01737398 Phase II/III, gerandomiseerd, dubbelblind, placebogecontroleerd, multicenter 172
ATTRm met neuropathie; 50% gelijktijdige hartbetrokkenheidISIS-TTRRX 300mg SC om de 12 uur gedurende 1 wk, vervolgens wekelijks gedurende 64 wk vs placebo Veranderingen in mNIS+7 en Norfolk-vragenlijst kwaliteit van leven Verwacht september 2017
Gemelde gevallen van ernstige trombocytopenie en bloedingen
Analyse van echocardiografische parameters en NT-proBNP verwacht bij patiënten zonder hypertensie met LVH > 12 mmBehandeling van TTR-cardiomyopathie met TTR-specifiek antisense oligonucleotide Phase II, open-label, niet-gerandomiseerd 20
ATTRm met hartbetrokkenheid en ATTRwtISIS-TTRRX 300mg SC every 12 h/wk Echocardiografische parameters en cardiale MRI versus historische controles Geen verslechtering in stam en verminderde LV-massa van ongeveer 5%
6 patiënten voltooid 12 mo; 15 patiënten 6 mo; 1 patiënt TxCNCT02627820 Phase II, open-label, niet-gerandomiseerd 50
ATTRwtISIS-TTRRX 300mg SC om de 12 uur gedurende 1 wk, daarna 1 wk gedurende 18 wk Veranderingen in rek gemeten door speckle tracking Geannuleerd zonder patiëntenrecrutering te starten Fase III studie met ISIS-TTRRX voor de behandeling van TTR amyloïde cardiopathie Phase III, gerandomiseerd, dubbelblind, placebogecontroleerd, multicenter 490
ATTRwt en ATTRm met hartbetrokkenheidISIS-TTRRX 300mg SC om de 12 uur gedurende 1 week, daarna wekelijks gedurende 16 weken met placebo, vervolgens wekelijks gedurende 24 mo Overlijden, TxC, of opname voor cardiovasculaire oorzaken On hold Stabilisatie van TTR Tafamidis NCT01994889 Phase III, gerandomiseerd, dubbelblind, placebo-gecontroleerd, multicenter 441
ATTRwt en ATTRm met hartbetrokkenheidTafamidis 20mg of 80mg oraal om de 24 uur gedurende 30 mo versus placebo Alle-oorzaak mortaliteit en cardiovasculaire ziekenhuisopname Eind februari 2018 NCT02791230 Extensie Fase III NCT01994889 330
ATTRwt en ATTRm met hartbetrokkenheidTafamidis 20 mg of 80 mg oraal om de 24 uur gedurende 60 mo All-mortaliteit en incidentie van bijwerkingen Verwacht december 2021 NCT00935012 Phase II, open-label, werkzaamheids- en veiligheidsonderzoek 31
ATTRwt of ATTRm p.Val122Ile met hartbetrokkenheidTafamidis 20mg oraal Veiligheid en effectiviteit Loopt tot december 2021 Diflunisal NCT00294671 Phase III, gerandomiseerde, dubbelblinde, placebogecontroleerd, multicenter 130
ATTRm met neurologisch fenotype (50% met cardiale betrokkenheid)Diflunisal 250mg oraal om de 12 uur vs placebo gedurende 24 mo NIS+7 op 24 mo NIS+7 diflunisal vs placebo 16.3 (P Geen vermindering van ventriculaire dikte of rek bij patiënten met hartbetrokkenheid vs placebo Beperking van afzettingen Doxycycline + TUDCA/UDCA NCT01171859 Phase II, open-label, niet-gerandomiseerd, prospectief 40
ATTR (25 ATTRm, 13 ATTRwt, en 2 ontvangers van domino levertransplantatie)Doxycycline 100 mg om de 12 uur + TUDCA 250 mg om de 8 uur gedurende 12 mo, vervolgens 6 mo zonder therapie Verbetering 14 patiënten trokken zich terug
Bijwerkingen huidreacties, 16 patiënten
68% van de 25 evalueerbare patiënten voldeden aan het primaire eindpunt
Over het geheel genomen verbetering van de belasting bij 12 mo en verslechtering na 6 mo zonder therapieNCT01855360 Phase II, open-label, niet-gerandomiseerd, prospectief vs historische controles 30
Cardiale ATTR amyloïdose (27 ATTRwt en 3 ATTRm). Historische controles, 14 ATTRwt-patiëntenDoxycycline 100 mg om de 12 uur + TUDCA 250 mg om de 8 uur gedurende 18 maanden Veranderingen in longitudinale rek om de 6 maanden 22 patiënten voltooiden de studie en waren evalueerbaar
Grote verslechtering van rek in controles versus behandelgroep
Verhoogd NT-proBNP in behandelgroep; niet gemeten bij controlesNCT01677286 Phase II, open-label, niet-gerandomiseerd, prospectief 25
Systemische amyloïdose (6 ATTRwt en 3 ATTRm)Doxycycline 100 mg om de 12 uur gedurende 12 mo Gebruiksveiligheid
Respons van aangedane organenVerergergering van NT-proBNP en nierfunctie
Geen verbetering in andere onderzochte parameters
60% van de patiënten had huidcomplicaties en 30% trok zich terug vanwege huid- of gastro-intestinale problemenNCT01171859 Phase II, open-label, niet gerandomiseerd, prospectief 45
35 met hartbetrokkenheid; 25 ATTRm; 5 ATTRm met TxH; 13 ATTRwt; en 2 ontvangers van domino levertransplantatiesDoxycycline 100 mg om de 12 uur + TUDCA 250 mg om de 8 uur gedurende 12 maanden
Navolgende follow-upfase zonder behandeling gedurende 6 maandenDrugrespons gedefinieerd als een Cardiale respons beoordeeld bij 25 patiënten
68% had cardiale respons
Toename van NT-proBNP en verslechtering van de belasting tijdens follow-up zonder behandeling
Groot aantal terugtrekkingen vanwege bijwerkingen
14 trokken zich terug in behandelingsfase en 5 stopten in fase zonder behandelingEffect van doxycycline + UDCA op ATTR Phase II, open-label, niet gerandomiseerd, prospectief 28
ATTR met cardiale betrokkenheid (27 ATTRm en 1 ATTRwt)Doxycycline 200 mg/d gedurende 4 wk, daarna 2 wk opgeschort, vervolgens UDCA 750 mg/d gedurende 12 maanden
Volgende follow-upfase zonder behandeling gedurende 6 maandenVeranderingen in NT-proBNP en Kumamoto-score Slechts 14% voltooide de studie en 36% voltooide 12 maanden
Geen veranderingen in NT-proBNP bij 6 mo en verslechtering bij 12 mo
Stabiele LVH
Verergering van Kumamoto-score bij 12 moEGCG NCT01171859 Phase II, open-label, niet-gerandomiseerd, prospectief 25
ATTRwt600 mg, EGCG gedurende 12 maanden Veranderingen in ECHO en cardiale MRI (n = 14) Verminderde LV-massa 6% door cardiale MRI (P = 0.03)
LVEF, myocardiale dikte, en MAPSE door ECHO onveranderdAntiSAP + CPHPC NCT03044353 Phase II, open-label, gerandomiseerd 40
Cohort 1: cardiale ATTR amyloïdose
Cohort 2: primaire amyloïdose na 6 mo chemotherapieAnti-SAP + CPHPC maandelijks gedurende 6 mo Verminderde amyloïdlast door cardiale MRI en ECHO Start in 2017 Anti-SAP + CPHPC, antiserum amyloïd P-component + (R)-1-6-oxo-hexanoyl]pyrrolidine-2-carboxylzuur; ATTRm, mutante transthyretine-amyloïdose; ATTRwt, transthyretine-amyloïdose van het wilde type; BNP, hersennatriuretisch peptide; ECHO, echocardiogram; EGCG, epigallocatechine-3-gallaat; IV, intraveneus; LV, linker hartkamer; LVEF, linker ventrikel ejectiefractie; LVH, linker ventrikel hypertrofie; MAPSE, mitralis annulaire vlak systolische excursie; mNIS, Modified Neuropathy Impairment Score; MRI, magnetische resonantie beeldvorming; NIS, Neuropathy Impairment Score; NIS-LL, Neuropathy Impairment Score of the Lower Limbs; NT-proBNP, amino-terminal pro-brain natriuretic peptide; SC, subcutaan; TTR, transthyretine; TUDCA, tauroursodeoxycholic acid; TxC, harttransplantatie; TxH, levertransplantatie; UDCA, ursodeoxycholic acid.
- –
De AO’s zijn korte strengen oligonucleotiden die zich specifiek aan RNA binden en zo de translatie en de eiwitsynthese verhinderen.4 ISIS-TTRRX is een subcutane AO, met aangetoonde dosisafhankelijke reducties in TTR-waarden van 75% tot 90% bij gezonde vrijwilligers.4 De fase III-studie bij patiënten met ATTRm en neurologisch fenotype eindigde in maart 2017 en de resultaten ervan worden eind 2017 verwacht. De Amerikaanse Food and Drug Administration heeft echter de start van een fase III-studie bij patiënten met ATTRwt en ATTRm met hartaandoeningen uitgesteld vanwege gevallen van ernstige trombocytopenie in de neurologische studie (tabel 2). Aangezien 50% van de deelnemers aan het neurologisch onderzoek een hartziekte had, zullen de resultaten van dit cardiale deelonderzoek bepalen of het fase III-onderzoek wordt hervat. Anderzijds zijn er voorlopige gegevens van een open-label fase II-studie. In deze studie kregen 22 patiënten met ATTRwt en ATTRm met hartaandoeningen een wekelijkse injectie met ISIS-TTRRX. Volgens het rapport is het veiligheidsprofiel van het geneesmiddel zeer gunstig en zijn de tussentijdse gegevens over de progressie van de hartziekte door CMR, NT-proBNP, en 6-minutentests positief.41
Stabilisatie van transthyretine
Dissociatie van het TTR-tetrameer in subeenheden is een cruciale stap in de vorming van ATTR-fibrillen. Diflunisal en tafamidis zijn 2 TTR stabilisatoren met aangetoonde werkzaamheid in ATTRm polyneuropathie.
- –
Tafamidis is een oraal toegediend klein molecuul dat zich bindt aan TTR op T4 bindingsplaatsen door het eiwit te stabiliseren en de dissociatie ervan te voorkomen. Na de publicatie van de resultaten van een gerandomiseerde dubbelblinde studie bij 125 patiënten met ATTRm en de Val30Met-mutatie in de beginfase van de neurologische ziekte,42 keurde het Europees Geneesmiddelenbureau het gebruik ervan in 2011 goed als weesgeneesmiddel om de neurologische progressie te vertragen. Recente gegevens tonen de effectiviteit van het geneesmiddel aan om neurologische stabiliteit te bereiken bij ten minste 60% van de deelnemers na meer dan 4 jaar follow-up. Tot op heden wordt het beperkt gebruikt bij ATTR en cardiologische aandoeningen. Een fase II-onderzoek bij 21 patiënten met ATTRm en verschillende mutaties toonde aan dat NT-proBNP en echocardiografische parameters stabiel bleven na 12 maanden.43 Gegevens van een 5-jarig cohortonderzoek bevestigden dat het geneesmiddel goed werd verdragen bij een dosis van 20 mg, hoewel weinig patiënten met ATTRwt stabiel bleven na 3,5 jaar.44 De ATTR-ACT-studie is een fase III-studie van 30 maanden waarin de werkzaamheid, veiligheid en verdraagbaarheid van doses van 20 mg en 80 mg tafamidis versus placebo wordt beoordeeld bij 440 patiënten met ATTRm, ATTRwt, en HF. Het primaire eindpunt omvat ziekenhuissterfte en -opname. De resultaten worden verwacht in 2018.3,27
- –
Diflunisal is een niet-steroïdaal ontstekingsremmend middel dat TTR-moleculen in vitro stabiliseert. Het is niet verkrijgbaar in Spanje, maar kan medisch worden aangevraagd uit het buitenland voor compassionate use. Een fase III studie van ATTRm bij patiënten met voornamelijk neurologische betrokkenheid, van wie meer dan de helft hartziekte had, vond geen significante verschillen in echocardiografische parameters gedurende de studieperiode (tabel 2).45 De mogelijkheid van gastro-intestinale bijwerkingen, nierfalen, waterretentie, en hypertensie maken het ongeschikt voor patiënten met hartziekte. De gegevens over diflunisal bij patiënten met ATTR zijn zeer beperkt. Er is één studie, maar die was beperkt omdat het een niet-gerandomiseerde single-center opzet was met weinig follow-up en weinig patiënten (n = 13). Er waren geen opnames voor gedecompenseerd HF, maar er was een significante verslechtering van de nierfunctie.46
- –
Meer recent heeft een Spaanse groep aangetoond dat tolcapone (een orale catechol-O-methyltransferase remmer gebruikt bij de behandeling van de ziekte van Parkinson) de mogelijkheid heeft om zich in vitro te binden aan het TTR van patiënten met ATTRwt en Val122Ile met een hogere affiniteit dan andere stabilisatoren.47
Eliminatie van amyloïde afzettingen
Amyloïde afzettingen zijn zeer stabiel en het lijkt erop dat het menselijk organisme weinig mogelijkheden heeft om ze te elimineren. Behandelingen die de aanmaak van nieuw amyloïd verhinderen, zoals chemotherapie bij AL, kunnen de afzettingen echter geleidelijk verwijderen met verschillende orgaanspecifieke snelheden. De klaring in het hart is bijzonder laag en tot nu toe is er weinig bewijs van regressie. Verschillende moleculen worden momenteel onderzocht om de amyloïd klaring in het hart te versnellen bij ATTR:
- –
Doxycycline (een veelgebruikt antibioticum) verstoort de vorming van amyloïde fibrillen. Het synergetische effect van de combinatie van doxycycline en tauroursodeoxycholisch galzuur (TUDCA), dat wordt gebruikt bij de behandeling van leverziekten, is aangetoond om TTR-afzettingen te verwijderen in diermodellen. Een fase II studie met 20 patiënten toonde geen cardiale of neurologische progressie aan na 1 jaar behandeling met doxycycline/TUDCA, met een aanvaardbaar veiligheids- en verdraagbaarheidsprofiel.4 Andere fase II studies hebben geprobeerd deze bevindingen te bevestigen met gecombineerde doxycycline/TUDCA, doxycycline/ursodeoxycholzuur, of doxycycline alleen.48-50 De voorlopige resultaten van een van deze studies suggereren een beschermend effect, met minder verslechtering van de hartfunctie door overbelasting in de behandelingsgroep. Een ander van deze studies verkreeg soortgelijke bevindingen bij 40 patiënten met ATTR: onder andere NT-proBNP, functionele klasse, LVEF en myocarddikteparameters bleven stabiel na 12 maanden (tabel 2). Niettemin hadden al deze studies een hoog uitvalpercentage (35%-44%), voornamelijk als gevolg van bijwerkingen, met name zonneovergevoeligheid en gastro-intestinale klachten (tot 30%).48-50
- –
Het EGCG (epigallocatechine-3 gallate) is de meest voorkomende catechine in groene thee, en er is in vitro en in een muismodel aangetoond dat het de vorming van amyloïde remt en bestaande afzettingen elimineert.4 De CMRI toonde aan dat dagelijkse toediening van 600mg EGCG geassocieerd was met stabilisatie van de linker ventrikelmassa in een groep van 25 patiënten (Tabel 2).51
- –
De PRX004 is een monoklonaal antilichaam dat werkt door te binden aan monomeer-specifieke epitopen en verkeerd gevouwen TTR. Het lokt aldus de eliminatie van afzettingen uit door fagocytose te activeren.52 De basis van zijn werkingsmechanisme is vergelijkbaar met dat van een antilichaam dat bij AL wordt gebruikt. Fase II studies met dit antilichaam laten veelbelovende resultaten zien. Een fase I-II-studie met dit nieuwe antilichaam zal in 2017 van start gaan.
- –
Ongeacht het type amyloïde precursoreiwit, bevatten alle afzettingen serum amyloïde component P (SAP). Met dit molecuul als doelwit is aangetoond dat anti-SAP antilichamen een macrofaag-gemedieerde en complement-afhankelijke reactie opwekken die in een muismodel een aanzienlijke eliminatie van viscerale amyloïde afzettingen veroorzaakt. De bis-D-prolineverbinding CPHPC kan plasma-SAP neutraliseren, en gelijktijdige toediening met anti-SAP IgG maakt het mogelijk dat het antilichaam SAP-bevattende afzettingen in weefsel bereikt.53 Een in 2015 gepubliceerde fase I-studie toonde de verwijdering aan van leverafzettingen bij 15 patiënten met systemische amyloïdose zonder betrokkenheid van het hart, met weinig bijwerkingen.53 Een fase II-studie van patiënten met ATTR cardiale amyloïdose en AL gaat in 2017 van start (tabel 2).
CONCLUSIES
Transthyretine cardiale amyloïdose wordt met toenemende frequentie gediagnosticeerd. 99mTc-DPD scintigrafie en CMRI zijn voorbeelden van technieken die kunnen worden gebruikt voor de eenvoudige en vroege identificatie van patiënten met ATTR.
Er zijn momenteel verschillende ATTR-specifieke geneesmiddelen in de laatste fasen van onderzoek. Daarom geloven we dat ATTR cardiale amyloïdose binnenkort zal worden beschouwd als een behandelbare entiteit in plaats van een dodelijke ziekte.
Financiering
Dit werk werd uitgevoerd met gedeeltelijke steun van het Carlos III Health Institute en de Spaanse Vereniging voor Cardiologie (onderzoeksbeurs 2016 aan E. González-López). Bijstand van het Carlos III Health Institute wordt gefinancierd door het Europees Fonds voor Regionale Ontwikkeling “Another Way to Make Europe”.
CONFLICTS OF INTEREST
E. González-López heeft als spreker deelgenomen aan activiteiten georganiseerd door Pfizer. P. Garcia-Pavia heeft betalingen ontvangen als spreker in door Pfizer georganiseerde activiteiten en als consultant voor Alnylam, Prothena, en Pfizer. E. González-López, A. López-Sainz, en P. Garcia-Pavia verklaren dat Pfizer onderzoeksprojecten van hun instelling heeft gefinancierd.
- –