20万人以上が経カテーテル大動脈弁置換術(TAVR)を受けており、毎年約14万人の患者が外科的生体弁置換術を受けています1,2。 特に、2つの疑問が、これらの一般的な臨床シナリオに対する意思決定の難しさを強調している。
- 生体弁置換術後の初期数カ月間、抗凝固療法で減らそうとしているのはどんな合併症か
- これらの合併症を減らすために、すべての患者に抗凝固療法を行うべきか? それとも、危険因子に基づいてより選択的なアプローチをとるべきでしょうか。
Thrombotic Risks After Bioprosthetic Valve Replacement
従来、弁置換術後の最初の数か月間の抗凝固療法の根拠は、おそらく縫合材およびまだ生体膜に覆われておらず内皮化していない縫合リングに関する血栓合併症を軽減することでした3,4。 血栓性合併症には、血栓塞栓症、弁の顕性血栓症、長期的な弁機能を損なう可能性のある不顕性組織化血栓の3つが考えられる。 人工弁置換術の頻度が高いにもかかわらず、これらの合併症に関するデータは限られており、その理由の一つは、これらの事象が稀であるように見えるからである
最近のメタ解析では、人工弁置換術後の事象率が低いことが強調されている。 外科的大動脈弁置換術を受けた患者31,740人を対象としたこの解析では、ビタミンK拮抗薬服用患者145人(1%)、ビタミンK拮抗薬非服用患者262人(1.5%)に早期血栓塞栓事象が発生しました(オッズ比0.96;95%信頼区間、0.60-1.52)。5 もし、ビタミンK拮抗薬を服用していない患者では、外科的大動脈弁置換術後の最初の数ヶ月間に血栓塞栓症の合併症が実際に0.5%増加すると仮定すると、適切に検出力を備えた無作為比較試験には、約15500人の患者が必要となります6。 現在までに、2つの無作為化試験が実施され、合計268人の患者がいます。7,8 患者数が少ないことを考えると、2つのグループに統計的に検出できる差がないことは驚くべきことではありません。
大規模な無作為化対照試験がない場合,臨床医は,デンマーク全国患者登録からの解析のような観察研究に洞察を求めなければならない。9 生体置換大動脈弁置換術を受けた患者4,075人のこの研究では,術後1~6カ月にワルファリン中止が血栓塞栓イベントおよび心血管死亡の増加と関連していることがわかった。 興味深いことに,治療群では最初の3ヵ月で脳卒中が増加したが,3ヵ月から6ヵ月の脳卒中の発生数は,ワルファリンを継続した患者と中止した患者で差がなく,この期間の発生数はわずか21件であった。 また、3ヵ月後と1年後の出血イベントにも差はなかった。 この観察は、ワルファリン投与患者は出血で入院する可能性が高いというこれまでの報告や臨床経験に反している5。したがって、心血管死亡率および血栓塞栓イベントに関する著者らの結論は、残留交絡に関連していた可能性がある。
残念ながら,血栓塞栓症イベントと比較して,生体弁血栓症に関する推論的な関連性については,発表されたデータから得られる知見はさらに乏しい。 その結果、生体弁血栓症の発生率は明確ではありませんが、ある研究では、生体弁大動脈弁の患者4,568人のうち、血栓に関連した大動脈弁狭窄症のために再手術を必要としたのはわずか8人でした11。 同様に、臨床的に静かな血栓症や、促進される可能性のある生体弁の変性の役割も、ほとんどわかっていません。
生体弁置換術後の選択的抗凝固療法
利益の大きさが不明であることと,十分に認められた出血リスクに基づいて,生体大動脈弁置換術後の普遍的抗凝固療法は正当化が難しい。この不確実性は,2014年の米国心臓病学会(ACC/AHA)弁膜症ガイドラインのクラスIIb推奨に反映されている12。 しかし、抗凝固療法をより強く考慮すべき特定の臨床状況が発生する可能性があります。 例えば、生体大動脈弁血栓症で再手術を受けた患者46人を含む最近のケースコントロール研究では、心エコー検査での平均ドップラー勾配がベースラインから>50%増加、尖の厚さの増加、尖の移動異常はすべて弁血栓症と関連していました13。したがって、抗凝固療法とフォローアップ心エコーの試験でドップラー勾配の評価を行えば、こうした患者でも考慮できる14 が、短期および長期弁機能がどの程度抗凝固によって修正されるかは明らかではありません。
さらに,生体弁を有する患者は,血栓塞栓事象および弁血栓症のリスクが高いと思われる(以下の図1-2および動画1-2を含む実例参照)。 生体弁置換僧帽弁は大動脈弁置換よりもはるかに一般的ではないため、データはさらに限られています。 しかし、216人の生体僧帽弁置換術患者を対象とした単一施設の研究では、10人(5%)が6ヵ月以内に虚血性脳卒中を発症しました15。さらに、149人の連続患者を対象とした別の研究では、9人(6%)が生体僧帽弁血栓症を発症しています16。 したがって、生体弁膜症僧帽弁置換術を受けた患者はリスクが高いと思われ、3~6カ月間はルーチンの抗凝固療法を検討する必要があり、これも2014 ACC/AHA 心臓弁膜症ガイドラインのクラスIIaの推奨に反映されています12
Illustrative Case: Bioprosthetic Mitral Valve Thrombosis
71歳の女性は、リウマチ性僧帽狭窄に対する生体弁膜症置換術から8カ月後に心不全で受診しました。 術後はクマジンで3か月間治療し、アスピリンを継続していた。 心房細動の既往はなく、無熱で、血液培養は陰性であった。
ビデオ 1
図1
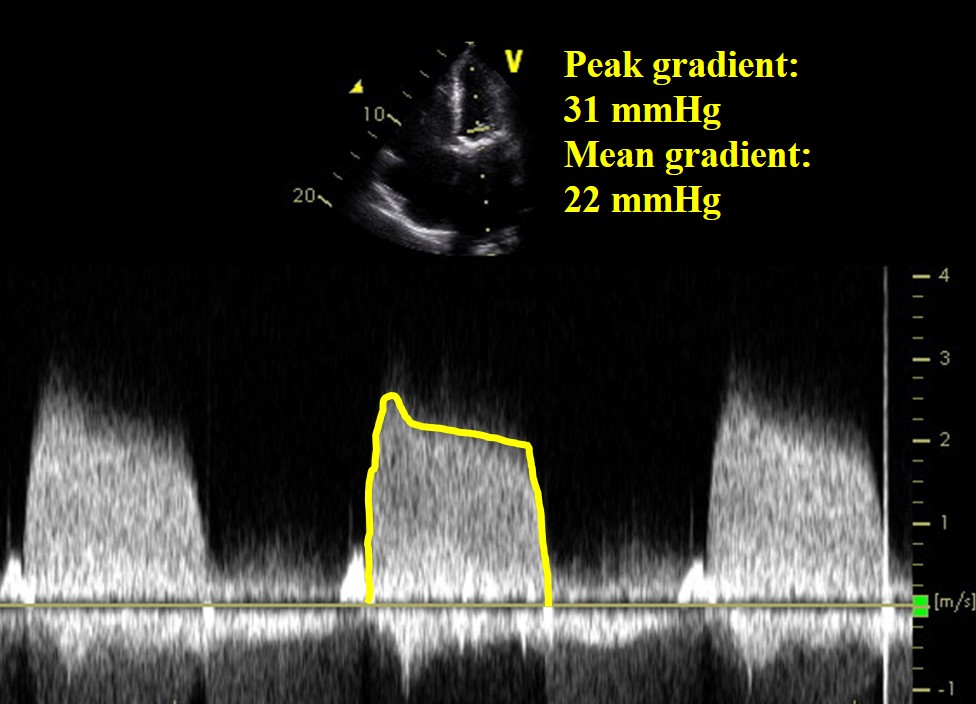
ビデオ2
図2
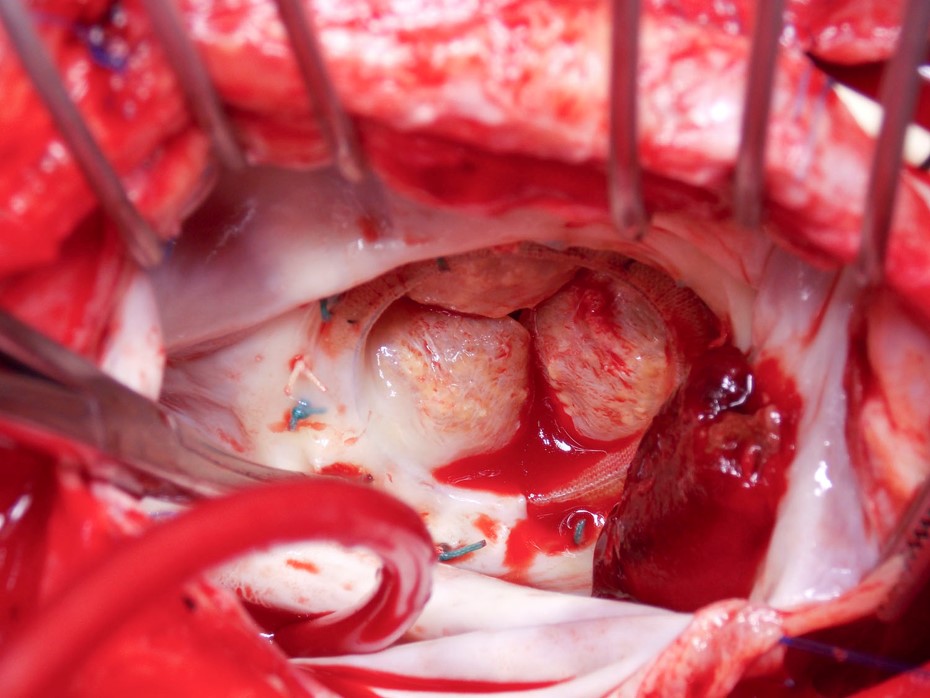
最後に、おそらく最も議論の余地があるのは、TAVRを受けた患者に対して抗凝固療法のアプローチを変えるべきかということであろう。 当初は,これらの患者をアスピリンとクロピドグレルで治療することが既定路線であった。これは,無作為化試験で行われたアプローチであったからである。 最近、心電図を用いた4次元コンピュータ断層撮影法(CTA)により、生体大動脈弁の弁尖移動度の低下と弁尖の肥厚低下が報告され、弁膜症が示唆された17,18。 重要なことは、これらのCTA異常はワルファリンによって消失する可能性があり、初期の抗凝固療法が行われなかったことが危険因子となりうることです19。しかし、現在のところ、これらの画像所見の臨床的意義は明らかではありません20。 幸い,TAVR後のリバーロキサバンと抗血小板療法を比較する無作為化試験GALILEO(Global Study Comparing a Rivaroxaban-Based Antithrombotic Strategy to an Antiplatelet-Based Strategy After Transcatheter Aortic Valve Replacement to Optimize Clinical Outcomes)が進行中で貴重な知見が得られるであろう21)。
結論
全体として,生体弁を有する患者において,早期の非手術的血栓塞栓事象はまれである。 さらに、顕性弁血栓症の発生率は低いと思われ、亜急性弁血栓症が弁の耐久性に及ぼす影響についてはまだ定義されていない。 これらの観察に加え、ワルファリンによる出血リスクの上昇を考慮し、我々は術後の抗凝固療法を選択的に行うことを提唱している(図3)。 生体大動脈弁の場合、心房細動などの確立した危険因子を持つ患者には、3〜6ヶ月の抗凝固療法が適応となります。 最近の新しいエビデンスによれば、ドップラー弁膜勾配の原因不明の増加や葉の肥厚の低下など、心エコーやCTAの異常所見がある患者には、抗凝固療法と綿密な経過観察を考慮する必要がある。 最後に、データは少ないが、生体弁を使用した患者は血栓性合併症のリスクが高いようであり、3〜6ヶ月間のルーチンの抗凝固療法が推奨される。
図3:生体弁置換術後の抗凝固療法へのアプローチ案
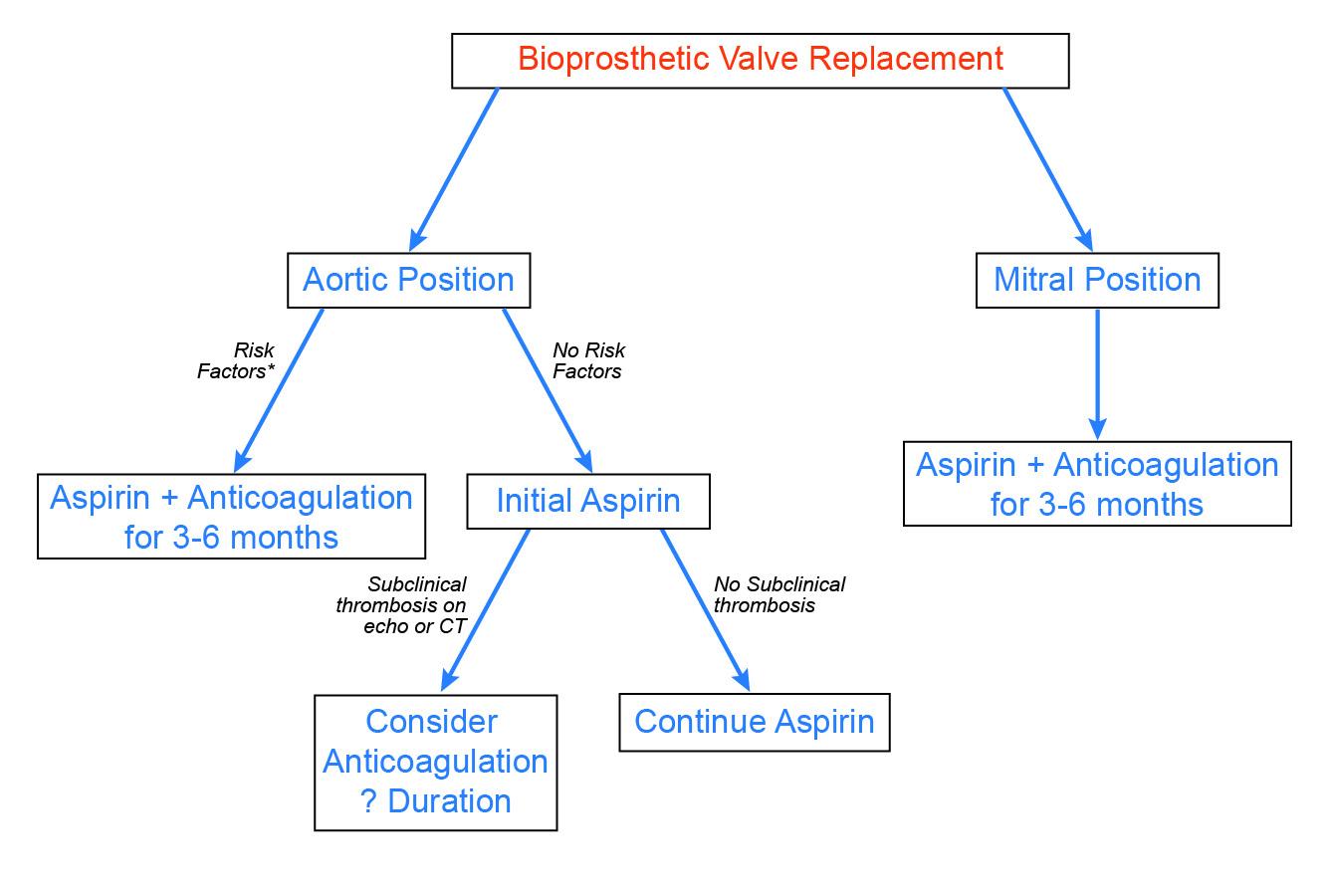
この記事は、免許を持つ医療従事者を対象とした教材を含み、教育および情報提供の目的でのみ使用されることを意図しています。 内容は特定の医療およびヘルスケアに関するものですが、個別の医療アドバイスに代わるものではなく、また個別の医療または健康関連の決定を行うための唯一の根拠として使用することを意図するものではありません。 記載されている見解や意見は、寄稿者及び編集者のものであり、必ずしもACCの見解を示すものではありません。 本資料は、取り上げた医学的状況に対する唯一の、あるいは必ずしも最良の、方法または手順を提示することを意図したものではなく、むしろアプローチ、見解、声明または意見を示すことを意図したものである。
- Pibarot P, Dumesnil JG. 人工心臓弁:最適な人工弁の選択と長期管理。
- Mack MJ, Douglas PS, Holmes DR.循環 2009;119:1034-48. 経カテーテル大動脈弁置換術後の弁血栓症にさらに光を当てる。 J Am Coll Cardiol 2016;67:656-8.
- Heras M, Chesebro JH, Fuster V, et al.High risk of thromboemboli early after bioprosthetic cardiac valve replacement.邦訳は「生体弁置換術後の血栓症」。 J Am Coll Caridol 1995;25:1111-9.
- Roudaut R, Serri K, Lafitte S. Thrombosis of prosthetic heart valves: diagnosis and therapeutic considerations.心臓弁の血栓症:診断と治療に関する考察。 Heart 2007;93:137-42.
- Masri A, Gillinov AM, Johnston DM, et al. 生体弁移植を受ける患者における抗凝固療法対抗血小板療法または無治療:系統的レビューとメタ解析.Masri A, Gillinov AM, Johnston DM, et al. Heart 2017;103:40-80.
- R Core Team (2015). R: A language and environment for statistical computing. R Foundation for Statistical Computing; Vienna, Austria. で入手可能。 https://www.R-project.org/. (関数 power.prop.test α = 0.05 and β = 0.8 を使用)
- Aramendi JI, Mestres CA, Martinez-León J, Campos V, Muñoz G, Navas C. Triflusal versus oral anticoagulation for primary prevention of thromboembolism after bioprosthetic valve replacement (trac): prospective, randomized, co-operative trial.(生体置換後血栓症予防におけるトリフルーザル対経口抗凝固療法:プロスペクティブ・ランダマイズ・コオペラティブ試験). Eur J Cardiothorac Surg 2005;27:854-60.
- Colli A, Mestres CA, Castella M, Gherli T. Comparing warfarin to aspirin (WoA) after aortic valve replacement with the St.Jude Medical Epic heart valve bioprosthesis: Results of the WoA Epic pilot trial.大動脈弁の人工心臓への置換術後、ワルファリンとアスピリンの比較. J Heart Valve Dis 2007;16:667-71.
- Mérie C, Køber L, Skov Olsen P, et al. Bioprosthetic aortic valve replacement after warfarin therapy duration with risk of mortality, thromboembolic complications, and bleeding.Association of warfarin therapy duration after biological aortic valve replacement in mortality, and blood. JAMA 2012;308:2118-25.
- Cremer PC, Rodriguez LL, Griffin BP, et al.生体弁置換術の早期失敗。 心エコー図と手術所見の相関によるメカニズムの洞察。 J Am Soc Echocardiogr 2015;28:1131-48.
- Brown ML, Park SJ, Sundt TM, Schaff HV.他。 大動脈位に生体弁を装着した患者における早期血栓症リスク。 J Thorac Cardiovasc Surg 2012;144:108-11.
- Nishimura RA, Otto CM, Bonow RO, et al. 2014 AHA/ACC guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines.心臓弁膜症の患者管理ガイドライン(2014 AHA/ACCガイドライン)。 J Am Coll Cardiol 2014;63:e57-185.
- Egbe AC, Pislaru SV, Pellikka PA, et al. Bioprosthetic Valve Thrombosis Versus Structural Failure(生体弁膜症対構造不全): 臨床的および心エコー的な予測因子。 J Am Coll Cardiol 2015;66:2285-94.
- Stewart WJ. 生体人工弁の血栓症。 無視してもいいのか? J Am Coll Cardiol 2015;66:2295-7.
- Russo A, Grigioni F, Avierinos JF, et al.Thromboembolic complications after surgical correction of mitral regurgitation incidence, predictors, and clinical implications.「僧帽弁閉鎖不全症の外科的矯正後の血栓症合併症の発生率、予測因子、臨床的意味合い。 J Am Coll Cardiol 2008;51:1203-11.
- Butnaru A, Shaheen J, Tzivoni D, Tauber R, Bitran D, Silberman S. Diagnosis and treatment of early bioprosthetic malfunction in the mitral valve position due to thrombus formation.(血栓形成による僧帽弁位置の生体機能低下の診断と治療)。 Am J Cardiol 2013;112:1439-44.
- Makkar RR, Fontana G, Jilaihawi H, et al. Possible Subclinical Leaflet Thrombosis in Bioprosthetic Aortic Valves.(生体人工大動脈弁の潜在的リーフレット血栓症の可能性). N Engj J Med 2015;373:2015-24.
- Pache G, Schoechlin S, Blanke P, et al. Early hypo-attenuated leaflet thickening in balloon-expandable transcatheter aortic heart valves.(バルーン拡張型経カテーテル大動脈弁の早期の葉脈肥厚)。 Eur Heart J 2016;37:2263-71.
- Hansson NC, Grove EL, Andersen HR, et al. Transcatheter Aortic Valve Thrombosis: Incidence, Predisposing Factors, and Clinical Implications.経カテーテル大動脈弁血栓症:発生率、素因、臨床的意義. J Am Coll Cardiol 2016;68:2059-69.
- Laschinger JC, Wu C, Ibrahim NG, Shuren JE.の項参照。 生体大動脈弁における葉身の動きの減少–FDAの見解。 N Engj J Med 2015;373:1996-8.
- Global Study Comparing arivAroxaban-based Antithrombotic Strategy to antipLatelet-based Strategy After Transcatheter aortIc vaLve rEplacement to Optimize Clinical Outcomes (GALILEO) (ClinicalTrails.gov website)の記事。 2016. で閲覧可能。 https://clinicaltrials.gov/ct2/show/NCT02556203. Accessed 11/29/2016.
臨床トピックスです。 抗凝固管理、不整脈と臨床EP、心臓外科、心不全・心筋症、侵襲的心血管造影・インターベンション、非侵襲的画像診断、心臓弁膜症、抗凝固管理と心房細動、心房細動・上室性不整脈。 大動脈手術、心臓手術と不整脈、心臓手術と心不全、心臓手術とVHD、急性心不全、インターベンションとイメージング、インターベンションと構造心疾患、血管造影、心エコー・超音波、核医学イメージング
Keywords 大動脈弁、大動脈弁狭窄症、心房細動、アスピリン、人工血管、症例対照研究、血管造影、狭窄、病理学的、心エコー、経食道、心電図、心不全、心臓弁膜症、大動脈弁狭窄症、心房細動、心房細動、心不全、心臓弁膜症、血管造影、心エコー、経食道心エコー、心エコー、心エコーコーコー、心電図、血管造影、血管造影、血管造影、心エコー 人工心臓, 僧帽弁, 僧帽弁狭窄症, 再手術, 危険因子, 脳卒中, 縫合糸, 血栓症, チクロピジン, 経カテーテル大動脈弁置換術, ビタミン K, ウォーファリン
< 一覧へ戻る