はじめに
鉄とアルコールの吸収に関する人類史上最初の言及は、テッサリアの伝説によると、イフィコスのアポロドルスが、野原に立って父親が子羊を去勢するのを見て、同じ罰で脅迫され、大人になったとき、アポロドルスはインポだったというものです。 Melampusという魔術師は、禿鷹に感化され、Apolodorusに、彼の父が子羊を去勢し、彼が脅されていたナイフの錆をワイングラスで飲ませて治した
私たちの病院で見られるアルコール患者の数は、それに伴うすべての病的状態を考慮すると、入院を必要とする患者と同様に多数である。
私たちの目的は、アルコール依存症に存在する血液学的病態の1つで、断酒だけでしばしば逆行する可能性のある鉄芽球性貧血とヘモシデロシスを思い出すことである。
1956年にBjorkmanが慢性難治性貧血と鉄芽球性輪症の患者4名を骨髄細胞のPrussian blue染色で報告しました。
これらの鉄芽球の輪がアルコールと関連しているという最初の証拠は、1965年にMac GibbonとMollinによって提案され、以来アルコール中毒がこの病理の最も一般的な原因となった。
1969年にHines(iを1に置き換える)は、慢性アルコール中毒において断酒による可逆的鉄芽球貧血の発生を説明した。
アルコールの影響
アルコールの造血組織に対する複数の病的影響(2で置き換え)は、次のように分けられる。
アルコールの直接作用によるもの
栄養不足による二次的作用に起因するもの
肝臓疾患によるもの
アルコール依存症では貧血がよく起こります。(3で置き換え)このうち、最も一般的なのは巨赤芽球性貧血と鉄芽球性貧血である。
後者は栄養的要因とビタミンB6代謝の障害に関連すると考えられる。
赤血球ピリドキサールホスホキナーゼ活性阻害の結果として、ピリドキシンがビタミンB6の活性型であるピリドキサールリン酸に変化する能力の低下が証明された。
また、エタノールは細胞内のピリドキサールリン酸(4で置き換え)の分解を促進することにより、膜アルカリホスファターゼの刺激剤として働く可能性も示唆されています。 このピリドキシン代謝の変化は、ピリドキシンの代謝物である4-ピリドキシン酸の尿中排泄量の減少、血清ピリドキサールリン酸の減少によって裏付けられます。
また、ピリドキサールリン酸は、鉄を含むヘモグロビン分画、すなわちヘモの前駆体の一つであるδ-アミノレブリン酸の合成にアジュバント因子として作用します。
他の研究では、エタノールが直接作用するだけでなく、その代謝物であるアセトアルデヒドを介して作用することが明らかにされています。 また、アセトアルデヒドは、リン酸化ビタミンB6化合物の分解を促進することにより、ピリドキサールリン酸の分解を増加させて血清ピリドキサールリン酸の減少を招き、in vitroでのヒト赤血球中のピリドキサールリン酸の生成を悪化させるとされている。
鉄染色法(プルシアンブルー染色、パール染色)を用いると、ヘモシデリンやフェリチンと思われる非ヘム鉄含有金属顆粒が赤芽球の核の周りにリングを形成する傾向にあります。 これらは鉄芽球リングあるいはリング鉄芽球と呼ばれる。
電子顕微鏡で見ると、これらの鉄芽球はミトコンドリアあるいは細胞質体のレベルで鉄が沈着していることがわかる。
これらの形態異常は、赤血球形成不全のすべての特徴と関連している:赤血球過形成、骨髄赤血球前駆体による鉄の取り込み増加、鉄の循環ヘモグロビンへの逆流による正常以下の取り込み、高フェレミア、正常芽球の巣内破壊、貧血、および細片球減少を引き起こしているのです。
赤血球骨髄の鉄芽球性リングの頻度は、慢性疾患患者、栄養失調のアルコール患者において高くなる。
臨床的・実験的証拠から、アルコール依存症患者における鉄芽球性貧血の発症には栄養的要因が重要であることが示唆された。
ヒトボランティアへの実験的アルコール慢性投与により、骨髄に鉄芽球性変化が生じた。
食事中のピリドキシンや葉酸が少ない状態でアルコールを投与すると、ほとんどの対象者で数週間後に
サイドボーラストの輪が発生した。
1970年にHinesとCowanはピリドキシンからピリドキサールリン酸へのリン酸化の変化に言及し、3つの調査によりピリドキシン代謝の障害を確認した:
アルコール補給の低葉酸食を維持した被験者3人のうち2人でピリドキサールリン酸と鉄芽球減少輪が生成されました。 7252>
慢性疾患のアルコール患者にピリドキシンを投与すると、対照群と比較してピリドキサールリン酸の生成に欠損が見られるようになった。
彼らは、アルコール依存症の被験者において、赤血球酵素によるピリドキシンからピリドキサールリン酸への変換がin vitroで減少したことを報告しています。 このことから、アルコールが赤血球のピリドキシンホスホリラーゼを直接的に抑制していることが推測される。 しかし、ピリドキサールリン酸の減少に関する別の説明として、アルコールの主要代謝物であるアセトアルデヒドが膜ホスファターゼ活性を刺激し、赤血球から血漿区画に移動するピリドキサールリン酸の量も減少させることが示唆された。
しかし、どのようなメカニズムであっても結果は同じで、いずれも赤芽球(鉄芽球)に含まれる鉄の量が増加します。
鉄芽球症では、赤血球への鉄の取り込みがうまくいかず、低色素症、赤血球生成不全、副血の増加などを引き起こします。
アルコール依存症における鉄過剰症(5で置き換え) アルコール依存症における鉄過剰症の原因は、アルコール飲料(特にワイン)の鉄分の増加を含め、単独または複合的に関与していることが多くなっています。 エタノールによる胃酸分泌の増加、溶血、消化管出血、葉酸欠乏、肝障害による腸管吸収の増加、膵障害、さらに副血を増加させ、ヘモシデロシスに至った。
デスフェロキサミンなどの鉄キレート剤を投与し、その後シデラーを測定すれば、鉄貯蔵量を半定量的に評価することができる。 7252>
しかし、他の研究では、入院中のアルコール患者において、血清鉄および/またはフェリチン濃度の両方が正常範囲内であるか、あまり上昇しないことが示されている。 食道静脈瘤による消化管出血がある場合、出血前は鉄の貯蔵量が正常値より多くても、枯渇している可能性があるため、これらの違いは研究対象となる患者の選択によるものと考えられる。
最後に、血清鉄を測定するために行われたほとんどの研究において、これらは常にアルコール中毒者で上昇し、鉄沈着とアルコール摂取量との間に相関関係が認められ、この要素がシデロシスの原因であることを示唆していることに注目すべきです。
鉄の吸収
1日に約5~15mgの鉄を摂取しても10%しか吸収されない
鉄の吸収に影響を与える要因は、管内、粘膜、全身の3段階で介入することができる。
内腔レベルでは、鉄の吸収はさまざまな食品の相互作用に依存することが知られており、アミノ酸のように吸収を促進するものと、吸収を低下させるものがあります。 7252>
Hemosiderosisを説明する試みとして、アルコール中毒患者の食事にはこの元素が非常に豊富に含まれていると最初に考えられた。 この観察は、バンタスヘモシデローシス、あるいはバンタスヘモシデローシスと呼ばれるものに基づいて行われた。 南アフリカ人がこれらの部族について行った研究によると、彼らが作っていたケフィアというビールのような飲み物は、鉄の容器で醸造されており、1リットルあたり30〜100mgの鉄分を含んでいることがわかった。 アルコール度数は非常に低く、1日に1000mgもの鉄分を大量に摂取していたという。
異なるアルコール飲料に含まれる鉄の量は非常に多様で、1リットルあたり350mg(ルーマニア)に達する場合もありますが、一般的にワイン(白、クラレット、赤)にはこの金属が豊富に含まれていると考えられています。
しかし、アルコール中毒者の中には、ワインではなく、ウィスキーやビールなど、ごく微量の鉄分を含む酒を主体に飲む人も少なくありません。
一方、バンタスの研究にもかかわらず、食事中の鉄分の過剰は、ヘモジドーシスの発症の十分な理由とはなりません。 そのため、エチオピアでは鉄分を多く含むテフという種子が食事の基本となっており、この金属を1日に300〜500mg摂取することが必要とされています。 このように摂取しても沈着量は増えず、鉄欠乏性貧血の頻度は一般人と変わらない。
したがって、食品中の鉄分量に価値がないことは明らかである。
これまでのところ、アルコールは鉄の吸収において管内レベルでは何の役割も果たしていないようです。
一般的なレベルでは、貯蔵鉄の状態がその吸収を左右し、減少すれば吸収が増加し、逆もまた然りであることが知られています。 赤血球生成もこのレベルで関与しており、増加するとその吸収を増加させる。 アルコールは血漿中の鉄のターンオーバーを促進しないようで、その吸収の増加を説明できる。
粘膜レベルでは、粘膜に含まれる鉄の量や、タンパク合成のレベルが、鉄の吸収に影響を与えることがある。 アルコール摂取後の葉酸欠乏は、鉄吸収の増加とそれに続くシデロシスの原因となり、アルコールの柔組織、特に肝臓への有害作用を悪化させることが示されています。
動物実験では、慢性アルコール投与は腸の鉄吸収増加を伴うことが示されていますが、そのメカニズムは不明でした。
十二指腸粘膜を通過する鉄のトランスロケーションに関与する少なくとも3つのメカニズムが、この10年間で証明されました。
トランスポーター介在(制御)
非エステル化脂肪酸による受動的メカニズム
(非制御)細胞外からの侵入
In vivo および in vitro 研究により、慢性アルコール患者における腸の透過性増大は腸の鉄吸収メカニズムの可能性があることが示されました。
他の研究では、アルコール依存症患者の腸管粘膜の鉄を取り込む本質的な能力が増加している可能性が示唆されている。
血清鉄が増加している者では、入院1週目に網状赤血球の発達に伴い鉄測定値が減少することが確認された。 また、鉄芽球性変化は可逆的であることが観察され、他の著者と一致した。 特徴的なリングは入院後1週間で骨髄から消失したが、一部は12日間持続した。
最近(6に置き換えて)、慢性アルコール中毒の患者において血清アシアロトランスフェリン値の増加が認められ、これは正常なトランスフェリン変異体に比べて組織特に肝細胞への鉄放出能力が増大していることを示しています。 この欠乏は、アルコール中毒者における鉄芽球性変化の発現に必要な前提条件である可能性が示唆されているが、他の著者は、著しい貧血にもかかわらず、骨髄に巨赤芽球性変化を認めず、末梢血に巨赤芽球症や好中球性過多もなく、血清および赤血球葉酸濃度は正常であるとして、異論を唱えている。
アルコール依存症の患者さんでは、結核や悪性疾患、腎不全などによる慢性疾患の貧血に、鉄芽球性貧血を伴うことが多く、このような患者さんが非常に多いことに注意する必要があります。
要約すると、アルコール摂取と不十分な食事は、鉄芽球性貧血およびヘモジデローシスの発症につながると考えられ、その病因はまだ確立されていませんが、考えられる要因としては次のようなものが挙げられます:
ヘム合成の一つ以上のステップに対するアルコールの毒性効果。
ピリドキサールリン酸の枯渇につながる栄養状態の悪さ、アセトアルデヒド、肝臓疾患またはその両方による異化の促進との関連
葉酸不足が悪化し、栄養補給の中止と補充が主役となる場合。
臨床例:
3ヶ月前から下肢(鞍上1/6、鞍下2/6)と仙骨の軟性浮腫、腹部膨満、粘膜皮膚蒼白、無力症、進行性アディナミで入院した55歳男性患者さんです。
病歴:
慢性アルコール中毒(1日2~3リットルのワインやビール)と喫煙(1日40本)、いずれも過去30年間。
病棟での検査結果:
胸部X線:右横隔膜洞の浸潤。 心胸部指数がやや上昇。
胸腔穿刺:滲出性特徴。 HTOのため、除菌赤血球2単位の輸血が適応となる。
予備診断:
Etiological: Chronic ethylism。 喫煙<7252><254>病態生理:腹水・浮腫症候群。 腹水・浮腫症候群。 腹水-浮腫性塗抹標本。 貧血気味。 胸水がたまる。 肝不全<7252><254>病理組織学的:肝腫大。 心肥大<7252><254>入院中に実施した検査結果:<7252><254>FEDA:慢性胃炎<7252><254>ダブルコントラスト注腸:腸管通過性保持<7252><254>心エコー図。 中等度の心嚢液貯留.
胸水:右胸水.
腹水:肝臓は脂肪肝に適合.
血清学:VDRL、シャーガス、BおよびC型肝炎は陰性です。
PAMO and BMO:骨髄に赤色系列の重度の造血障害あり
Perls: 細胞内および細胞外の鉄顆粒が増加することが認められる。
PBH:得られた材料は、診断結論のための代表的なものではなかった。
検査室
Hematocrit (%):11から変動した。8~19
赤血球(x10E12/l):1.1~1.94の変動を示した
白血球(x10E9/l):7.7~9.9の変動を示した。2
ヘモグロビン(g/dL):4.4から6までとなった。8
血小板(x10E9/l):102から346
血清(mg/dl):248から75
フェリチン(ng/dl)の範囲である。 594
TIBC(Total Iron Binding Capacity)(mg/dl):360
トランスフェリン飽和率:95~24
総ビリルビン(mg/dl):1~24の変動を呈し、1.5~2.0mg/dlの変動を呈し、2.0mg/dlの変動を呈す。6から0.51
直接ビリルビン(mg/dl):1.92から0.18
間接ビリルビン(mg/dl):2.99から0.33
治療:
低塩・低蛋白食を実施します。 水制限.
PHP 21滴/分で交互に滴下。 アルブミン1瓶を8時間おきに並行して投与し、その後フロセミドを1アンプル投与する。 スピロノラクトン 12時間おきに1錠。 フィトメナジオン(コナシオン)1アンプル12時間ごと
ラクチュロース(ラクチュロン)大さじ1杯6時間ごと。 ビタミンB群 12時間おきに1錠
患者の反応が良いため、利尿剤とビタミンB群の内服治療を継続する。 7252>
患者は腹水性浮腫の状態に対して良好な臨床経過を示したため、ビタミンBを投与し、アルコールを摂取しないように助言して退院した。
当院のメディカルクリニックの外来診療とアルバレス病院の血液内科によるメディカルコントロールを継続。
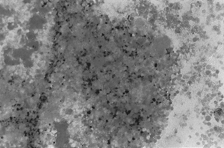
PAMO X 100
– Perls staining. 細胞外の鉄の沈着が激しい髄質の塊が目立つ。
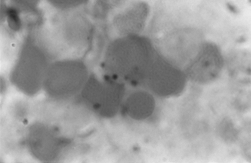
PAMO X 1000
– Perls staining. 赤芽球内鉄沈着が認められる。
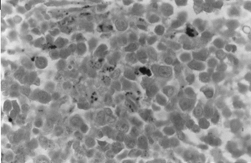
BMOX100
– Perls 染色。 赤芽球内外の高密度な鉄の集積が観察されるところ。
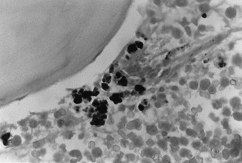
BMO X 1000
– ペリス染色。 細胞内外の高密度な鉄の集積が観察されるところ。
この患者は、入院後の経過も良好でした。 60日後の血液検査の結果は、HTO43%、GR5.1 X 10E12/L、GB8.7 X10E9/L、HB13.9 g/di、Plaq.354 X10E9/Lで、治療遵守のみでした。
120日後にも同じ血液検査結果でモニターされました。