Introduzione
La produzione e il consumo di rifiuti plastici stanno aumentando ad un ritmo allarmante, con l’aumento della popolazione umana, la rapida crescita economica, la continua urbanizzazione e i cambiamenti nello stile di vita. Inoltre, la breve durata di vita della plastica accelera la produzione di rifiuti plastici su base giornaliera. La produzione globale di plastica è stata stimata in circa 300 milioni di tonnellate all’anno ed è in continuo aumento ogni anno (Miandad et al., 2016a; Ratnasari et al., 2017). La plastica è fatta di idrocarburi petrolchimici con additivi come ritardanti di fiamma, stabilizzatori e ossidanti che la rendono difficile da bio-degradare (Ma et al., 2017). Il riciclaggio dei rifiuti plastici viene effettuato in diversi modi, ma nella maggior parte dei paesi in via di sviluppo, lo smaltimento a cielo aperto o in discarica è una pratica comune per la gestione dei rifiuti plastici (Gandidi et al., 2018). Lo smaltimento dei rifiuti plastici nelle discariche fornisce un habitat per insetti e roditori, che possono causare diversi tipi di malattie (Alexandra, 2012). Inoltre il costo del trasporto, della manodopera e della manutenzione possono aumentare il costo dei progetti di riciclaggio (Gandidi et al., 2018). Inoltre, a causa della rapida urbanizzazione, il terreno disponibile per le discariche, soprattutto nelle città, si sta riducendo. La pirolisi è una tecnica comune utilizzata per convertire i rifiuti plastici in energia, sotto forma di combustibili solidi, liquidi e gassosi.
La pirolisi è la degradazione termica dei rifiuti plastici a diverse temperature (300-900°C), in assenza di ossigeno, per produrre olio liquido (Rehan et al., 2017). Diversi tipi di catalizzatori sono utilizzati per migliorare il processo di pirolisi dei rifiuti plastici in generale e per aumentare l’efficienza del processo. I catalizzatori hanno un ruolo molto critico nel promuovere l’efficienza del processo, indirizzando la reazione specifica e riducendo la temperatura e il tempo del processo (Serrano et al., 2012; Ratnasari et al., 2017). Una vasta gamma di catalizzatori sono stati impiegati nei processi di pirolisi della plastica, ma i catalizzatori più ampiamente utilizzati sono ZSM-5, zeolite, Y-zeolite, FCC, e MCM-41 (Ratnasari et al., 2017). La reazione catalitica durante la pirolisi dei rifiuti plastici su catalizzatori acidi solidi può includere reazioni di cracking, oligomerizzazione, ciclizzazione, aromatizzazione e isomerizzazione (Serrano et al., 2012).
Diversi studi hanno riportato l’uso di catalizzatori microporosi e mesoporosi per la conversione dei rifiuti plastici in olio liquido e carbone. Uemichi et al. (1998) hanno effettuato la pirolisi catalitica del polietilene (PE) con catalizzatori HZSM-5. L’uso di HZSM-5 ha aumentato la produzione di olio liquido con la composizione di composti aromatici e isoalcani. Gaca et al. (2008) hanno effettuato la pirolisi dei rifiuti plastici con MCM-41 modificato e HZSM-5 e hanno riportato che l’uso di HZSM-5 ha prodotto idrocarburi più leggeri (C3-C4) con il massimo di composti aromatici. Lin et al. (2004) hanno usato diversi tipi di catalizzatori e hanno riferito che anche la miscelazione di HZSM-5 con SiO2-Al2O3 mesoporoso o MCM-41 ha portato alla massima produzione di olio liquido con una produzione minima di gas. Aguado et al. (1997) hanno riportato la produzione di composti aromatici e alifatici dalla pirolisi catalitica di PE con HZSM-5, mentre l’uso di MCM-41 mesoporoso ha diminuito i composti aromatici prodotti a causa della sua bassa attività catalitica acida. L’uso di catalizzatori sintetici ha migliorato il processo generale di pirolisi e la qualità dell’olio liquido prodotto. Tuttavia, l’uso di catalizzatori sintetici ha aumentato il costo del processo di pirolisi.
I catalizzatori NZ possono essere usati per superare le sfide economiche della pirolisi catalitica che viene con l’uso di catalizzatori costosi. Negli ultimi anni, NZ ha guadagnato un’attenzione significativa per le sue potenziali applicazioni ambientali. Naturalmente, NZ si trova in Giappone, USA, Cuba, Indonesia, Ungheria, Italia e Regno dell’Arabia Saudita (KSA) (Sriningsih et al., 2014; Nizami et al., 2016). Il deposito di NZ in KSA si trova principalmente in Harrat Shama e Jabbal Shama e contiene principalmente minerali di mordenite con alta stabilità termica, rendendolo adatto come catalizzatore nella pirolisi dei rifiuti plastici. Sriningsih et al. (2014) hanno modificato la NZ di Sukabumi, Indonesia, depositando metalli di transizione come Ni, Co e Mo e hanno effettuato la pirolisi del polietilene a bassa densità (LDPE). Gandidi et al. (2018) hanno utilizzato NZ da Lampung, Indonesia per la pirolisi catalitica dei rifiuti solidi urbani.
Questo è il primo studio per indagare l’effetto della zeolite naturale saudita modificata, sulla qualità del prodotto e sulla resa dalla pirolisi catalitica dei rifiuti plastici. Il catalizzatore della zeolite naturale saudita è stato modificato tramite una nuova attivazione termica (TA-NZ) a 550°C e un’attivazione acida (AA-NZ) con HNO3 per migliorare le sue proprietà catalitiche. La pirolisi catalitica di diversi tipi di rifiuti plastici (PS, PE, PP e PET) come singoli o mescolati in diversi rapporti, in presenza di catalizzatori di zeolite naturale modificata (NZ) in un piccolo reattore di pirolisi su scala pilota, è stata effettuata per la prima volta. Sono state studiate la qualità e la resa dei prodotti di pirolisi come olio liquido, gas e carbone. La composizione chimica dell’olio liquido è stata analizzata tramite GC-MS. Inoltre, sono stati discussi il potenziale e le sfide delle bioraffinerie basate sulla pirolisi.
Materiali e metodi
Preparazione della materia prima e avvio del reattore
I rifiuti plastici usati come materia prima nel processo di pirolisi catalitica sono stati raccolti a Jeddah e comprendevano borse della spesa, bicchieri e piatti usa e getta, e bottiglie di acqua potabile, che consistono rispettivamente in polietilene (PE), polipropilene (PP), polistirene (PS) e polietilene tereftalato (PET). La selezione di questi materiali plastici è stata fatta in base al fatto che sono la fonte primaria di rifiuti plastici prodotti in KSA. Per ottenere una miscela omogenea, tutti i campioni di rifiuti sono stati frantumati in pezzi più piccoli di circa 2 cm2. La pirolisi catalitica è stata effettuata utilizzando un singolo o una miscela di questi rifiuti di plastica in diversi rapporti (Tabella 1). Sono stati usati 1000 g di materia prima, con 100 g di catalizzatore in ogni esperimento. La zeolite naturale saudita (NZ), raccolta da Harrat-Shama situata a nord-ovest della città di Jeddah, KSA (Nizami et al., 2016), è stata modificata mediante trattamento termico e acido e utilizzata in questi esperimenti di pirolisi catalitica. NZ è stata frantumata in polvere (<100 nm) in un mulino a sfere (Retsch MM 480) per 3 ore con 20 Hz/sec, prima della modifica e del suo utilizzo nella pirolisi. Per l’attivazione termica (TA), NZ è stata riscaldata in un forno a muffola a 550°C per 5 ore, mentre per l’attivazione acida (AA) NZ è stata immersa in una soluzione 0,1 M di acido nitrico (HNO3) per 48 ore e continuamente agitata utilizzando un agitatore digitale IKA HS 501 a 50 rpm. Successivamente, il campione è stato lavato con acqua deionizzata fino ad ottenere un pH normale.

Tabella 1.
Gli esperimenti sono stati condotti in un piccolo reattore di pirolisi su scala pilota a 450°C, utilizzando una velocità di riscaldamento di 10°C/min e un tempo di reazione di 75 min (Figura 1). La resa ottenuta di ogni prodotto di pirolisi è stata calcolata in base al peso, dopo il completamento di ogni esperimento. La caratterizzazione dell’olio liquido prodotto è stata effettuata per studiare l’effetto della composizione della materia prima sulla qualità dell’olio liquido prodotto in presenza di NZ modificato. La TGA è stata effettuata sul feedstock per ottenere le condizioni di processo ottimali come la temperatura e il tempo di reazione (75 min) in condizioni controllate. Nella TGA, sono stati presi 10 μg di ogni tipo di rifiuto plastico e riscaldati con una velocità di 10°C da 25 a 900°C sotto un flusso continuo di azoto (50 ml/min). Gli autori di questo studio hanno recentemente pubblicato un lavoro sull’effetto della composizione del feedstock e dei catalizzatori di zeolite naturali e sintetici senza modifica del catalizzatore su diversi tipi di rifiuti plastici (Miandad et al., 2017b; Rehan et al., 2017).

Figura 1. Piccolo reattore di pirolisi su scala pilota (Miandad et al., 2016b).
Setup sperimentale
Il piccolo reattore su scala pilota ha la capacità di essere utilizzato sia come pirolisi termica che catalitica, utilizzando diverse materie prime come materiali plastici e biomassa (Figura 1). In questo studio, i catalizzatori NZ modificati sono stati aggiunti nel reattore con la materia prima. Il reattore di pirolisi può contenere fino a 20 L di materia prima e la temperatura massima di lavoro sicura fino a 600°C può essere raggiunta con i tassi di riscaldamento desiderati. I parametri dettagliati del reattore di pirolisi sono stati pubblicati in precedenza (Miandad et al., 2016b, 2017b). Quando la temperatura aumenta oltre certi valori, i rifiuti plastici (polimeri organici) si convertono in monomeri che vengono trasferiti al condensatore, dove questi vapori vengono condensati in olio liquido. È stato utilizzato un sistema di condensazione continuo con un bagno d’acqua e un refrigerante ACDelco Classic per garantire che la temperatura di condensazione fosse mantenuta al di sotto dei 10°C e per assicurare la massima condensazione del vapore in olio liquido. L’olio liquido prodotto è stato raccolto dal serbatoio di raccolta dell’olio, ed è stata effettuata un’ulteriore caratterizzazione per scoprire la sua composizione chimica e le caratteristiche per altre potenziali applicazioni.
Metodi analitici
L’olio di pirolisi è stato caratterizzato usando diverse tecniche come la gascromatografia accoppiata alla spettrofotometria di massa (GC-MS), la spettroscopia infrarossa a trasformata di Fourier (FT-IR),
calorimetro a bomba e TGA (Mettler Toledo TGA/SDTA851) adottando i metodi standard ASTM. I gruppi funzionali nell’olio di pirolisi sono stati analizzati da uno strumento FT-IR, Perkin Elmer’s, UK. L’analisi FT-IR è stata condotta utilizzando un minimo di 32 scansioni con una media di 4 segnali IR cm-1 nella gamma di frequenza di 500-4.000 cm-1.
La composizione chimica dell’olio è stata studiata utilizzando un GC-MS (Shimadzu QP-Plus 2010) con rilevatore FI. È stata utilizzata una colonna capillare GC lunga 30 m e larga 0,25 mm rivestita con un film spesso 0,25 μm di fenil-metilpolisilossano al 5% (HP-5). Il forno è stato impostato a 50°C per 2 min e poi aumentato fino a 290°C utilizzando una velocità di riscaldamento di 5°C/min. La temperatura della sorgente ionica e della linea di trasferimento è stata mantenuta a 230 e 300°C e l’iniezione splitless è stata applicata a 290°C. La libreria di dati dello spettro di massa NIST08s è stata utilizzata per identificare i picchi cromatografici e le percentuali dei picchi sono state valutate per la loro area di picco totale del cromatogramma ionico (TIC). I valori di alto riscaldamento (HHV) dell’olio liquido prodotto ottenuto da diversi tipi di rifiuti plastici sono stati misurati seguendo il metodo standard ASTM D 240 con uno strumento Calorimetro a Bomba (Calorimetro Parr 6200), mentre la produzione di gas è stata stimata utilizzando la formula standard di equilibrio di massa, considerando la differenza di peso dell’olio liquido e del carbone.
Risultati e discussione
Analisi TGA del Feedstock
TGA è stata effettuata per ogni tipo di rifiuto plastico su base individuale per determinare la temperatura ottimale per la degradazione termica. Tutti i tipi di rifiuti plastici mostrano un comportamento di degradazione simile con la rapida perdita di peso degli idrocarburi entro il ristretto intervallo di temperatura (150-250°C) (Figura 2). La massima degradazione per ogni tipo di rifiuto plastico è stata raggiunta entro 420-490°C. PS e PP hanno mostrato una decomposizione a fase singola, mentre PE e PET hanno mostrato una decomposizione a due fasi in condizioni controllate. La decomposizione a fase singola corrisponde alla presenza di un legame carbonio-carbonio che promuove il meccanismo di scissione casuale con l’aumento della temperatura (Kim et al., 2006). La degradazione del PP è iniziata a una temperatura molto bassa (240°C) rispetto ad altre materie prime. La metà del carbonio presente nella catena del PP consiste in carbonio terziario, che promuove la formazione di carbocation durante il suo processo di degradazione termica (Jung et al., 2010). Questa è probabilmente la ragione per ottenere la massima degradazione del PP a una temperatura inferiore. La degradazione iniziale del PS è iniziata a 330°C e la degradazione massima è stata raggiunta a 470°C. Il PS ha una struttura ciclica, e la sua degradazione in condizioni termiche coinvolge sia la catena casuale che la scissione della catena finale, che migliora il suo processo di degradazione (Demirbas, 2004; Lee, 2012).
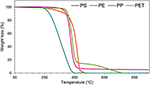
Figura 2. Analisi termogravimetrica (TGA) di PS, PE, PP e rifiuti plastici in PET.
PE e PET hanno mostrato un processo di decomposizione in due fasi; la degradazione iniziale è iniziata a temperature più basse seguita dall’altra fase di degradazione a una temperatura più alta. La degradazione iniziale del PE è iniziata a 270°C e si è propagata lentamente ma gradualmente fino alla temperatura di 385°C. Dopo quella temperatura, è stata osservata una forte degradazione, e il 95% di degradazione è stato raggiunto con un ulteriore aumento di circa 100°C. Un simile modello di degradazione a due fasi è stato osservato per la plastica PET e la degradazione iniziale è iniziata a 400°C con una forte diminuzione della perdita di peso. Tuttavia, la seconda degradazione è iniziata a una temperatura leggermente superiore (550°C). La degradazione iniziale di PE e PET può essere dovuta alla presenza di alcune impurità volatili come il filler additivo utilizzato durante la sintesi della plastica (Dimitrov et al., 2013).
Vari ricercatori hanno riportato che la degradazione di PE e PET richiede temperature più elevate rispetto ad altre plastiche (Dimitrov et al., 2013; Rizzarelli et al., 2016). Lee (2012) ha riferito che il PE ha una struttura ramificata a catena lunga e che la sua degradazione avviene tramite la scissione casuale della catena, richiedendo quindi una temperatura più alta, mentre la degradazione del PET segue la scissione casuale dei legami esteri che porta alla formazione di oligomeri (Dziecioł e Trzeszczynski, 2000; Lecomte e Liggat, 2006). La degradazione iniziale del PET era forse dovuta alla presenza di alcune impurità volatili come il dietilenglicole (Dimitrov et al., 2013). La letteratura riporta che la presenza di queste impurità volatili promuove ulteriormente il processo di degradazione dei polimeri (McNeill e Bounekhel, 1991; Dziecioł e Trzeszczynski, 2000). La differenza nelle curve TGA dei vari tipi di plastica potrebbe essere dovuta alla loro struttura mesoporosa (Chandrasekaran et al., 2015). Inoltre, Lopez et al. (2011) hanno riportato che l’uso di catalizzatori diminuisce la temperatura del processo. Pertanto, 450°C potrebbe essere presa come temperatura ottimale, in presenza di NZ attivata, per la pirolisi catalitica dei suddetti rifiuti plastici.
Effetto della materia prima e dei catalizzatori sulla resa dei prodotti di pirolisi
È stato esaminato l’effetto dell’attivazione termica e acida di NZ sulla resa del prodotto del processo di pirolisi (Figura 3). La pirolisi catalitica della plastica PS individuale utilizzando i catalizzatori TA-NZ e AA-NZ ha mostrato le più alte rese di olio liquido del 70 e 60%, rispettivamente, rispetto a tutti gli altri tipi di rifiuti plastici individuali e combinati studiati. L’alta resa di olio liquido dalla pirolisi catalitica di PS è stata riportata anche in diversi altri studi (Siddiqui e Redhwi, 2009; Lee, 2012; Rehan et al., 2017). Siddiqui e Redhwi (2009) hanno riferito che PS ha una struttura ciclica, che porta all’alta resa di olio liquido dalla pirolisi catalitica. Lee (2012) ha riferito che la degradazione di PS si è verificata attraverso entrambe le scissioni a catena casuale e a catena terminale, portando così alla produzione della struttura ad anello stabile del benzene, che migliora l’ulteriore cracking e può aumentare la produzione di olio liquido. Inoltre, in presenza di catalizzatori acidi, la degradazione di PS ha seguito un meccanismo di carbenium, che ha subito un’ulteriore idrogenazione (trasferimento di idrogeno inter/intramolecolare) e β-scissione (Serrano et al., 2000). Inoltre, la degradazione del PS si è verificata a una temperatura inferiore, rispetto ad altre plastiche come il PE, a causa della sua struttura ciclica (Wu et al., 2014). D’altra parte, la pirolisi catalitica di PS ha prodotto una maggiore quantità di char (24,6%) con il catalizzatore AA-NZ rispetto al catalizzatore TA-NZ (15,8%). Ma et al. (2017) hanno anche riportato l’alta produzione di char dalla pirolisi catalitica di PS con un catalizzatore di zeolite acida (Hβ). Gli alti numeri di produzione di char erano dovuti all’alta acidità del catalizzatore, che favorisce la produzione di char attraverso intense reazioni di reticolazione secondaria (Serrano et al., 2000).
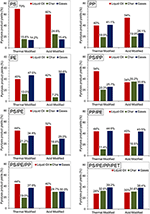
Figura 3. Effetto di TA-NZ e AA-NZ sulla resa del prodotto di pirolisi.
La pirolisi catalitica di PP ha prodotto un olio liquido maggiore (54%) con il catalizzatore AA-NZ rispetto al catalizzatore TA-NZ (40%) (Figura 3). D’altra parte, il catalizzatore TA-NZ ha prodotto grandi quantità di gas (41,1%), che può essere dovuto alla minore attività catalitica del catalizzatore TA-NZ. Secondo Kim et al. (2002) i catalizzatori con bassa acidità e aree superficiali BET con strutture microporose, favoriscono la degradazione iniziale di PP che può portare alla massima produzione di gas. Obali et al. (2012) hanno effettuato la pirolisi di PP con un catalizzatore carico di allumina e hanno riportato la massima produzione di gas. Inoltre, la formazione di carbocation durante la degradazione del PP, dovuta alla presenza di carbonio terziario nella sua catena di carbonio, può anche favorire la produzione di gas (Jung et al., 2010). Syamsiro et al. (2014) hanno anche riportato che la pirolisi catalitica di PP e PS con un catalizzatore di zeolite naturale attivato con acido (HCL) ha prodotto più gas rispetto al processo con un catalizzatore di zeolite naturale attivato termicamente, a causa della sua elevata acidità e area superficiale BET.
La pirolisi catalitica di PE con catalizzatori TA-NZ e AA-NZ ha prodotto quantità simili di olio liquido (40 e 42%). Tuttavia, le più alte quantità di gas (50,8 e 47,0%) sono state prodotte dal PE, usando AA-NZ e TA-NZ rispettivamente, rispetto a tutti gli altri tipi di plastica studiati. La produzione di carbone è stata più bassa in questo caso, 7,2 e 13,0% con AA-NZ e TA-NZ, rispettivamente. Vari studi hanno anche riportato la minore produzione di char dalla pirolisi catalitica del PE (Xue et al., 2017). Lopez et al. (2011) hanno riportato che i catalizzatori con alta acidità hanno migliorato il cracking dei polimeri durante la pirolisi catalitica. L’aumento del cracking, in presenza di un catalizzatore ad alta acidità, promuove la produzione di gas (Miandad et al., 2016b, 2017a). Zeaiter (2014) ha effettuato la pirolisi catalitica del PE con la zeolite HBeta e ha riportato il 95,7% di produzione di gas grazie all’alta acidità del catalizzatore. Anche Batool et al. (2016) hanno riportato la massima produzione di gas dalla pirolisi catalitica del PE, con catalizzatore ZSM-5 altamente acido. Secondo Lee (2012) e Williams (2006), il PE ha una struttura a catena lunga di carbonio, e la sua degradazione avviene in modo casuale in molecole a catena più piccola attraverso la scissione casuale della catena, che può promuovere la produzione di gas. Durante la pirolisi del PE, che detiene solo i legami C-H e C-C, inizialmente si è verificata la rottura della spina dorsale della macromolecola e ha prodotto radicali liberi stabili. Successivamente, le fasi di idrogenazione si sono verificate, portando alla sintesi di radicali liberi secondari (nuovo legame C-H stabile), che hanno portato alla β-scissione e prodotto un gruppo insaturo (Rizzarelli et al., 2016).
La pirolisi catalitica di PP/PE (rapporto 50/50%) non ha mostrato alcuna differenza significativa nelle rese complessive dei prodotti quando si utilizzano sia AA-NZ che TA-NZ. L’olio liquido prodotto dalla pirolisi catalitica di PP/PE era del 44 e 40% con i catalizzatori TA-NZ e AA-NZ, rispettivamente. Una leggera diminuzione nella resa dell’olio liquido da AA-NZ potrebbe essere dovuta alla sua alta acidità. Syamsiro et al. (2014) hanno riferito che AA-NZ con HCl ha un’alta acidità rispetto a TA-NZ, ha prodotto meno resa in olio liquido e ha avuto un’alta produzione di gas. Nel complesso la pirolisi catalitica di PP/PE ha prodotto la massima quantità di gas con basse quantità di char. L’alta produzione di gas può essere dovuta alla presenza di PP. La degradazione del PP migliora il processo di carbocation a causa della presenza di carbonio terziario nella sua catena di carbonio (Jung et al., 2010). Inoltre, la degradazione del PE in presenza di catalizzatore favorisce anche la produzione di gas con una bassa resa di olio liquido. Tuttavia, quando la pirolisi catalitica di PP e PE è stata effettuata separatamente con PS, è stata osservata una differenza significativa nella resa del prodotto.
C’è stata una differenza significativa nella resa di olio liquido del 54 e 34% per la pirolisi catalitica di PS/PP (rapporto 50/50%) con catalizzatori TA-NZ e AA-NZ, rispettivamente. Allo stesso modo, è stata osservata una differenza significativa nella resa del char del 20,3 e del 35,2%, mentre la resa elevata dei gas era del 25,7 e del 30,8% usando i catalizzatori TA-NZ e AA-NZ, rispettivamente. Lopez et al. (2011) e Seo et al. (2003) hanno riportato che un catalizzatore con alta acidità promuove il processo di cracking e produce la massima produzione di gas. Inoltre, la presenza di PP migliora anche la produzione di gas a causa del processo di carbocation durante la degradazione (Jung et al., 2010). Kim et al. (2002) hanno riportato che la degradazione del PP produce il massimo di gas in presenza di catalizzatori acidi.
La pirolisi catalitica di PS con PE (rapporto 50/50%) in presenza del catalizzatore TA-NZ ha prodotto il 44% di olio liquido, tuttavia il 52% di olio liquido è stato ottenuto utilizzando il catalizzatore AA-NZ. Kiran et al. (2000) hanno effettuato la pirolisi di PS con PE a diversi rapporti e hanno riportato che un aumento della concentrazione di PE ha diminuito la concentrazione di olio liquido con l’aumento del gas. La presenza di PS con PE promuove il processo di degradazione a causa della produzione di un anello di benzene stabile attivo da PS (Miandad et al., 2016b). Wu et al. (2014) hanno effettuato la TGA di PS con PE e hanno osservato due picchi, il primo per PS a bassa temperatura, seguito dalla degradazione di PE ad alta temperatura. Inoltre, la degradazione del PE segue un processo a catena radicale libera e un processo di idrogenazione, mentre il PS segue un processo a catena radicale che include vari passaggi (Kiran et al., 2000). Quindi, anche quando si considerano i fenomeni di degradazione, il PS risulta in una degradazione maggiore rispetto al PE e produce anelli di benzene stabili (McNeill et al., 1990).
La pirolisi catalitica di PS/PE/PP (rapporto 50/25/25%) ha mostrato rese di olio liquido leggermente inferiori rispetto alla pirolisi catalitica di tutti i singoli tipi di plastica. La resa in olio da entrambi i catalizzatori, TA-NZ e AA-NZ, in questo caso, è simile, 44 e 40%, rispettivamente. La produzione di carbone era più alta (29,7%) con il catalizzatore AA-NZ che (19,0%) con il catalizzatore TA-NZ, che può essere dovuto alle reazioni di polimerizzazione (Wu e Williams, 2010). Inoltre, l’aggiunta di PET con PS, PE e PP (rapporto 20/40/20/20%) ha ridotto le rese di olio liquido fino al 28 e al 30% complessivamente, usando i catalizzatori TA-NZ e AA-NZ, rispettivamente, con frazioni più alte di char e gas. Demirbas (2004) ha effettuato la pirolisi di PS/PE/PP e ha riportato risultati simili per la resa del prodotto. Adnan et al. (2014) hanno effettuato la pirolisi catalitica di PS e PET utilizzando il catalizzatore Al-Al2O3 con rapporti di 80/20% e hanno riportato solo il 37% di olio liquido. Inoltre, Yoshioka et al. (2004) hanno riportato la massima produzione di gas e carbone con una produzione trascurabile di olio liquido dalla pirolisi catalitica del PET. Inoltre, la massima produzione di carbone è stata riportata anche quando la pirolisi catalitica del PET è stata effettuata con altre plastiche (Bhaskar et al., 2004). La maggiore produzione di carbone dalla pirolisi del PET era dovuta alle reazioni di carbonizzazione e condensazione durante la pirolisi ad alta temperatura (Yoshioka et al., 2004). Inoltre, la presenza dell’atomo di ossigeno favorisce anche l’alta produzione di char dalla pirolisi catalitica del PET (Xue et al., 2017). Thilakaratne et al. (2016) hanno riportato che la produzione di radicali senza benzene, con due carboni attivati, è il precursore del coke catalitico dalla degradazione del PET.
Effetto dei catalizzatori sulla composizione dell’olio liquido
La composizione chimica dell’olio liquido prodotto dalla pirolisi catalitica di diversi rifiuti plastici utilizzando catalizzatori TA-NZ e AA-NZ sono stati caratterizzati mediante GC-MS (Figure 4, 5). La composizione dell’olio liquido prodotto è influenzata dai diversi tipi di materia prima e dai catalizzatori utilizzati nel processo di pirolisi (Miandad et al., 2016a,b,c). L’olio liquido prodotto dai singoli tipi di plastica come PS, PP e PE conteneva una miscela di composti aromatici, alifatici e altri idrocarburi. I composti aromatici trovati nell’olio, da PS e PE, erano più alti rispetto al PP usando il catalizzatore TA-NZ. I composti aromatici sono aumentati nell’olio da PS e PP ma si sono ridotti in PE quando si usa il catalizzatore AA-NZ. Il catalizzatore mesoporoso e acido porta alla produzione di idrocarburi a catena più corta a causa della sua elevata capacità di cracking (Lopez et al., 2011). Tuttavia, i catalizzatori microporosi e meno acidi favoriscono la produzione di idrocarburi a catena lunga in quanto il processo di cracking avviene solo sulla superficie esterna dei catalizzatori. Nel complesso, in presenza di catalizzatori, PE e PP seguono il meccanismo di scissione a catena casuale, mentre PS segue il meccanismo di unzipping o scissione della catena finale (Cullis e Hirschler, 1981; Peterson et al., 2001). La scissione della catena terminale porta alla produzione di monomeri, mentre la scissione della catena casuale produce oligomeri e monomeri (Peterson et al., 2001).
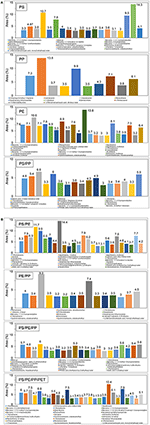
Figura 4. (A,B) GC-MS di olio liquido prodotto da diversi tipi di rifiuti plastici con TA-NZ.
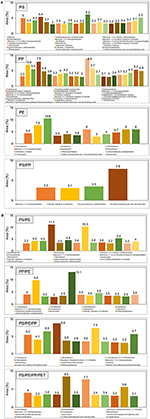
Figura 5. (A,B) GC-MS dell’olio liquido prodotto da diversi tipi di rifiuti plastici con AA-NZ.
L’olio liquido prodotto dalla pirolisi catalitica del PE, quando si usano entrambi i catalizzatori, produce principalmente naftalene, fenantrene, naftalene, 2-etenile, 1-pentadecene, antracene, 2-metil-, esadecano e così via (figure 4A, 5A). Questi risultati concordano con diversi altri studi (Lee, 2012; Xue et al., 2017). La produzione di un derivato del benzene rivela che TA-NZ migliora il processo di aromatizzazione rispetto a AA-NZ. Xue et al. (2017) hanno riportato che le olefine intermedie prodotte dalla pirolisi catalitica del PE, si sono ulteriormente aromatizzate all’interno dei pori dei catalizzatori. Tuttavia, la reazione di aromatizzazione porta ulteriormente alla produzione di atomi di idrogeno che possono migliorare il processo di aromatizzazione. Lee (2012) ha riportato che lo ZSM-5 ha prodotto più composti aromatici rispetto al catalizzatore mordenite, a causa della sua struttura cristallina.
Ci sono due possibili meccanismi che possono coinvolgere la degradazione del PE in presenza di un catalizzatore; l’astrazione di ioni ibridi dovuta alla presenza di siti Lewis o, a causa del meccanismo dello ione carbenio attraverso l’aggiunta di un protone (Rizzarelli et al., 2016). Inizialmente, la degradazione inizia sulla superficie esterna dei catalizzatori e successivamente procede con un’ulteriore degradazione nei pori interni dei catalizzatori (Lee, 2012). Tuttavia, i catalizzatori microporosi ostacolano l’ingresso di molecole più grandi e quindi dalla pirolisi catalitica del PE con catalizzatori microporosi vengono prodotti composti a catena di carbonio più elevata. Inoltre, in presenza di catalizzatori acidi, a causa del meccanismo del carbenio, la formazione di composti aromatici e olefinici può aumentare (Lee, 2012). Lin et al. (2004) hanno riportato la produzione di olefine altamente reattive, come prodotti intermedi durante la pirolisi catalitica del PE, che possono favorire la produzione di paraffina e composti aromatici nell’olio liquido prodotto. Inoltre, la presenza di un catalizzatore acido e di un atomo di idrogeno libero può portare all’alchilazione di toluene e benzene, convertendo il benzene intermedio alchilato alla produzione di naftalene a causa dell’aromatizzazione (Xue et al., 2017).
L’olio liquido prodotto dalla pirolisi catalitica di PS con TA-NZ e AA-NZ, contiene diversi tipi di composti. Alpha-Methylstyrene, Benzene, 1,1′-(2-butene-1,4-diyl)bis-, Bibenzyl, Benzene, (1,3-propanediyl), Phenanthrene, 2-Phenylnaphthalene e così via erano i principali composti trovati nell’olio liquido prodotto (Figure 4A, 5A). L’olio liquido prodotto dalla pirolisi catalitica di PS, con entrambi i catalizzatori attivati, contiene principalmente idrocarburi aromatici con alcune paraffine, naftalene e composti olefinici (Rehan et al., 2017). Tuttavia, in presenza di un catalizzatore, è stata raggiunta la massima produzione di composti aromatici (Xue et al., 2017). Ramli et al. (2011) hanno anche riportato la produzione di olefine, naftalene con composti aromatici dalla pirolisi catalitica di PS con Al2O3, supportato con catalizzatori Cd e Sn. La degradazione del PS inizia con il cracking sulla superficie esterna del catalizzatore ed è poi seguita dal reforming all’interno dei pori del catalizzatore (Uemichi et al., 1999). Inizialmente, il cracking del polimero viene effettuato dal sito acido di Lewis sulla superficie dei catalizzatori per produrre intermedi carbocationici, che evaporano ulteriormente o subiscono il reforming all’interno dei pori del catalizzatore (Xue et al., 2017).
La pirolisi catalitica di PS produce principalmente stirene e il suo derivato come i principali composti nell’olio liquido prodotto (Siddiqui e Redhwi, 2009; Rehan et al., 2017). La conversione dello stirene nel suo derivato è stata aumentata in presenza di catalizzatori protonati a causa dell’idrogenazione (Kim et al., 2002). Shah e Jan (2015) e Ukei et al. (2000) hanno riportato che l’idrogenazione dello stirene aumentava con l’aumento della temperatura di reazione. Ogawa et al. (1982) hanno effettuato la pirolisi di PS con il catalizzatore allumina-silice a 300°C e hanno trovato l’idrogenazione dello stirene al suo derivato. Ramli et al. (2011) hanno riportato il possibile meccanismo di degradazione del PS su catalizzatori acidi che può avvenire a causa dell’attacco di un protone associato ai siti acidi di Bronsted, con conseguente meccanismo dello ione carbenio, che subisce ulteriormente la β-scissione ed è poi seguito dal trasferimento di idrogeno. Inoltre, la reazione di reticolazione è stata favorita da forti siti acidi di Bronsted e quando questa reazione è avvenuta il cracking di completamento può diminuire in una certa misura e migliorare la produzione di carbone (Serrano et al., 2000). Inoltre, i catalizzatori di silice-allumina non hanno forti siti acidi di Bronsted, anche se potrebbero non migliorare la reazione di reticolazione ma favorire il processo di idrogenazione. Quindi, può essere la ragione per cui lo stirene non è stato trovato nell’olio liquido, tuttavia, il suo derivato è stato rilevato in quantità elevate (Lee et al., 2001). Xue et al. (2017) hanno anche riportato la dealchilazione dello stirene, dovuta al ritardo dell’evaporazione all’interno del reattore, che può portare a un processo di reforming migliorato e alla produzione di un derivato dello stirene. TA-NZ e AA-NZ contengono un’elevata quantità di allumina e silice che porta all’idrogenazione dello stirene al suo derivato, con conseguente produzione di monomeri di stirene invece di stirene.
La pirolisi catalitica di PP ha prodotto una miscela complessa di olio liquido contenente aromatici, olefine e composti di naftalina. Benzene, 1,1′-(2-butene-1,4-diyl)bis-, benzene, 1,1′-(1,3-propanediyl)bis-, antracene, 9-metil-, naftalene, 2-fenil-, 1,2,3,4-tetraidro-1-fenil-, naftalene, fenantrene ecc. erano i principali composti trovati nell’olio liquido (Figure 4A, 5A). Questi risultati sono in linea con altri studi che hanno effettuato la pirolisi catalitica di PP con vari catalizzatori (Marcilla et al., 2004). Inoltre, la degradazione di PP con AA-NZ ha portato alla massima produzione di composti fenolici. La maggiore produzione era forse dovuta alla presenza di siti altamente acidi, in quanto favorisce la produzione di composti fenolici. Inoltre, la presenza di un alto sito acido sui catalizzatori ha migliorato il meccanismo di oligomerizzazione, aromatizzazione e deossigenazione che ha portato alla produzione di composti poliaromatici e naftalenici. Dawood e Miura (2002) hanno anche riportato l’alta produzione di questi composti dalla pirolisi catalitica di PP con una HY-zeolite modificata ad alta acidità.
La composizione dell’olio dalla pirolisi catalitica di PP con PE contiene composti trovati nell’olio di entrambe le materie prime di tipo plastico individuale. Miandad et al. (2016b) hanno riferito che la composizione della materia prima influenza anche la qualità e la composizione chimica dell’olio. L’olio liquido prodotto dalla pirolisi catalitica di PE/PP contiene composti aromatici, olefinici e naftalenici. I principali composti trovati sono: benzene, 1,1′-(1,3-propandiyl)bis-, mono(2-ethylhexyl) estere, acido 1,2-benzendicarbossilico, antracene, pentadecano, fenantrene, 2-fenilnaftalene e così via (Figure 4B, 5B). Jung et al. (2010) hanno riferito che la produzione aromatica dalla pirolisi catalitica PP/PE potrebbe seguire il meccanismo di reazione Diels-Alder ed è poi seguita dalla deidrogenazione. Inoltre, la pirolisi catalitica di PP e PE effettuata individualmente con PS, ha prodotto principalmente composti aromatici a causa della presenza di PS. L’olio liquido prodotto da PS/PP contiene benzene, 1,1′-(1,3-propanediyl)bis, acido 1,2-benzenedicarbossilico, estere disoottile, bibenzile, fenantrene, 2-fenilnaftalene, benzene, (4-methyl-1-decenyl)- e così via (Figure 4A, 5A). La pirolisi catalitica PS con PE ha prodotto principalmente olio liquido con composti principali di azulene, naftalene, 1-metil-, naftalene, 2-etenile, benzene, 1,1′-(1,3-propanediyl)bis-, fenantrene, 2-fenilnaftalene, benzene, 1,1′-(1-metil-1,2-etanediyl)bis- e alcuni altri composti pure (Figure 4B, 5B). Miskolczi et al. (2006) hanno effettuato la pirolisi di PS con PE con un rapporto di 10 e 90%, rispettivamente, e hanno riportato la massima produzione di aromatici anche ad un rapporto molto basso di PS. Miandad et al. (2016b) hanno riportato che la pirolisi termica del PE con PS senza catalizzatore, ha portato alla conversione del PE in olio liquido con un’alta composizione di aromatici. Tuttavia la pirolisi termica del solo PE senza un catalizzatore lo ha convertito in cera invece di olio liquido a causa della sua forte struttura ramificata a catena lunga (Lee, 2012; Miandad et al., 2016b). Wu et al. (2014) hanno effettuato la TGA di PS con PE e hanno riportato che la presenza di PS favorisce la degradazione del PE, a causa della produzione di anelli benzenici stabili.
La composizione chimica dell’olio di pirolisi, per diversi gruppi funzionali, è stata studiata utilizzando FT-IR. I dati ottenuti hanno rivelato la presenza di gruppi funzionali aromatici e alifatici nell’olio (Figure 6, 7). Un picco molto forte a 696 cm-1 è stato osservato nella maggior parte degli oli liquidi ottenuti utilizzando entrambi i catalizzatori, che corrisponde all’alta concentrazione di composti aromatici. Altri due picchi, che sono evidenti, erano visibili a circa 1.456 e 1.495 cm-1 per C-C con legami singoli e doppi, corrispondenti a composti aromatici. Inoltre, alla fine dello spettro, forti picchi a 2.850, 2.923, e 2.958 cm-1 sono stati osservati in tutti i tipi di oli liquidi tranne il PS, corrispondenti al tratto C-H dei composti alcani. Nel complesso, l’olio liquido ottenuto dalla pirolisi catalitica di diversi rifiuti plastici utilizzando il catalizzatore AA-NZ, ha mostrato più picchi rispetto ai campioni provenienti dai catalizzatori TA-NZ. Questi picchi extra corrispondevano a composti aromatici, alcani e alcheni. Ciò indica che, come previsto, l’AA-NZ aveva migliori proprietà catalitiche rispetto al TA-NZ. Diversi ricercatori hanno riportato risultati simili, che l’olio liquido prodotto da PS era dominante con aromatici. Tekin et al. (2012) e Panda e Singh (2013) hanno anche riportato la presenza di aromatici con alcuni alcani e alcheni dalla pirolisi catalitica di PP. Kunwar et al. (2016) hanno effettuato la pirolisi termica e catalitica del PE e hanno riportato che l’olio liquido prodotto conteneva alcani e alcheni come gruppo funzionale principale. Nel complesso, l’analisi FT-IR ha fornito maggiori informazioni sulla composizione chimica dell’olio liquido prodotto, dalla pirolisi catalitica di diversi rifiuti plastici, utilizzando catalizzatori NZ modificati e ha ulteriormente confermato i nostri risultati GC-MS.

Figura 6. Analisi FT-IR dell’olio liquido prodotto dalla pirolisi catalitica con TA-NZ.

Figura 7. Analisi FT-IR dell’olio liquido prodotto dalla pirolisi catalitica con AA-NZ.
Applicazioni potenziali dei prodotti di pirolisi
L’olio liquido prodotto dalla pirolisi catalitica di diversi tipi di materie prime plastiche ha un alto numero di composti aromatici, olefine e naftalene che si trovano nei prodotti petroliferi. Inoltre, l’HHV dell’olio liquido prodotto è stato trovato nell’intervallo di 41,7-44,2 MJ/kg (Tabella 2) che è molto vicino al valore energetico del diesel convenzionale. Il più basso HHV di 41,7 MJ/kg è stato trovato nell’olio liquido ottenuto da PS usando il catalizzatore TA-NZ, mentre il più alto HHV di 44,2 MJ/kg era da PS/PE/PP usando il catalizzatore AA-NZ. Quindi, l’olio liquido di pirolisi prodotto da vari rifiuti plastici ha il potenziale per essere utilizzato come fonte alternativa di energia. Secondo Lee et al. (2015) e Rehan et al. (2016), la produzione di elettricità è ottenibile utilizzando l’olio liquido di pirolisi in un motore diesel. Saptoadi e Pratama (2015) hanno utilizzato con successo l’olio liquido pirolitico come alternativa in una stufa a cherosene. Inoltre, i composti aromatici prodotti possono essere utilizzati come materia prima per la polimerizzazione in varie industrie chimiche (Sarker e Rashid, 2013; Shah e Jan, 2015). Inoltre, vari ricercatori hanno utilizzato l’olio liquido prodotto come carburante per il trasporto dopo la miscelazione con il diesel convenzionale a diversi rapporti. Gli studi sono stati condotti per esplorare il potenziale dell’olio liquido prodotto nel contesto delle prestazioni del motore e delle emissioni di scarico del veicolo. Nileshkumar et al. (2015) e Lee et al. (2015) hanno riferito che il rapporto di miscelazione 20:80% di olio liquido pirolitico e diesel convenzionale, rispettivamente, ha dato risultati di prestazioni del motore simili al diesel convenzionale. Inoltre, allo stesso rapporto di miscelazione anche le emissioni di scarico erano simili, tuttavia le emissioni di scarico aumentavano con l’aumento della quantità di olio pirolitico miscelato (Frigo et al., 2014; Mukherjee e Thamotharan, 2014).
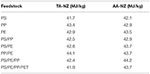
Tabella 2. Alti valori di riscaldamento (HHV) dell’olio di pirolisi da varie materie prime utilizzando catalizzatori TA-NZ e AA-NZ.
Il residuo (char) lasciato dopo il processo di pirolisi può essere utilizzato per diverse applicazioni ambientali. Diversi ricercatori hanno attivato il char tramite vapore e attivazione termica (Lopez et al., 2009; Heras et al., 2014). Il processo di attivazione ha aumentato l’area superficiale BET e ridotto la dimensione dei pori del carbone (Lopez et al., 2009). Inoltre, Bernando (2011) ha aggiornato il carbone di plastica con biomateriale e ha effettuato l’adsorbimento (3,6-22,2 mg/g) del colorante blu di metilene dalle acque reflue. Miandad et al. (2018) hanno usato il carbone ottenuto dalla pirolisi dei rifiuti plastici PS per sintetizzare un nuovo nano-adsorbente a doppio strato di ossidi di carbonio-metallo (C/MnCuAl-LDOs) per l’adsorbimento del rosso Congo (CR) nelle acque reflue. Inoltre, il carbone può essere usato come materia prima per la produzione di carbone attivo.
Limitazioni dell’analisi GC-MS dell’olio di pirolisi
Ci sono alcune limitazioni nel condurre l’analisi quantitativa accurata dei componenti chimici nell’olio di pirolisi usando GC-MS. In questo studio, abbiamo usato la percentuale di massa delle diverse sostanze chimiche trovate nei campioni di olio, calcolata in base alle aree dei picchi identificati da una colonna DP5-MS a fase normale e dal FID. I picchi identificati sono stati abbinati alla libreria di spettri del NIST e della banca di massa. I composti sono stati scelti in base all’indice di somiglianza (SI > 90%). Un ulteriore confronto con standard noti (CRM) ha permesso di confermare i composti identificati. La colonna e i rivelatori utilizzati erano limitati solo agli idrocarburi. In realtà, però, l’olio della maggior parte dei rifiuti plastici ha una struttura chimica complessa e può contenere altri gruppi di sostanze chimiche non identificate come zolfo, azoto e idrocarburi contenenti ossigeno. Questo è il motivo per cui è necessaria un’analisi chimica qualitativa più approfondita e accurata per comprendere appieno la chimica dell’olio di pirolisi, utilizzando una calibrazione e standardizzazione avanzata e utilizzando diversi rivelatori MS come SCD e NCD, nonché diverse colonne GC.
Il potenziale e le sfide delle bioraffinerie basate sulla pirolisi
Le bioraffinerie dei rifiuti stanno attirando un’enorme attenzione come soluzione per convertire i rifiuti urbani e altri rifiuti da biomassa in una serie di prodotti come combustibili, energia, calore e altri prodotti chimici e materiali di valore. Diversi tipi di bioraffinerie, come una bioraffineria basata sull’agricoltura, una bioraffineria di rifiuti animali, una bioraffineria di acque reflue, una bioraffineria basata sulle alghe, una raffineria di rifiuti plastici, una bioraffineria basata sulla silvicoltura, una bioraffineria di rifiuti industriali e una bioraffineria di rifiuti alimentari ecc. possono essere sviluppate a seconda del tipo e della fonte dei rifiuti (Gebreslassie et al., 2013; De Wild et al., 2014; Nizami et al., 2017a,b; Waqas et al., 2018). Queste bioraffinerie possono svolgere un ruolo significativo per ridurre l’inquinamento ambientale legato ai rifiuti e le emissioni di gas serra. Inoltre, generano benefici economici sostanziali e possono aiutare a raggiungere un’economia circolare in qualsiasi paese.
Una bioraffineria basata sulla pirolisi può essere sviluppata per trattare una gamma di rifiuti da biomassa e rifiuti plastici per produrre combustibili liquidi e gassosi, energia, biochar e altri prodotti chimici di valore superiore utilizzando un approccio integrato. L’approccio integrato aiuta a raggiungere i massimi benefici economici e ambientali con una produzione minima di rifiuti. Ci sono molte sfide e margini di miglioramento nelle bioraffinerie basate sulla pirolisi, che devono essere affrontate e ottimizzate per assicurare i massimi benefici. Anche se l’olio di pirolisi contiene più energia del carbone e di alcuni altri combustibili, la pirolisi stessa è un processo ad alta intensità energetica, e il prodotto petrolifero richiede più energia per essere raffinato (Inman, 2012). Questo significa che l’olio di pirolisi potrebbe non essere molto meglio del diesel convenzionale o di altri combustibili fossili in termini di emissioni di gas serra, anche se sono necessari studi di ricerca molto dettagliati sul bilancio di massa e di energia attraverso i confini dell’intero processo per confermarlo. Per superare questi requisiti energetici di processo, possono essere sviluppate tecnologie più avanzate usando l’integrazione di energie rinnovabili come quella solare o idroelettrica con le bioraffinerie basate sulla pirolisi, per ottenere i massimi benefici economici e ambientali.
La disponibilità di flussi di rifiuti di plastica e biomassa come materie prime per le bioraffinerie basate sulla pirolisi, è un’altra grande sfida, poiché il riciclaggio non è attualmente molto efficiente, specialmente nei paesi in via di sviluppo. I gas prodotti dalla pirolisi di alcuni rifiuti plastici come il PVC sono tossici, e quindi la tecnologia di trattamento delle emissioni della pirolisi deve essere ulteriormente raffinata per ottenere i massimi benefici ambientali. L’olio di pirolisi ottenuto da vari tipi di plastica deve essere pulito in modo significativo prima di essere usato in qualsiasi applicazione, per garantire un impatto ambientale minimo. L’alto contenuto aromatico dell’olio di pirolisi è buono e alcuni composti aromatici come benzene, toluene e stirene possono essere raffinati e venduti in un mercato già stabilito. Tuttavia, alcuni degli idrocarburi aromatici sono noti cancerogeni e possono causare gravi danni alla salute umana e all’ambiente. È quindi necessaria una seria considerazione a questo proposito.
Altri aspetti per l’ottimizzazione delle bioraffinerie basate sulla pirolisi, come i nuovi catalizzatori avanzati emergenti compresi i nano-catalizzatori, devono essere sviluppati e applicati nei processi di pirolisi per aumentare la qualità e la resa dei prodotti, e per ottimizzare il processo complessivo. Il mercato per i prodotti di bioraffinazione basati sulla pirolisi dovrebbe essere creato/espanso per attrarre ulteriore interesse e finanziamenti, al fine di rendere questo concetto più pratico e di successo. Allo stesso modo, è necessaria una maggiore attenzione per condurre ulteriori ricerche e lavori di sviluppo per arricchire il concetto di bioraffineria e per sfruttare il suo vero potenziale. Inoltre, è vitale condurre una valutazione dettagliata dell’impatto economico e ambientale delle bioraffinerie durante la fase di progettazione, usando strumenti specializzati come la valutazione del ciclo di vita (LCA). La LCA può analizzare l’impatto ambientale della bioraffineria e di tutti i prodotti conducendo bilanci dettagliati dell’energia e dei materiali di tutte le fasi della vita, compresa l’estrazione e la lavorazione delle materie prime, la produzione, la distribuzione del prodotto, l’uso, la manutenzione e lo smaltimento/riciclaggio. I risultati della LCA aiuteranno a determinare la sostenibilità delle bioraffinerie, che è fondamentale per prendere la decisione giusta.
Conclusioni
La pirolisi catalitica è una tecnica promettente per convertire i rifiuti plastici in olio liquido e altri prodotti a valore aggiunto, usando un catalizzatore di zeolite naturale (NZ) modificato. La modifica dei catalizzatori NZ è stata effettuata tramite una nuova attivazione termica (TA) e acida (AA) che ha migliorato le loro proprietà catalitiche. La pirolisi catalitica di PS ha prodotto il più alto olio liquido (70 e 60%) rispetto a PP (40 e 54%) e PE (40 e 42%), usando i catalizzatori TA-NZ e AA-NZ, rispettivamente. La composizione chimica dell’olio di pirolisi è stata analizzata usando GC-MS, ed è stato trovato che la maggior parte dell’olio liquido ha prodotto un alto contenuto aromatico con alcuni composti alifatici e altri idrocarburi. Questi risultati sono stati ulteriormente confermati dall’analisi FT-IR che mostrava chiari picchi corrispondenti a gruppi funzionali aromatici e altri idrocarburi. Inoltre, l’olio liquido prodotto da diversi tipi di rifiuti plastici aveva valori di riscaldamento più alti (HHV) nell’intervallo di 41,7-44,2 MJ/kg simili a quelli del diesel convenzionale. Pertanto, ha il potenziale per essere usato in varie applicazioni di energia e trasporto dopo un ulteriore trattamento e raffinazione. Questo studio è un passo verso lo sviluppo di bioraffinerie basate sulla pirolisi. Le bioraffinerie hanno un grande potenziale per convertire i rifiuti in energia e altri prodotti di valore e potrebbero aiutare a realizzare economie circolari. Tuttavia, ci sono molte sfide tecniche, operative e socio-economiche, come discusso sopra, che devono essere superate per raggiungere i massimi benefici economici e ambientali delle bioraffinerie.
Data Availability
Tutti i set di dati generati per questo studio sono inclusi nel manoscritto e/o nei file supplementari.
Author Contributions
RM ha eseguito gli esperimenti di pirolisi e ha aiutato nella scrittura del manoscritto. HK, JD, JG e AH hanno effettuato la caratterizzazione dettagliata dei prodotti del processo. MR e ASA hanno analizzato i dati e scritto parti del manoscritto. MAB, MR e A-SN hanno corretto e modificato il manoscritto. ASA e IMII hanno sostenuto il progetto finanziariamente e tecnicamente.
Dichiarazione di conflitto di interessi
Gli autori dichiarano che la ricerca è stata condotta in assenza di relazioni commerciali o finanziarie che potrebbero essere interpretate come un potenziale conflitto di interessi.
Riconoscimenti
MR e A-SN ringraziano il Center of Excellence in Environmental Studies (CEES), King Abdulaziz University (KAU), Jeddah, KSA e il Ministero dell’Educazione, KSA per il supporto finanziario sotto il Grant No. 2/S/1438. Gli autori sono anche grati a Deanship of Scientific Research (DSR) a KAU per il loro sostegno finanziario e tecnico a CEES.
Adnan, A., Shah, J., e Jan, M. R. (2014). Studi di degradazione del polistirene utilizzando catalizzatori supportati da Cu. J. Anal. Appl. Pyrol. 109, 196-204. doi: 10.1016/j.jaap.2014.06.013
CrossRef Full Text | Google Scholar
Aguado, J., Sotelo, J. L., Serrano, D. P., Calles, J. A., e Escola, J. M. (1997). Conversione catalitica di poliolefine in combustibili liquidi su MCM-41: confronto con ZSM-5 e SiO2-Al2O3 amorfo. Ener fuels 11, 1225-1231. doi: 10.1021/ef970055v
CrossRef Full Text | Google Scholar
Alexandra, L. C. (2012). Rifiuti solidi urbani: Trasformare un problema in risorsa-rifiuto: Le sfide per i paesi in via di sviluppo, Urban Specialist. Banca Mondiale. 2-4 p.
Batool, M., Shah, A. T., Imran Din, M., e Li, B. (2016). Pirolisi catalitica di polietilene a bassa densità utilizzando unità di keggin monovacant incapsulati cetyltrimethyl ammonium e ZSM-5. J. Chem. 2016:2857162. doi: 10.1155/2016/2857162
CrossRef Full Text | Google Scholar
Bernando, M. (2011). “Caratterizzazione fisico-chimica dei catrami prodotti nella copirrolisi dei rifiuti e possibili percorsi di valorizzazione”, in Chemical Engineering (Lisboa: Universidade Nova de Lisboa), 27-36.
Bhaskar, T., Kaneko, J., Muto, A., Sakata, Y., Jakab, E., Matsui, T., et al. (2004). Studi di pirolisi delle plastiche PP/PE/PS/PVC/HIPS-Br mescolate con PET e dealogenazione (Br, Cl) dei prodotti liquidi. J. Anal. Appl. Pyrolysis 72, 27-33. doi: 10.1016/j.jaap.2004.01.005
CrossRef Full Text | Google Scholar
Chandrasekaran, S. R., Kunwar, B., Moser, B. R., Rajagopalan, N., e Sharma, B. K. (2015). Cracking termico catalitico di plastica postconsumo rifiuti a combustibili. 1. Cinetica e ottimizzazione. Energy Fuels 29, 6068-6077. doi: 10.1021/acs.energyfuels.5b01083
CrossRef Full Text | Google Scholar
Cullis, C. F., e Hirschler, M. M. (1981). La combustione dei polimeri organici. Vol. 5. Londra: Oxford University Press.
Dawood, A., and Miura, K. (2002). Pirolisi catalitica di polipropilene (PP) irradiato con c su HY-zeolite per migliorare la reattività e la selettività del prodotto. Polym. Degrad. Stab. 76, 45-52. doi: 10.1016/S0141-3910(01)00264-6
CrossRef Full Text | Google Scholar
De Wild, P. J., Huijgen, W. J., and Gosselink, R. J. (2014). Pirolisi della lignina per bioraffinerie lignocellulosiche redditizie. Biocarburanti Bioprod. Biorefining 8, 645-657. doi: 10.1002/bbb.1474
CrossRef Full Text | Google Scholar
Demirbas, A. (2004). Pirolisi di rifiuti plastici municipali per il recupero di idrocarburi a benzina. J. Anal. Appl. Pyrolysis 72, 97-102. doi: 10.1016/j.jaap.2004.03.001
CrossRef Full Text | Google Scholar
Dimitrov, N., Krehula, L. K., Siročić, A. P., and Hrnjak-Murgić, Z. (2013). Analisi dei prodotti di bottiglie in PET riciclate mediante pirolisi-gas cromatografia. Polym. Degrad. Stab. 98, 972-979. doi: 10.1016/j.polymdegradstab.2013.02.013
CrossRef Full Text | Google Scholar
Dziecioł, M., and Trzeszczynski, J. (2000). Prodotti volatili della degradazione termica del poli (etilene tereftalato) in atmosfera di azoto. J. Appl. Polym. Sci. 77, 1894-1901. doi: 10.1002/1097-4628(20000829)77:9<1894::AID-APP5>3.0.CO;2-Y
CrossRef Full Text | Google Scholar
Frigo, S., Seggiani, M., Puccini, M., e Vitolo, S. (2014). Produzione di combustibile liquido dalla pirolisi dei pneumatici usati e il suo utilizzo in un motore Diesel. Fuel 116, 399-408. doi: 10.1016/j.fuel.2013.08.044
CrossRef Full Text | Google Scholar
Gaca, P., Drzewiecka, M., Kaleta, W., Kozubek, H., e Nowinska, K. (2008). Degradazione catalitica di polietilene su setaccio molecolare mesoporoso MCM-41 modificato con composti eteropolici. Polish J. Environ. Stud. 17, 25-35.
Google Scholar
Gandidi, I. M., Susila, M. D., Mustofa, A., and Pambudi, N. A. (2018). Cracking termico-catalitico di rifiuti solidi urbani reali in Bio-Crude Oil. J. Energy Inst. 91, 304-310. doi: 10.1016/j.joei.2016.11.005
CrossRef Full Text | Google Scholar
Gebreslassie, B. H., Slivinsky, M., Wang, B., and You, F. (2013). Ottimizzazione del ciclo di vita per la progettazione sostenibile e le operazioni di bioraffineria di idrocarburi tramite pirolisi veloce, hydrotreating e hydrocracking. Comput. Chem. Eng. 50, 71-91. doi: 10.1016/j.compchemeng.2012.10.013
CrossRef Full Text | Google Scholar
Heras, F., Jimenez-Cordero, D., Gilarranz, M. A., Alonso-Morales, N., and Rodriguez, J. J. (2014). Attivazione del carbone di pneumatici di scarto mediante ossidazione ciclica in fase liquida. Processo combustibile. Technol. 127, 157-162. doi: 10.1016/j.fuproc.2014.06.018
CrossRef Full Text | Google Scholar
Inman, M. (2012). Cucinare il carburante. Nat. Clim. Change 2, 218-220. doi: 10.1038/nclimate1466
CrossRef Full Text | Google Scholar
Jung, S. H., Cho, M. H., Kang, B. S., e Kim, J. S. (2010). Pirolisi di una frazione di rifiuti di polipropilene e polietilene per il recupero di aromatici BTX utilizzando un reattore a letto fluido. Processo del combustibile. Technol. 91, 277-284. doi: 10.1016/j.fuproc.2009.10.009
CrossRef Full Text | Google Scholar
Kim, H. S., Kim, S., Kim, H. J., and Yang, H. S. (2006). Proprietà termiche dei compositi poliolefinici riempiti di farina biologica con diversi tipi e contenuti di agenti compatibilizzanti. Thermochim. Acta 451, 181-188. doi: 10.1016/j.tca.2006.09.013
CrossRef Full Text | Google Scholar
Kim, J. R., Yoon, J. H., and Park, D. W. (2002). Riciclaggio catalitico della miscela di polipropilene e polistirene. Polym. Degrad. Stab. 76, 61-67. doi: 10.1016/S0141-3910(01)00266-X
CrossRef Full Text | Google Scholar
Kiran, N., Ekinci, E., and Snape, C. E. (2000). Riciclaggio di rifiuti plastici tramite pirolisi. Resour. Conserv. Recycl. 29, 273-283. doi: 10.1016/S0921-3449(00)00052-5
CrossRef Full Text | Google Scholar
Kunwar, B., Moser, B. R., Chandrasekaran, S. R., Rajagopalan, N., and Sharma, B. K. (2016). Depolimerizzazione catalitica e termica della plastica di polietilene ad alta densità post-consumo di basso valore. Energia 111, 884-892. doi: 10.1016/j.energy.2016.06.024
CrossRef Full Text | Google Scholar
Lecomte, H. A., e Liggat, J. J. (2006). Meccanismo di degradazione delle unità di dietilenglicole in un polimero tereftalato. Polym. Degrad. Stab. 91, 681-689. doi: 10.1016/j.polymdegradstab.2005.05.028
CrossRef Full Text | Google Scholar
Lee, K. H. (2012). Effetti dei tipi di zeoliti sulla valorizzazione catalitica dell’olio di cera da pirolisi. J. Anal. Appl. Pyrol. 94, 209-214. doi: 10.1016/j.jaap.2011.12.015
CrossRef Full Text | Google Scholar
Lee, S., Yoshida, K., e Yoshikawa, K. (2015). Applicazione di olio di pirolisi di plastica dei rifiuti in un motore diesel a iniezione diretta: Per una piccola scala di elettrificazione non di rete. Energia Environ. Res. 5:18. doi: 10.5539/eer.v5n1p18
CrossRef Full Text
Lee, S. Y., Yoon, J. H., Kim, J. R., e Park, D. W. (2001). Degradazione catalitica del polistirene su zeolite naturale clinoptilolite. Polym. Degrad. Stab. 74, 297-305. doi: 10.1016/S0141-3910(01)00162-8
CrossRef Full Text | Google Scholar
Lin, Y. H., Yang, M. H., Yeh, T. F., and Ger, M. D. (2004). Degradazione catalitica del polietilene ad alta densità su catalizzatori mesoporosi e microporosi in un reattore a letto fluido. Polym. Degrad. Stab. 86, 121-128. doi: 10.1016/j.polymdegradstab.2004.02.015
CrossRef Full Text | Google Scholar
Lopez, A., Marco d, I., Caballero, B. M., Laresgoiti, M. F., Adrados, A., and Torres, A. (2011). Pirolisi dei rifiuti plastici urbani II: influenza della composizione della materia prima in condizioni catalitiche. Rifiuti Manag. 31, 1973-1983. doi: 10.1016/j.wasman.2011.05.021
CrossRef Full Text | Google Scholar
Lopez, G., Olazar, M., Artetxe, M., Amutio, M., Elordi, G., e Bilbao, J. (2009). Attivazione a vapore del carbone pirolitico di pneumatici a diverse temperature. J. Anal. Appl. Pyrol. 85, 539-543. doi: 10.1016/j.jaap.2008.11.002
CrossRef Full Text | Google Scholar
Ma, C., Yu, J., Wang, B., Song, Z., Xiang, J., Hu, S., et al. (2017). Pirolisi catalitica di polistirene ad alto impatto ritardato dalla fiamma su vari catalizzatori acidi solidi. Processo del combustibile. Technol. 155, 32-41. doi: 10.1016/j.fuproc.2016.01.018
CrossRef Full Text | Google Scholar
Marcilla, A., Beltrán, M. I., Hernández, F., and Navarro, R. (2004). Disattivazione HZSM5 e HUSY durante la pirolisi catalitica del polietilene. Appl. Catal. A Gen. 278, 37-43. doi: 10.1016/j.apcata.2004.09.023
CrossRef Full Text | Google Scholar
McNeill, I. C., and Bounekhel, M. (1991). Studi di degradazione termica dei poliesteri tereftalati: 1. Poli (alchilene tereftalati). Polimero Degrad. Stab. 34, 187-204. doi: 10.1016/0141-3910(91)90119-C
CrossRef Full Text | Google Scholar
McNeill, I. C., Zulfiqar, M., e Kousar, T. (1990). Un’indagine dettagliata dei prodotti della degradazione termica del polistirene. Polym. Degrad. Stab. 28, 131-151. doi: 10.1016/0141-3910(90)90002-O
CrossRef Full Text | Google Scholar
Miandad, R., Barakat, M. A., Aburiazaiza, A. S., Rehan, M., Ismail, I. M. I., e Nizami, A. S. (2017b). Effetto dei tipi di rifiuti plastici sull’olio liquido di pirolisi. Int. Biodeterior. Biodegrad. 119, 239-252. doi: 10.1016/j.ibiod.2016.09.017
CrossRef Full Text | Google Scholar
Miandad, R., Barakat, M. A., Aburiazaiza, A. S., Rehan, M., e Nizami, A. S. (2016a). Pirolisi catalitica dei rifiuti plastici: una recensione. Sicurezza di processo Environ. Protect. 102, 822-838. doi: 10.1016/j.psep.2016.06.022
CrossRef Full Text | Google Scholar
Miandad, R., Barakat, M. A., Rehan, M., Aburiazaiza, A. S., Ismail, I. M. I., e Nizami, A. S. (2017a). Rifiuti plastici a olio liquido attraverso la pirolisi catalitica utilizzando catalizzatori di zeoliti naturali e sintetici. Rifiuti Manag. 69, 66-78. doi: 10.1016/j.wasman.2017.08.032
PubMed Abstract | CrossRef Full Text | Google Scholar
Miandad, R., Kumar, R., Barakat, M. A., Basheer, C., Aburiazaiza, A. S., Nizami, A. S., et al. (2018). Conversione non sfruttata del carbone di rifiuti plastici in LDO carbonio-metallo per l’adsorbimento del rosso Congo. J Colloid Interface Sci. 511, 402-410. doi: 10.1016/j.jcis.2017.10.029
PubMed Abstract | CrossRef Full Text | Google Scholar
Miandad, R., Nizami, A. S., Rehan, M., Barakat, M. A., Khan, M. I., Mustafa, A., et al. (2016b). Influenza della temperatura e del tempo di reazione sulla conversione dei rifiuti di polistirolo in olio liquido di pirolisi. Rifiuti Manag. 58, 250-259. doi: 10.1016/j.wasman.2016.09.023
PubMed Abstract | CrossRef Full Text | Google Scholar
Miandad, R., Rehan, M., Nizami, A. S., Barakat, M. A. E. F., e Ismail, I. M. (2016c). “The energy and value- added products from pyrolysis of waste plastics,” in Recycling of Solid Waste for Biofuels and Bio- Chemicals, eds O. P. Karthikeyan, K. H. Subramanian, and S. Muthu (Singapore: Springer), 333-355.
Google Scholar
Miskolczi, N., Bartha, L., and Deak, G. (2006). Degradazione termica di polietilene e polistirene dall’industria dell’imballaggio su diversi catalizzatori in materie prime simili al carburante. Polym. Degrad. Stab. 91, 517-526. doi: 10.1016/j.polymdegradstab.2005.01.056
CrossRef Full Text | Google Scholar
Mukherjee, M. K., e Thamotharan, P. C. (2014). Prestazioni e test delle emissioni di diverse miscele di olio di plastica di scarto con diesel ed etanolo su motore diesel bicilindrico a quattro tempi. IOSR J. Mech. Civil Eng. 11, 2278-1684. doi: 10.9790/1684-11214751
CrossRef Full Text
Nileshkumar, K. D., Jani, R. J., Patel, T. M., e Rathod, G. P. (2015). Effetto del rapporto di miscela di olio di pirolisi plastica e carburante diesel sulle prestazioni del motore CI monocilindrico. Int. J. Sci. Technol. Eng. 1, 2349-2784.
Google Scholar
Nizami, A. S., Ouda, O. K. M., Rehan, M., El-Maghraby, A. M. O., Gardy, J., Hassanpour, A., et al. (2016). Il potenziale delle zeoliti naturali dell’Arabia Saudita nelle tecnologie di recupero energetico. Energy 108, 162-171. doi: 10.1016/j.energy.2015.07.030
CrossRef Full Text | Google Scholar
Nizami, A. S., Rehan, M., Waqas, M., Naqvi, M., Ouda, O. K. M., Shahzad, K., et al. (2017a). Bioraffinerie di rifiuti: abilitare le economie circolari nei paesi in via di sviluppo. Bioresour. Technol. 241, 1101-1117. doi: 10.1016/j.biortech.2017.05.097
PubMed Abstract | CrossRef Full Text | Google Scholar
Nizami, A. S., Shahzad, K., Rehan, M., Ouda, O. K. M., Khan, M. Z., Ismail, I. M. I., et al. (2017b). Sviluppare la bioraffineria dei rifiuti a Makkah: un modo per convertire i rifiuti urbani in energia rinnovabile. Appl. Energia. 186, 189-196. doi: 10.1016/j.apenergy.2016.04.116
CrossRef Full Text | Google Scholar
Obali, Z., Sezgi, N. A., e Doğu, T. (2012). Degradazione catalitica di polipropilene su catalizzatori mesoporosi caricati con allumina. Chimica. Eng. J. 207, 421-425. doi: 10.1016/j.cej.2012.06.146
CrossRef Full Text | Google Scholar
Ogawa, T., Kuroki, T., Ide, S., e Ikemura, T. (1982). Recupero di derivati indan da rifiuti di polistirolo. J. Appl. Polym. Sci. 27, 857-869. doi: 10.1002/app.1982.070270306
CrossRef Full Text | Google Scholar
Panda, A. K., e Singh, R. K. (2013). Ottimizzazione sperimentale del processo per la degradazione termocatalitica dei rifiuti di polipropilene a combustibile liquido. Adv. Energy Eng. 1, 74-84.
Google Scholar
Peterson, J. D., Vyazovkin, S., and Wight, C. A. (2001). Cinetica della degradazione termica e termo-ossidativa di polistirene, polietilene e poli (propilene). Macromol. Chem. Phys. 202, 775-784. doi: 10.1002/1521-3935(20010301)202:6<775::AID-MACP775>3.0.CO;2-G
CrossRef Full Text | Google Scholar
Ramli, M. R., Othman, M. B. H., Arifin, A., and Ahmad, Z. (2011). Rete di reticolazione di polidimetilsilossano tramite meccanismi di aggiunta e condensazione (RTV). Parte I: sintesi e proprietà termiche. Polym. Degrad. Stab. 96, 2064-2070. doi: 10.1016/j.polymdegradstab.2011.10.001
CrossRef Full Text | Google Scholar
Ratnasari, D. K., Nahil, M. A., and Williams, P. T. (2017). Pirolisi catalitica dei rifiuti di plastica utilizzando la catalisi a stadi per la produzione di oli idrocarburici gamma benzina. J. Anal. Appl. Pyrolysis 124, 631-637. doi: 10.1016/j.jaap.2016.12.027
CrossRef Full Text | Google Scholar
Rehan, M., Miandad, R., Barakat, M. A., Ismail, I. M. I., Almeelbi, T., Gardy, J., et al. (2017). Effetto dei catalizzatori di zeolite sull’olio liquido di pirolisi. Int. Biodeterior. Biodegrad. 119, 162-175. doi: 10.1016/j.ibiod.2016.11.015
CrossRef Full Text | Google Scholar
Rehan, M., Nizami, A. S., Shahzad, K., Ouda, O. K. M., Ismail, I. M. I., Almeelbi, T., et al. (2016). Combustibile liquido pirolitico: una fonte di energia rinnovabile a Makkah. Energy Sources A 38, 2598-2603. doi: 10.1080/15567036.2016.1153753
CrossRef Full Text | Google Scholar
Rizzarelli, P., Rapisarda, M., Perna, S., Mirabella, E. F., La Carta, S., Puglisi, C., et al. (2016). Determinazione del polietilene in miscele di polimeri biodegradabili e in sacchetti di trasporto compostabili mediante Py-GC/MS e TGA. J. Anal. Appl. Pirolisi 117,72-81. doi: 10.1016/j.jaap.2015.12.014
CrossRef Full Text | Google Scholar
Saptoadi, H., e Pratama, N. N. (2015). Utilizzo di olio di scarto della plastica come parziale sostituto del cherosene in fornelli pressurizzati. Int. J. Environ. Sci. Dev. 6, 363-368. doi: 10.7763/IJESD.2015.V6.619
CrossRef Full Text | Google Scholar
Sarker, M., e Rashid, M. M. (2013). Miscela di rifiuti plastici di polistirolo e polipropilene in combustibile di grado leggero utilizzando il catalizzatore Fe2O3. Int. J. Renew. Energy Technol. Res. 2, 17-28.
Google Scholar
Seo, Y. H., Lee, K. H., and Shin, D. H. (2003). Indagine sulla degradazione catalitica del polietilene ad alta densità mediante analisi del tipo di gruppo idrocarburo. J. Anal. Appl. Pyrol. 70, 383-398. doi: 10.1016/S0165-2370(02)00186-9
CrossRef Full Text | Google Scholar
Serrano, D. P., Aguado, J., and Escola, J. M. (2000). Conversione catalitica di polistirene su HMCM-41, HZSM-5 e amorfo SiO2-Al2O3: confronto con cracking termico. Appl. Catal. B:Environ. 25, 181-189. doi: 10.1016/S0926-3373(99)00130-7
CrossRef Full Text | Google Scholar
Serrano, D. P., Aguado, J., e Escola, J. M. (2012). Sviluppare catalizzatori avanzati per la conversione di rifiuti plastici poliolefinici in combustibili e prodotti chimici. ACS Catal. 2, 1924-1941. doi: 10.1021/cs3003403
CrossRef Full Text | Google Scholar
Shah, J., e Jan, M. R. (2015). Effetto del polietilene tereftalato sulla pirolisi catalitica del polistirene: Indagine dei prodotti liquidi. J. Taiwan Inst. Chem. Eng. 51, 96-102. doi: 10.1016/j.jtice.2015.01.015
CrossRef Full Text | Google Scholar
Siddiqui, M. N., and Redhwi, H. H. (2009). Pirolisi di plastiche miste per il recupero di prodotti utili. Processo combustibile. Technol. 90, 545-552. doi: 10.1016/j.fuproc.2009.01.003
CrossRef Full Text | Google Scholar
Sriningsih, W., Saerodji, M. G., Trisunaryanti, W., Armunanto, R., and Falah, I. I. (2014). Produzione di carburante da rifiuti di plastica LDPE su zeolite naturale supportato Ni, Ni-Mo, Co e Co-Mo metalli. Proc. Environ. Sci. 20, 215-224. doi: 10.1016/j.proenv.2014.03.028
CrossRef Full Text | Google Scholar
Syamsiro, M., Cheng, S., Hu, W., Saptoadi, H., Pratama, N. N., Trisunaryanti, W., et al. (2014). Combustibile liquido e gassoso da rifiuti di plastica mediante processi sequenziali di pirolisi e reforming catalitico su catalizzatori indonesiani di zeolite naturale. Rifiuti Technol. 2, 44-51. doi: 10.12777/wastech.2.2.44-51
CrossRef Full Text | Google Scholar
Tekin, K., Akalin, M. K., Kadi, C., e Karagöz, S. (2012). Degradazione catalitica del polipropilene di scarto mediante pirolisi. J. Energy Ins. 85, 150-155. doi: 10.1179/1743967112Z.00000000029
CrossRef Full Text | Google Scholar
Thilakaratne, R., Tessonnier, J. P., e Brown, R. C. (2016). Conversione di metossi e idrossile funzionalità di monomeri fenolici su zeoliti. Chimica verde. 18, 2231-2239. doi: 10.1039/c5gc02548f
CrossRef Full Text | Google Scholar
Uemichi, Y., Hattori, M., Itoh, T., Nakamura, J., e Sugioka, M. (1998). Comportamenti di disattivazione dei catalizzatori di zeolite e silice-allumina nella degradazione del polietilene. Ind. Eng. Chem. Res. 37, 867-872. doi: 10.1021/ie970605c
CrossRef Full Text | Google Scholar
Uemichi, Y., Nakamura, J., Itoh, T., Sugioka, M., Garforth, A. A., and Dwyer, J. (1999). Conversione di polietilene in carburanti a benzina mediante degradazione catalitica a due stadi usando Silica-Alumina e Zeolite HZSM-5. Ind. Eng. Chem. Res. 38, 385-390. doi: 10.1021/ie980341+
CrossRef Full Text | Google Scholar
Ukei, H., Hirose, T., Horikawa, S., Takai, Y., Taka, M., Azuma, N., et al. Degradazione catalitica del polistirene in stirene e un progetto di polistirene riciclabile con catalizzatori dispersi. Catal. Today 62, 67-75. doi: 10.1016/S0920-5861(00)00409-0
CrossRef Full Text | Google Scholar
Waqas, M., Rehan, M., Aburiazaiza, A. S., and Nizami, A. S. (2018). “Chapter 17-Wastewater Biorefinery based on the microbial electrolysis cell: opportunities and challenges,” in Progress and Recent Trends in Microbial Fuel Cells, eds K. Dutta and P. Kundu (New York, NY: Elsevier Inc.), 347-374. doi: 10.1016/B978-0-444-64017-8.00017-8
CrossRef Full Text
Williams, P. T. (2006). “Rendimento e composizione dei gas e degli oli/cere dal riciclo a materia prima dei rifiuti di plastica”. In Feeds Tock Recycling and Pyrolysis of Waste Plastics: Converting Waste Plastics into Diesel and Other Fuels, eds J. Scheirs and W. Kaminsky (West Sussex: John Wiley & Sons Press), 285-309.
Google Scholar
Wu, C., and Williams, P. T. (2010). Pirolisi-gassificazione di plastica, plastica mista e rifiuti plastici del mondo reale con e senza catalizzatore Ni-Mg-Al. Fuel 89, 3022-3032. doi: 10.1016/j.fuel.2010.05.032
CrossRef Full Text | Google Scholar
Wu, J., Chen, T., Luo, X., Han, D., Wang, Z., e Wu, J. (2014). Analisi TG/FTIR sul comportamento di coprolisi di PE, PVC e PS. Rifiuti Manag. 34, 676-682. doi: 10.1016/j.wasman.2013.12.005
PubMed Abstract | CrossRef Full Text | Google Scholar
Xue, Y., Johnston, P., e Bai, X. (2017). Effetto della modalità di contatto del catalizzatore e dell’atmosfera di gas durante la pirolisi catalitica dei rifiuti plastici. Energia Conv. Manag. 142, 441-451. doi: 10.1016/j.enconman.2017.03.071
CrossRef Full Text | Google Scholar
Yoshioka, T., Grause, G., Eger, C., Kaminsky, W., e Okuwaki, A. (2004). Pirolisi del poli (etilene tereftalato) in un impianto a letto fluido. Polym. Degrad. Stab. 86, 499-504. doi: 10.1016/j.polymdegradstab.2004.06.001
CrossRef Full Text | Google Scholar
Zeaiter, J. (2014). Uno studio di processo sulla pirolisi dei rifiuti di polietilene. Carburante 133, 276-282. doi: 10.1016/j.fuel.2014.05.028
CrossRef Full Text | Google Scholar