Introduzione
Forse il primo riferimento nella storia umana all’assorbimento di ferro e alcol risale al 1200 a.C., una leggenda della Tessaglia racconta come Apolodoro di Iphycus, stando in un campo a guardare suo padre castrare gli agnelli, fu minacciato dalla stessa punizione; quando divenne adulto, Apolodoro era impotente. Uno stregone di nome Melampus, ispirato da un avvoltoio, guarì Apolodoro facendogli bere in un bicchiere di vino la ruggine del coltello con cui suo padre castrava gli agnelli e con cui era stato minacciato.
Numerosa è la popolazione di pazienti alcolizzati visti nel nostro ospedale così come quelli che richiedono un ricovero, tenendo conto di tutte le entità morbose che lo accompagnano.
Con questa comunicazione vogliamo ricordare una delle patologie ematologiche presenti nell’alcolismo che spesso può regredire con la sola astinenza: l’anemia sideroblastica e l’emosiderosi.
Bjorkman nel 1956 descrisse quattro pazienti con anemie croniche refrattarie e anelli sideroblastici con colorazione blu di Prussia delle cellule del midollo osseo.
La prima prova che questi anelli sideroblastici fossero associati all’alcol fu proposta da Mac Gibbon e Mollin nel 1965, da quando l’alcolismo è diventato la causa più comune di questa patologia.
Nel 1969 Hines (sostituendo la i con la 1) descrisse nell’alcolismo cronico la comparsa di un’anemia sideroblastica reversibile dovuta all’astinenza.
Effetti dell’alcol
I molteplici effetti patologici dell’alcol (sostituire con 2) sul tessuto ematopoietico possono essere suddivisi in:
Quelli risultanti dall’effetto diretto dell’alcool
Quelli derivanti da effetti secondari a carenze nutrizionali
Quelli causati da malattie epatiche
L’anemia è una causa comune negli alcolisti.(sostituire con 3) Di questi i più comuni sono l’anemia megaloblastica e l’anemia sideroblastica.
Questi ultimi sarebbero legati a fattori nutrizionali e a disturbi del metabolismo della vitamina B6.
È stata dimostrata una diminuzione della capacità della piridossina di convertirsi in piridossal fosfato, la forma attiva della vitamina B6, come risultato dell’inibizione dell’attività piridossal fosfochinasi eritrocitaria.
È stato anche suggerito che l’etanolo può agire come stimolante della fosfatasi alcalina di membrana accelerando la degradazione del fosfato piridossale cellulare (sostituire con 4). Questa alterazione del metabolismo della piridossina è corroborata da una diminuzione dell’escrezione urinaria di acido piridossico 4-piridossico, che è un metabolita della piridossina, e una diminuzione del fosfato piridossale nel siero.
Il fosfato piridossale agisce anche come fattore coadiuvante nella sintesi dell’acido delta-aminolevulinico, che è uno dei precursori della frazione di emoglobina contenente ferro, cioè l’haemo.
Altri studi hanno dimostrato che l’etanolo agisce non solo direttamente ma anche attraverso il suo metabolita acetaldeide. L’acetaldeide è stata anche accreditata di aumentare la degradazione del fosfato piridossale, portando a una diminuzione del fosfato piridossale nel siero e peggiorando la formazione del fosfato piridossale nei globuli rossi umani in vitro, accelerando la degradazione dei composti fosforilati della vitamina B6.
Quando si usano metodi di colorazione del ferro (blu di Prussia e colorazione Pearls), i granuli metallici non eme contenenti ferro, presumibilmente sotto forma di emosiderina o ferritina, tendono a formare un anello intorno al nucleo degli eritroblasti. Questi sono chiamati anelli sideroblastici o sideroblasti ad anello.
La microscopia elettronica ha dimostrato che questi sideroblasti hanno i depositi di ferro a livello dei mitocondri o dei corpi citoplasmatici.
Queste anomalie morfologiche sono associate a tutte le caratteristiche dell’eritropoiesi inefficace: iperplasia eritroide, aumento dell’assorbimento del ferro da parte dei precursori eritroidi del midollo osseo, incorporazione subnormale del ferro nell’emoglobina circolante con riflusso del ferro nella circolazione, causando iperferremia, distruzione intra-maria dei normoblasti, anemia e reticolocitopenia.
La frequenza dell’anello sideroblastico nel midollo eritroide è più frequente nel paziente malato cronico e nei pazienti alcolisti malnutriti.
L’evidenza clinica e sperimentale suggerisce che un fattore nutrizionale è importante nella patogenesi dell’anemia sideroblastica nei pazienti alcolisti.
La somministrazione cronica sperimentale di alcol in volontari umani ha prodotto cambiamenti sideroblastici nel midollo osseo.
Quando l’alcol è stato somministrato con piridossina e folati bassi nella dieta, anelli di
sideroblasti sviluppati dopo diverse settimane nella maggior parte dei soggetti studiati.
Nel 1970 Hines e Cowan citano un’alterazione nella fosforilazione della piridossina a fosfato piridossale confermando così il disordine nel metabolismo della piridossina da tre linee di ricerca:
Diminuzione del fosfato piridossale e anelli sideroblastici sono stati prodotti in 2 di 3 soggetti che sono stati mantenuti su diete a basso contenuto di folati con integrazione di alcol. Hanno poi mostrato una risposta ematologica dopo la somministrazione di fosfato piridossale ma non con acido folico o piridossina terapeutica.
In seguito alla somministrazione di piridossina negli alcolisti malati cronici, c’è una carenza nella formazione di fosfato piridossale rispetto ai controlli.
Essi descrivono una riduzione in vitro della conversione della piridossina in fosfato piridossale da parte di un enzima eritrocitario in soggetti alcolisti. Questo porta a postulare una soppressione diretta della piridossina fosforilasi eritrocitaria da parte dell’alcol. Tuttavia, una spiegazione alternativa per la diminuzione del fosfato piridossale suggerisce che l’acetaldeide, il principale metabolita dell’alcol stimola l’attività della fosfatasi di membrana e riduce anche la quantità di fosfato piridossale trasferito dal globulo rosso al compartimento plasmatico.
Tuttavia, indipendentemente dal meccanismo, il risultato è lo stesso, tutti portando ad un aumento della quantità di Fe contenuto negli eritroblasti (sideroblasti)
Sideroblastosi comporta scarsa incorporazione di ferro nel globulo rosso con conseguente ipocromia, eritropoiesi inefficace, e sideremia aumentato.
Emosiderosi negli alcolisti (sostituire con 5) Un’ampia varietà di cause di sovraccarico di ferro negli alcolisti sono state implicate da sole o collettivamente compreso l’aumento significativo di ferro di alcune bevande alcoliche (specialmente i vini), aumento della secrezione di acido cloridrico gastrico indotta dall’etanolo, emolisi, perdita di sangue gastrointestinale, carenza di acido folico, aumento dell’assorbimento intestinale dovuto al danno epatico e danno pancreatico, aumentando ulteriormente la sideremia e portando all’emosiderosi.
Alcuni studi documentano un aumento dei livelli di ferritina sierica nei pazienti alcolisti, che riflette un aumento delle riserve di ferro.
Dopo la somministrazione di chelanti del ferro come la desferroxamina e la successiva misurazione della sideruria, le riserve di ferro possono essere valutate semi-quantitativamente. Negli alcolisti l’escrezione di ferro dopo questi chelanti è anche aumentata rispetto ai controlli.
Tuttavia, altri studi mostrano in pazienti alcolisti ospedalizzati che entrambe le concentrazioni di ferro sierico e/o ferritina sono entro limiti normali o meno comunemente elevate. Queste differenze possono essere dovute alla scelta dei pazienti inclusi nello studio; se i pazienti hanno sanguinamento gastrointestinale a causa di varici esofagee, possono avere depositi di ferro impoverito, anche se prima del sanguinamento erano sopra il normale.
Infine, bisogna notare che nella maggior parte degli studi realizzati per misurare il ferro nel siero, questi sono sempre risultati elevati negli alcolisti, con una correlazione tra i depositi di ferro e la quantità di alcol consumato, suggerendo che questo elemento è la causa della siderosi.
Assorbimento del ferro
Circa da 5 a 15 mg di ferro ingerito quotidianamente, solo il 10% viene assorbito.
I fattori che influenzano l’assorbimento del ferro possono intervenire a tre livelli: intraluminale, mucoso e generale.
A livello intraluminale, l’assorbimento del ferro è noto per dipendere dall’interazione di diversi alimenti, in modo che alcuni, come gli aminoacidi, facilitare l’assorbimento e altri possono diminuire. L’assenza di secrezioni digestive può essere un fattore che modifica l’assorbimento.
Nel tentativo di spiegare l’emosiderosi, si è pensato inizialmente che la dieta dei pazienti alcolisti fosse molto ricca di questo elemento. Questa osservazione si basava su ciò che si chiama emosiderosi bantesca o bantus haemosiderosis. Studi condotti da sudafricani su queste tribù hanno scoperto che una bevanda che preparavano chiamata kefir, una specie di birra, veniva prodotta in recipienti di ferro, con un contenuto di ferro da 30 a 100 mg per litro. Il contenuto alcolico della bevanda era molto basso, e ne consumavano grandi quantità, fino a 1000 mg di ferro al giorno. La fabbricazione del kefir non viene più effettuata con la conseguente scomparsa dell’emosiderosi in questa tribù.
Le quantità di ferro presenti nelle diverse bevande alcoliche sono molto variabili, arrivando in alcuni casi fino a 350 mg per litro (Romania), anche se in generale si può considerare che il vino (bianco, chiaretto o rosso) è ricco di questo metallo.
Ma ci sono anche molti alcolisti la cui bevanda principale non è il vino ma il whisky, la birra o altri, che contengono quantità trascurabili di ferro.
D’altra parte, nonostante lo studio sui banti, un eccesso di ferro nella dieta non è motivo sufficiente per sviluppare l’emosiderosi. Così, in Etiopia, la base della dieta è il teff, un seme che contiene una grande quantità di ferro, con un apporto giornaliero di 300 a 500 mg di questo metallo. Nonostante questa assunzione i depositi non sono aumentati e la frequenza di anemia da carenza di ferro non è diversa dalla popolazione generale.
È ovvio quindi che la quantità di ferro negli alimenti non ha alcun valore.
Finora sembrerebbe che l’alcol non abbia alcun ruolo a livello intraluminale nell’assorbimento del ferro.
A livello generale si sa che lo stato delle riserve di ferro condiziona il loro assorbimento; se sono diminuite, l’assorbimento aumenta e viceversa. Anche l’eritropoiesi è coinvolta a questo livello, aumentando il suo assorbimento quando aumenta. L’alcol non sembra accelerare il turn over del ferro plasmatico, il che potrebbe spiegare l’aumento del suo assorbimento.
A livello delle mucose, la quantità di ferro contenuta nella mucosa, così come il livello di sintesi proteica, può influenzare l’assorbimento del ferro. È stato dimostrato che la carenza di acido folico in seguito all’ingestione di alcol può essere responsabile di un aumento dell’assorbimento del ferro e della conseguente siderosi, che aggrava gli effetti nocivi dell’alcol sul parenchima e più in particolare sul fegato.
In studi sugli animali è stato dimostrato che la somministrazione cronica di alcol può essere accompagnata da un aumento dell’assorbimento intestinale del ferro, il cui meccanismo è sconosciuto.
Negli ultimi dieci anni sono stati dimostrati almeno tre meccanismi coinvolti nella traslocazione del ferro attraverso la mucosa duodenale:
Trasportatore-mediato (regolato)
Meccanismo passivo mediato da acidi grassi non esterificati
Ingresso paracellulare (non regolato)
Studi in vivo e in vitro hanno mostrato una maggiore permeabilità intestinale negli alcolisti cronici offrendo un possibile meccanismo di assorbimento intestinale del ferro.
Altri studi suggeriscono che ci può essere un aumento della capacità intrinseca della mucosa intestinale dei pazienti alcolisti di assorbire il ferro.
Si è osservato che in quelli con ferro sierico aumentato, le misure di ferro sono diminuite durante la prima settimana di ricovero con lo sviluppo di reticolociti. È stato anche osservato che i cambiamenti sideroblastici erano reversibili in accordo con altri autori. Gli anelli caratteristici sono scomparsi dal midollo durante la prima settimana di ricovero, anche se alcuni hanno persistito per dodici giorni.
Recentemente (sostituire con 6) sono stati trovati livelli sierici aumentati di asialotransferrina in pazienti con alcolismo cronico; questo mostra una maggiore capacità di rilasciare ferro ai tessuti, specialmente agli epatociti, rispetto alle normali varianti di transferrina.
È stato sottolineato che ci può essere anche una forte relazione tra i cambiamenti sideroblastici e la carenza di folati. Si suggerisce che questa carenza può essere la precondizione necessaria per l’espressione dei cambiamenti sideroblastici negli alcolisti, anche se altri autori non sono d’accordo, come nonostante l’anemia marcata non avevano cambiamenti megaloblastici nel midollo e nessuna macrocitosi o ipersegmentazione neutrofila nel sangue periferico e siero e le concentrazioni di folato eritrocitario erano normali.
È importante notare che nei pazienti alcolisti, l’anemia delle malattie croniche dovute a tubercolosi, malattie maligne o insufficienza renale è spesso associata all’anemia sideroblastica, che è molto comune in questa popolazione.
In sintesi, l’assunzione di alcol insieme a una dieta inadeguata può portare allo sviluppo di anemia sideroblastica ed emosiderosi la cui patogenesi non è ancora stabilita e i probabili fattori includono:
Effetto tossico dell’alcol su una o più fasi della sintesi dell’eme.
Associazione con cattivo stato nutrizionale che porta alla deplezione di fosfato piridossale e catabolismo accelerato causato da acetaldeide, malattia epatica o entrambi
Carenza di folato esacerbata e dove il ritiro nutrizionale e la sostituzione giocano un ruolo importante.
Caso clinico:
Un paziente maschio di 55 anni ricoverato con edema degli arti inferiori (1/6 sovrapatellari, 2/6 infrapatellari) e dell’osso sacro di consistenza molle, distensione addominale, pallore della pelle delle mucose, astenia e adinamia progressiva di tre mesi.
Storia:
Alcolismo cronico (2 o 3 litri di vino e/o birra al giorno) e fumo (40 sigarette al giorno), entrambi negli ultimi 30 anni.
Risultati degli studi effettuati in reparto:
Radiografia del torace: effacement del seno costodiaframmatico destro. Indice cardiotoracico leggermente aumentato.
Paracentesi: caratteristiche essudative.
Trasfusioni: A causa di HTO. trasfusione di 2 unità di globuli rossi deplasmati indicata.
Diagnosi presuntiva:
Eziologica: Etilismo cronico. Fumo.
Patofisiologico: sindrome ascitico-edematosa. Sindrome ascitico-edematosa. Seme ascitico-edematoso. Anemico. Versamento pleurico. Insufficienza epatica.
Anatomopatologico: Epatomegalia. Cardiomegalia.
Risultati di studi eseguiti durante il ricovero:
FEDA: gastrite cronica.
Colon con doppio contrasto: transito intestinale conservato.
Ecocardiogramma: Versamento pericardico moderato.
Ecopleurale: Versamento pleurico destro.
Ecoaddominale: Fegato compatibile con fegato grasso.
Serologia: negativo per VDRL, Chagas, Epatite B e C.
PAMO e BMO: midollo osseo con grave dispoiesi della serie rossa.
Perls: si osserva un aumento dei granuli di ferro intra ed extracellulari.
PBH: il materiale ottenuto era poco rappresentativo per la conclusione diagnostica.
Laboratorio
Ematocrito (%): variava da 11.8 a 19
Cellule rosse (x10E12/l): ha presentato una variazione da 1,1 a 1,94
Cellule bianche (x10E9/l): ha presentato una variazione da 7,7 a 9.2
Emoglobina (g/dl): variava da 4,4 a 6.8
Piastrine (x10E9/l): variava da102 a 346
Ferremia (mg/dl): variava da248 a 75
Ferritina (ng/dl): 594
TIBC (Total Iron Binding Capacity) (mg/dl): 360
Percentuale di saturazione della transferrina: presenta una variazione da 95 a 24
Bilirubina totale (mg/dl): presenta una variazione da 1.6 a 0,51
Bilirubina diretta (mg/dl): ha mostrato una variazione da 1,92 a 0,18
Bilirubina indiretta (mg/dl): ha mostrato una variazione da 2,99 a 0,33
Trattamento medico:
Dieta iposodica e povera di proteine. Limitazione dell’acqua.
PHP a 21 gocce al minuto alternativamente. Albumina una fiala in parallelo ogni 8 ore, seguita da una fiala di furosemide. Spironolattone una compressa ogni 12 ore. Phytomenadione (Konakion) una fiala ogni 12 ore.
Lattulosio (Lactulon) un cucchiaio ogni 6 ore. Complesso di vitamina B una compressa ogni 12 ore.
Data la buona risposta del paziente, il trattamento medico orale con diuretici e complesso B viene continuato. Il lattulosio e il fitomenadione furono sospesi.
Il paziente presentò un’evoluzione clinica favorevole per il suo stato edematoso ascitico, per cui fu dimesso, essendo medicato con vitamina B e consigliato di non bere alcol.
Continua il suo controllo medico da parte degli ambulatori della Clinica Medica del nostro Ospedale e dal Servizio di Ematologia dell’Ospedale Álvarez..
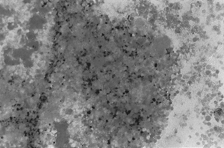
PAMO X 100
– Colorazione di Perls. Spicca un nodulo midollare con intenso deposito di ferro extracellulare.
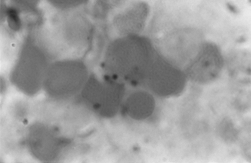
PAMO X 1000
– Colorazione di Perls. Si osserva un deposito di ferro intraeritroblastico.
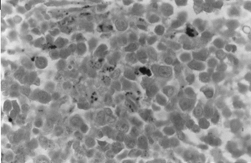
BMOX100
– Colorazione di Perls. Dove si osservano densi accumuli di ferro intra ed extra eritroblastici.
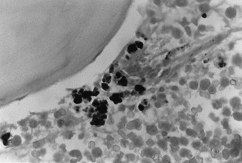
BMO X 1000
– Colorazione Peris. Dove si osservano densi accumuli di ferro intra ed extraitroblastici.
Il paziente ha avuto una buona evoluzione post-internalizzazione. A sessanta giorni fece un esame del sangue con i seguenti risultati: HTO 43%, GR 5,1 X 10E12/L, GB 8,7 X10E9/L, HB 13,9 g/di, Plaq.354 X10E9/L, con solo la conformità al trattamento.
Dopo centoventi giorni fu monitorato di nuovo con gli stessi risultati dell’esame del sangue.