Az elmúlt hónapokban a SARS-CoV-2 olyan változatait mutatták ki, amelyek szokatlan módon sokkal több genommutációt tartalmaznak, mint korábban. Ezeket “aggodalomra okot adó változatoknak” (VOC) nevezték el, mivel feltételezték, hogy a genommutációk hatással lehetnek a terjedésre, az immunrendszer ellenőrzésére és a virulenciára. Az alábbiakban e kérdések mindegyikével külön-külön foglalkozom.
Transzmisszió
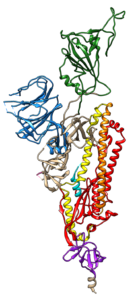
A B.1.1.7 nevű SARS-CoV-2 vonal 2020 szeptemberében jelent meg az Egyesült Királyságban, és 17 genomiális mutációt tartalmaz, amelyek közül néhány a spike fehérje aminosavváltozatait eredményezi (a képen). Hasonló, de eltérő változatokat mutattak ki más helyeken is, többek között Dél-Afrikában (B.1.135) és Brazíliában, de a B.1.1.7-es vonalat vizsgálták a legjobban. A változások jó összefoglalása megtalálható ebben a kéziratban. Számos bizonyíték vezetett arra a következtetésre, hogy a B.1.1.1.7 vonalba tartozó vírusok a korábbi izolátumokhoz képest fokozott átvihetőséggel rendelkezhetnek. Ezek közé tartozik a korábbi változatok rövid időn belüli gyors kiszorulása az Egyesült Királyságban; az ilyen változatok R-indexének nyilvánvaló növekedése; és a vírus RNS megnövekedett szintje a nasopharyngeális mosásokban, PCR vagy RNS-szekvenálással mérve.
A transzmisszió virológiai meghatározása a vírusoknak az egyik gazdaszervezetből a másikba történő átvitele. A SARS-CoV-2 esetében ilyen átvitel akkor következik be, amikor a fertőző vírusrészecskék a légúti cseppekben kilélegezve egy másik gazdaszervezetbe jutnak, ahol fertőzést indítanak el. A B.1.1.1.7 vonal fokozott átvitelére vonatkozó, fent említett bizonyítékok mind közvetettek, és nem bizonyítják, hogy a változatok virológiai értelemben valóban jobban terjednek a gazdák között. A variáns populációnövekedése lehet például az emberi viselkedésben bekövetkezett változások következménye. Az R-indexet, az átvihetőség mértékét nemcsak a vírus, hanem az emberi viselkedés is befolyásolja. Az orrgaratmosásban talált megnövekedett RNS-szint szintén nem meggyőző az átvitel szempontjából. A vírus RNS nem azonos a fertőző vírussal, és nem végeztek olyan vizsgálatokat, amelyek a B.1.1.1.7 vonal változatával fertőzött egyénekből származó fertőző vírus kioldódását más változatokkal összehasonlítva mérték volna.
Kétségtelen, hogy a B.1.1.1.7 vonal gyorsan kiszorította a többit az Egyesült Királyságban. Azt, hogy ez a viselkedés a vírus egyik gazdatestről a másikra való átvitelének fokozott képességének köszönhető-e, nem sikerült bizonyítani. A variánst más országokban is kimutatták, és az ezeken a helyeken való elterjedése nem áll összhangban a fokozott terjedéssel (ahogyan azt fentebb definiáltam). Például most már tudjuk, hogy a B.1.1.1.7 vonal 5-6 héttel az Egyesült Királyságban történő kimutatása előtt jelen volt az Egyesült Államokban, mégis januárban az esetek mindössze 0,3%-át tette ki országosan. Két hónapos kaliforniai forgalom után a becslések szerint ez a vonal az esetek 0,4%-át teszi ki, míg az Egyesült Királyságban hasonló időpontban 1,2%-ot. Floridában a vonal nagyobb elterjedtséggel, az esetek 0,7%-ával jár együtt, de más amerikai államokban nem ez a helyzet.
Ezek az adatok hangsúlyozzák, hogy nem vonhatjuk le azt a következtetést, hogy a B.1.1.7 vonal biológiailag jobban terjed. Valószínűleg több tényező játszik szerepet, és ezért jobb, ha a B.1.1.7 vonalváltozatokat és a többit a fitnesz – a vírus szaporodási sikere – szempontjából vizsgáljuk. A fitneszre számos tényező hatással lehet, nem csak az átvitel. Ezek közé tartozhat a részecske nagyobb fizikai stabilitása, az immunválaszokkal szembeni nagyobb ellenálló képesség, a vírus orrgaratban való jelenlétének hosszabb időtartama, a gazdaszervezetben termelt fertőző vírus mennyiségének növekedése, a fertőzés hatékonyabb megtelepedése a gazdaszervezetben, és így tovább. Ezek bármelyikének enyhe növekedése egy adott variáns kialakulásához vezethet egy populáción belül, de valójában nem befolyásolja az emberről emberre történő átvitelt. Azt is figyelembe kell venni, hogy az ilyen mutációk alapító hatás révén terjednek-e – vagyis hogy a megfelelő időben a megfelelő helyen vannak-e.
A SARS-CoV-2 variánsok terjedésének közelítésére használt statisztikai modellek nem bizonyíthatnak biológiai tulajdonságot, mivel a populáción való áthajtás különböző fitneszparaméterek következménye lehet. Kísérletekre van szükség vagy állatmodellekben (ebben az esetben az emberre való vonatkoztathatóság ismeretlen), vagy a fertőző vírus mérésére emberekben. Ez utóbbiak közül eddig egyiket sem végezték el a jelenlegi változatok esetében.
Immunkontroll
Közvetlenebb kérdés, hogy a VOC-on belül a spike fehérje bármelyik változása befolyásolja-e az immunválasznak a fertőzések kontrollálására való képességét. Ezt a kérdést közvetlenül a semlegesítő antitestek esetében vizsgálták, pl. azoknál, amelyek képesek blokkolni a fertőzést. Az antitestek felismerik a vírusrészecskén található specifikus fehérjeszekvenciákat, és különösen a spike fehérjét azok esetében, akik mRNS-vakcinát kaptak. A variánsokban azonosított spike-változások egy része olyan régiókban található, amelyekről ismert, hogy antitesteket kötnek. Következésképpen fontos kérdés, hogy a vakcinázás képes-e gátolni a vírusváltozatokkal való fertőzést.
Ezt a kérdést a Moderna és a Pfizer mRNS-vakcinák esetében is megvizsgálták. Az mRNS-1273-mal immunizált személyek szérája hatékonyan semlegesítette a B.1.1.1.7 vonalból származó SARS-CoV-2 spike glikoproteint hordozó pszeudotípusos vírusokat. Ezek a szérumok csökkent (6,4-szeres) semlegesítési titerrel rendelkeztek, amikor a dél-afrikai B.1.351 vonalból származó vírusokat használták. Ezek a szérumok azonban még mindig teljes mértékben semlegesítették a B.1.351-et 1:290-es titerrel, ami elegendő lehet a súlyos COVID-19 megelőzéséhez. Mindazonáltal a Moderna bejelentette, hogy egy módosított vakcinát (mRNS-1273.351) fog előállítani, amely a B.1..351 aminosavváltozásokat.
Egy külön vizsgálatban a Pfizer BNT162b2 mRNS-vakcinával beoltott egyének szérumát a B.1.1.7 (69/70 aminosavak törlése, N501Y, D614G) vagy a B.1.351 (E484K + N501Y + D614G) vonalból kiválasztott tüskés aminosavváltozásokat tartalmazó SARS-CoV-2 vírusokkal végzett neutralizációs vizsgálatokban tesztelték. Ezek a módosítások kis mértékben befolyásolták a szérumokkal való semlegesítést. A módosított vírusok azonban nem tartalmazzák a B.1.1.7 és B.1.351 vírusokban található változások teljes körét, ami megmagyarázhatja az mRNS-1273 által indukált antitestekkel összehasonlított szérumok eltérő eredményeit.
Ezek a megfigyelések bizalmat adnak annak, hogy a két mRNS-vakcina védelmet nyújt a jelenleg keringő változatok által okozott COVID-19 ellen. A genomikai felügyeletet azonban fokozni kell annak biztosítása érdekében, hogy az esetlegesen megjelenő új tüskeváltozásokat gyorsan észleljék, és meghatározzák a semlegesítésre gyakorolt hatásukat.
A betegség súlyossága
Egy korábbi vizsgálat nem mutatott bizonyítékot arra, hogy a B.1.1.7 vonalba tartozó vírusok a kórházi kezelés vagy a halálozás fokozott kockázatával járnának. Három különálló vizsgálat további adatainak vizsgálata után azonban a NERVTAG arra a következtetésre jutott, hogy “reális a lehetősége annak, hogy a VOC B.1.1.7 vírusokkal való fertőzés a nem VOC vírusokkal való fertőzéshez képest megnövekedett halálozási kockázattal jár”. Erre a következtetésre a VOC B.1.1.1.7 vagy nem VOC vírusokkal fertőzött egyének körében jelentett halálozási arányok statisztikai elemzésével jutottak. Az egyik vizsgálatban például a halálozás relatív kockázata 1,35 volt (1,08-1,68 közötti 95%-os konfidenciaintervallummal). Egy másik vizsgálatban a VOC-vírusok vagy nem VOC-vírusok által okozott esetek halálozási arányának átlagos aránya 1,36 volt (95%-os CI 1,18-1,56). Ezek kis különbségek, nagy konfidenciaintervallumokkal, amelyek a nincs hatástól a nagyobb hatásig terjednek, és a szerzők megjegyzik, hogy a halálozás abszolút kockázata továbbra is alacsony. A statisztikákat az összes COVID-19 vírussal kapcsolatos haláleset korlátozott adathalmazának (8%) elemzésével számították ki, és következésképpen hibásak lehetnek. Továbbá nem tűnik úgy, hogy a VOC-vírusok okozta fertőzéssel összefüggésben megnövekedett kórházi kezelés kockázata állna fenn. Az én olvasatom szerint ez a jelentés elsősorban figyelmeztetésként szolgál a variánsok genomikai felügyeletének folytatására a halálozási kockázat tekintetében, és nem von le következtetést az ok-okozati összefüggésekre vonatkozóan.
Frissítve: A Novavax most tette közzé a 3. fázisú, tüskefehérje alapú COVID-19 vakcina első eredményeit. A hatékonyság közel 90%-os volt az Egyesült Királyságban, de egy kisebb dél-afrikai vizsgálatban 50%-os volt a B.1.135 variáns ellen.