Bevezetés
A vas és az alkohol felszívódására vonatkozó első említés az emberiség történetében talán Kr. e. 1200-ból származik, egy thesszáliai legenda szerint Iphycus Apolodorus, aki egy mezőn állva nézte, ahogy apja bárányokat kasztrál, ugyanezzel a büntetéssel fenyegették; amikor felnőtté vált, Apolodorus impotens lett. Egy Melampus nevű varázsló, akit egy keselyű ihletett, úgy gyógyította meg Apolodorust, hogy egy pohár borban megitatta vele annak a késnek a rozsdáját, amellyel apja kasztrálta a bárányokat, és amellyel őt fenyegették.
A kórházunkban látott alkoholbetegek, valamint a kórházi kezelést igénylő betegek száma, figyelembe véve az ezzel járó összes kóros entitást, igen nagy.
Ezzel a közleményünkkel az a célunk, hogy felidézzük az alkoholizmusban jelenlévő hematológiai kórképek egyikét, amely az absztinencia mellett gyakran visszafejlődhet: a szideroblasztos vérszegénységet és a hemosziderózist.
Bjorkman 1956-ban négy krónikus refrakter anémiás és szideroblasztos gyűrűs beteget írt le, akiknél a csontvelősejtek poroszkék festődést mutattak.
Az első bizonyítékot, hogy ezek a szideroblasztgyűrűk az alkohollal kapcsolatosak, Mac Gibbon és Mollin javasolta 1965-ben, azóta az alkoholizmus vált e kórkép leggyakoribb okává.
1969-ben Hines (az i-t 1-gyel helyettesítve) leírta a krónikus alkoholizmusban az absztinencia következtében kialakuló reverzibilis szideroblasztos anaemia előfordulását.
Az alkohol hatásai
Az alkoholnak a vérképzőszövetre gyakorolt többszörös kóros hatása (2-re cserélve) a következőkre osztható:
Az alkohol közvetlen hatásából eredő
A táplálkozási hiányosságok másodlagos hatásaiból eredő
A májbetegség által okozott
A vérszegénység gyakori ok az alkoholistáknál.(3 helyett) Ezek közül a leggyakoribbak a megaloblasztos vérszegénység és a szideroblasztos vérszegénység.
Az utóbbi a táplálkozási tényezőkkel és a B6-vitamin metabolizmusának zavarával függ össze.
A piridoxin piridoxálfoszfáttá, a B6-vitamin aktív formájává való átalakulási képességének csökkenését az eritrociták piridoxálfoszfokináz aktivitásának gátlása következtében mutatták ki.
Azt is feltételezték, hogy az etanol a sejtpiridoxál-foszfát lebontásának felgyorsításával a membrán alkalikus foszfatáz serkentőjeként hathat (4-re cserélve). A piridoxin metabolizmusának ezt a változását alátámasztja a piridoxin metabolitjának számító 4-piridoxsav vizeletkiválasztásának csökkenése és a szérum piridoxálfoszfát szintjének csökkenése.
A piridoxálfoszfát a delta-aminolevulinsav szintézisében is segítő tényezőként működik, amely a vasat tartalmazó hemoglobinfrakció, azaz a hemo egyik prekurzora.
Más vizsgálatok kimutatták, hogy az etanol nemcsak közvetlenül, hanem metabolitja, az acetaldehid révén is hat. Az acetaldehidnek tulajdonítják azt is, hogy fokozza a piridoxálfoszfát lebomlását, ami a szérum piridoxálfoszfát csökkenéséhez vezet, és rontja a piridoxálfoszfát képződését az emberi vörösvértestekben in vitro a foszforilált B6-vitamin-vegyületek lebomlásának felgyorsításával.
A vasfestési módszerek (poroszkék és gyöngyházfestés) alkalmazásakor a nem heme vastartalmú fémszemcsék, feltehetően heemosiderin vagy ferritin formájában, hajlamosak gyűrűt alkotni az eritroblasztok magja körül. Ezeket szideroblasztgyűrűknek vagy gyűrűs szideroblasztoknak nevezik.
Az elektronmikroszkópia kimutatta, hogy ezekben a szideroblasztokban a vaslerakódások a mitokondriumok vagy a citoplazmatikus testek szintjén vannak.
Ezek a morfológiai eltérések a nem hatékony erythropoiesis összes jellemzőjével társulnak: erythroid hyperplasia, a csontvelői erythroid prekurzorok fokozott vasfelvétele, a vas szubnormális beépülése a keringő hemoglobinba, a vas visszaáramlásával a keringésbe, ami hyperferrémiát, a normoblasztok marcona pusztulását, anaemiát és reticulocytopeniát okoz.
A szideroblasztos gyűrű gyakorisága az eritroid csontvelőben gyakoribb a krónikus betegekben és az alultáplált alkoholos betegekben.
Klinikai és kísérleti bizonyítékok arra utalnak, hogy egy táplálkozási tényező fontos szerepet játszik az alkoholbetegek szideroblasztos vérszegénységének patogenezisében.
Az alkohol kísérleti, krónikus adagolása emberi önkénteseken szideroblasztos elváltozásokat okozott a csontvelőben.
Amikor az alkoholt alacsony étrendi piridoxin- és folsavszint mellett adták, a
sideroblasztok gyűrűi néhány hét után a legtöbb vizsgált alanynál kialakultak.
1970-ben Hines és Cowan a piridoxin piridoxálfoszfáttá történő foszforilációjának megváltozását említi, így a piridoxin-anyagcsere zavarait három vizsgálatsorral igazolta:
A piridoxálfoszfát és a szideroblasztos gyűrűk csökkenése 3 alanyból 2-nél jelentkezett, akiket alacsony folsavtartalmú étrenden tartottak alkoholpótlással. Ezután hematológiai választ mutattak a piridoxilfoszfát adagolását követően, de folsav vagy piridoxinterápiás szerek esetén nem.
A krónikusan beteg alkoholistáknál a piridoxin adagolását követően a kontrollokhoz képest hiány mutatkozik a piridoxilfoszfát képződésében.
Leírják a piridoxin piridoxálfoszfáttá történő átalakulásának in vitro csökkenését egy eritrocita enzim által alkoholbetegeknél. Ez az eritrociták piridoxin-foszforilázának alkohol általi közvetlen szuppresszióját feltételezi. A piridoxál-foszfát csökkenésének alternatív magyarázata szerint azonban az alkohol fő metabolitja, az acetaldehid serkenti a membránfoszfatáz-aktivitást, és csökkenti a vörösvértestből a plazmakompartmentbe jutó piridoxál-foszfát mennyiségét.
A mechanizmustól függetlenül azonban az eredmény ugyanaz, mindegyik az eritroblasztokban (szideroblasztokban) lévő Fe mennyiségének növekedéséhez vezet
A szideroblasztózis a vasnak a vörösvértestekbe való rossz beépülésével jár, ami hipokrómia, hatástalan eritropoézis és fokozott sziderémia kialakulásához vezet.
Hemosiderosis alkoholistáknál(5-re cserélve) Az alkoholisták vastúlterhelésének számos oka van, amelyeket külön-külön vagy együttesen, beleértve egyes alkoholos italok (különösen a borok) jelentős vasszint-emelkedését, etanol okozta fokozott gyomorsósav-szekréció, hemolízis, gyomor-bélrendszeri vérveszteség, folsavhiány, májkárosodás miatt fokozott bélrendszeri felszívódás és hasnyálmirigy-károsodás, ami tovább fokozza a sziderémiát és hemosziderózist eredményez.
Az alkoholbetegek megnövekedett szérumferritinszintjét több tanulmány is dokumentálja, ami a megnövekedett vasraktárakra utal.
A vas kelátorok, például desferroxamin adása és az ezt követő szideruria mérése után a vasraktárak félig-meddig kvantitatív módon értékelhetők. Alkoholistáknál a vaskiválasztás ezen kelátumok után is megnövekedett a kontrollhoz képest.
Más vizsgálatok azonban azt mutatják kórházi alkoholbetegeknél, hogy mind a szérum vas- és/vagy ferritinkoncentráció a normál határértékeken belül van, vagy ritkábban emelkedett. Ezek a különbségek a vizsgálatba bevont betegek kiválasztásából adódhatnak; ha a betegeknek a nyelőcső visszértágulatai miatt gyomor-bélrendszeri vérzésük van, a vasraktáraik kimerülhetnek, még akkor is, ha a vérzés előtt a normálisnál magasabbak voltak.
Végezetül meg kell jegyezni, hogy a legtöbb vizsgálatban, amelyet a szérumvas mérésére végeztek, ezeket mindig emelkedettnek találták az alkoholistáknál, és összefüggést találtak a vaslerakódás és az elfogyasztott alkohol mennyisége között, ami arra utal, hogy ez az elem a sziderózis oka.
A vas felszívódása
A naponta bevitt vasnak körülbelül 5-15 mg-ból csak 10%-a szívódik fel.
A vas felszívódását befolyásoló tényezők három szinten avatkozhatnak be: intraluminális, nyálkahártyán belüli és általános szinten.
A vas felszívódása intraluminális szinten köztudottan a különböző élelmiszerek kölcsönhatásától függ, így egyesek, például az aminosavak, elősegítik a felszívódást, mások pedig csökkenthetik azt. Az emésztési váladék hiánya olyan tényező lehet, amely módosítja a felszívódást.
A hemosziderózis magyarázatára tett kísérlet során először azt gondolták, hogy az alkoholbetegek étrendje nagyon gazdag ebben az elemben. Ennek a megfigyelésnek az alapja az úgynevezett bantus haemosiderosis vagy bantus haemosiderosis volt. Dél-afrikaiak által e törzseken végzett tanulmányok megállapították, hogy az általuk készített kefir nevű italt, egyfajta sört, vasedényekben főzték, vastartalma literenként 30-100 mg volt. Az ital alkoholtartalma nagyon alacsony volt, és nagy mennyiséget fogyasztottak belőle, akár napi 1000 mg vasat is. A kefir előállítása már nem folyik, aminek következtében a hemosiderózis eltűnt ebben a törzsben.
A különböző alkoholos italokban lévő vas mennyisége nagyon változó, egyes esetekben akár 350 mg/liter (Románia) is lehet, bár általánosságban elmondható, hogy a bor (fehér, bordó vagy vörös) gazdag ebben a fémben.
De sok alkoholista is van, akinek a fő itala nem a bor, hanem a whisky, a sör vagy más italok, amelyek elhanyagolható mennyiségű vasat tartalmaznak.
Másrészt, a bantuszokon végzett tanulmányok ellenére, a táplálékban lévő vastöbblet nem elegendő ok a hemosziderózis kialakulásához. Így Etiópiában az étrend alapja a teff, egy nagy mennyiségű vasat tartalmazó mag, amelyből naponta 300-500 mg-ot kell bevinni. E bevitel ellenére a lerakódások nem növekednek, és a vashiányos vérszegénység gyakorisága nem különbözik az átlagpopulációétól.
Az tehát nyilvánvaló, hogy az élelmiszerekben lévő vasmennyiségnek nincs jelentősége.
Egyelőre úgy tűnik, hogy az alkohol intraluminális szinten nem játszik szerepet a vas felszívódásában.
Az általános szinten ismert, hogy a vasraktárak állapota befolyásolja a felszívódást; ha ezek csökkennek, a felszívódás nő, és fordítva. Az eritropoézis ezen a szinten is részt vesz, növelve a felszívódást, amikor megnő. Úgy tűnik, hogy az alkohol nem gyorsítja a plazma vasának átfordulását, ami magyarázatot adhat a felszívódás növekedésére.
A nyálkahártya szintjén a nyálkahártyában található vas mennyisége, valamint a fehérjeszintézis szintje befolyásolhatja a vas felszívódását. Kimutatták, hogy az alkoholfogyasztást követő folsavhiány felelős lehet a fokozott vasfelszívódásért és az azt követő sziderózisért, ami súlyosbítja az alkohol káros hatásait a parenchimára és különösen a májra.
Állatkísérletekben kimutatták, hogy a krónikus alkoholbevitel a bélrendszeri vasfelszívódás növekedésével járhat, amelynek mechanizmusa ismeretlen.
Az elmúlt évtizedben legalább három, a vasnak a nyombélnyálkahártyán keresztüli transzlokációjában szerepet játszó mechanizmust mutattak ki:
Transzporter által közvetített (szabályozott)
Passzív mechanizmus, amelyet nem-észterezett zsírsavak közvetítenek
(Szabályozatlan) paracelluláris bejutás
In vivo és in vitro vizsgálatok kimutatták a krónikus alkoholisták fokozott bélpermeabilitását, amely a bélrendszeri vasfelszívódás lehetséges mechanizmusát kínálja.
Más vizsgálatok arra utalnak, hogy az alkoholbetegek bélnyálkahártyájának intrinzikális vasfelvevő képessége megnövekedhet.
Megfigyelték, hogy azoknál, akiknek szérumvasszintje emelkedett, a kórházi kezelés első hetében a retikulociták kialakulásával együtt csökkentek a vasmérések. Azt is megfigyelték, hogy a szideroblasztos elváltozások más szerzőkkel összhangban reverzibilisek voltak. A jellegzetes gyűrűk a kórházi kezelés első hetében eltűntek a csontvelőből, bár néhány még tizenkét napig fennmaradt.
A közelmúltban (6. helyett) krónikus alkoholizmusban szenvedő betegeknél megnövekedett szérum asialotranszferrin-szintet találtak; ez a normál transzferrin-változatokhoz képest a vas szövetekbe, különösen a hepatocitákba történő felszabadulásának fokozott képességét mutatja.
Rámutattak, hogy a szideroblasztos elváltozások és a folsavhiány között is szoros kapcsolat állhat fenn. Azt feltételezik, hogy ez a hiány lehet a szükséges előfeltétele a szideroblasztos elváltozások kifejeződésének az alkoholistáknál, bár más szerzők nem értenek ezzel egyet, mivel a kifejezett vérszegénység ellenére nem volt megaloblasztos elváltozás a csontvelőben, és nem volt makrocitózis vagy neutrofil hiperszegmentáció a perifériás vérben, és a szérum és az eritrociták folsavkoncentrációja normális volt.
Fontos megjegyezni, hogy az alkoholbetegeknél a tuberkulózis, rosszindulatú betegségek vagy veseelégtelenség miatt kialakuló krónikus betegségek vérszegénysége gyakran társul szideroblasztos vérszegénységgel, ami nagyon gyakori ebben a populációban.
Összefoglalva, az alkoholfogyasztás a nem megfelelő táplálkozással együtt valószínűleg szideroblasztos vérszegénység és hemosziderózis kialakulásához vezet, amelynek patogenezise még nem tisztázott, de a valószínű tényezők közé tartoznak:
Az alkohol toxikus hatása a hemszintézis egy vagy több lépésére.
Az acetaldehid, májbetegség vagy mindkettő által okozott piridoxál-foszfát kimerüléshez és gyorsított katabolizmushoz vezető rossz tápláltsági állapottal való összefüggés
Elterjedt folsavhiány, és ahol a táplálékmegvonás és pótlás jelentős szerepet játszik.
Klinikai eset:
Egy 55 éves férfi beteg az alsó végtagok (1/6 suprapatelláris, 2/6 infrapatelláris) és a keresztcsont puha állagú ödémájával, haspuffadással, a bőr nyálkahártya sápadtságával, aszténiával és három hónapja tartó progresszív adynamiával jelentkezett.
Előzmények:
Krónikus alkoholizmus (napi 2-3 liter bor és/vagy sör) és dohányzás (napi 40 szál cigaretta), mindkettő az elmúlt 30 évben.
A kórteremben végzett vizsgálatok eredményei:
Mellkasröntgen: a jobb costodiaphragmatikus sinus kiürülése. A szív- és mellkasi index enyhén emelkedett.
Paracentézis: exsudatív tünetek.
Transzfúziók: HTO miatt. 2 egység deplazmatizált vörösvértest transzfúziója javallott.
Presumptív diagnózis:
Etiológiai: Krónikus etilizmus. Dohányzás.
Patofiziológiai: Ascitikus-ödémás szindróma. Ascitisz-ödémás szindróma. Ascitikus-ödémás kenet. Anaemiás. Pleuralis folyadékgyülem. Májelégtelenség.
Anatomopatológiai: Hepatomegália. Kardiomegália.
A kórházi tartózkodás alatt végzett vizsgálatok eredményei:
FEDA: Krónikus gastritis.
Dupla kontrasztos beöntés vastagbél: A bél tranzitja megmaradt.
Echokardiogram: Mérsékelt perikardiális folyadékgyülem.
Echopleuralis: Jobb oldali pleuralis folyadék.
Echoabdominalis: Zsírmájjal összeegyeztethető máj.
Serológia: VDRL, Chagas, Hepatitis B és C negatív.
PAMO és BMO: A csontvelőben súlyos dyspoiesis a vörös sorozatokban.
Perls: fokozott intra- és extracelluláris vasszemcsék figyelhetők meg.
PBH: a kapott anyag kevéssé volt reprezentatív a diagnosztikai következtetés levonásához.
Laboratórium
Hematokrit (%): 11 között változott.8-19
Vörösvértestek (x10E12/l): 1,1 és 1,94 között változott
Fehérvértestek (x10E9/l): 7,7 és 9 között változott.2
Hemoglobin (g/dl): 4,4 és 6 között változott.8
Plateletek (x10E9/l): 102 és 346
Ferrémiás szint (mg/dl): 248 és 75
Ferritin ( ng/dl): 594
TIBC (teljes vasmegkötő kapacitás) (mg/dl): 360
Transzferrin telítettségi százalék: 95 és 24 között változott
Teljes bilirubin (mg/dl): 1.6 és 0,51 között
Direkt bilirubin (mg/dl): 1,92 és 0,18 között változott
Indirekt bilirubin (mg/dl): 2,99 és 0,33 között változott
Az orvosi kezelés:
Hyposzódium és fehérjeszegény diéta. Vízkorlátozás.
PHP 21 csepp per perc váltakozva. Albumin egy ampulla párhuzamosan 8 óránként, majd egy ampulla furoszemid. Spironolakton egy tabletta 12 óránként. Fitomenadion (Konakion) egy ampulla 12 óránként.
Laktulóz (Lactulon) egy evőkanál 6 óránként. B-vitamin-komplex 12 óránként egy tabletta.
A beteg jó válasza miatt a diuretikumokkal és B-komplexszel történő orális gyógyszeres kezelés folytatódik. A laktulózt és a fitomenadiont abbahagyták.
A beteg aszcitiszes ödémás állapota kedvezően alakult, ezért elbocsátották, B-vitaminnal kezelték, és tanácsolták, hogy ne fogyasszon alkoholt.
Kórházunk Orvosi Klinikájának ambulanciáin és az Álvarez Kórház Hematológiai Szolgálatán folyamatos az orvosi ellenőrzése.
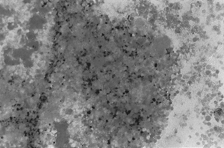
PAMO X 100
– Perls-festés. Kiemelkedik egy intenzív extracelluláris vaslerakódással rendelkező medulláris csomó.
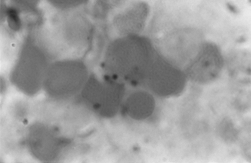
PAMO X 1000
– Perls-festés. Intraerythroblastikus vaslerakódás figyelhető meg.
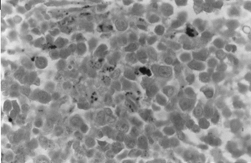
BMOX100
– Perls-festés. Ahol sűrű intra- és extra-erythroblastikus vasfelhalmozódások figyelhetők meg.
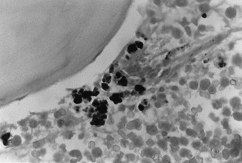
BMO X 1000
– Peris festés. Ahol sűrű intra- és extraitroblastikus vasfelhalmozódások figyelhetők meg.
A beteg jól fejlődött az internálás után. Hatvan nap múlva vérvizsgálatot végeztek rajta a következő eredményekkel: HTO 43%, GR 5,1 X 10E12/L, GB 8,7 X10E9/L, HB 13,9 g/di, Plaq.354 X10E9/L, kizárólag a kezelés betartása mellett.
Százhúsz nap múlva ismét ellenőrizték, ugyanazokkal a vérvizsgálati eredményekkel.
Százhúsz nap múlva ismét ellenőrizték, ugyanazokkal a vérvizsgálati eredményekkel.
Százhúsz nap múlva ismét ellenőrizték, ugyanazokkal a vérvizsgálati eredményekkel.