Az addukt (a latin adductus, “felé húzott” szóból, alternatívaként az “addíciós termék” szűkítése) két vagy több különböző molekula közvetlen addíciójának terméke, amelynek eredményeként egyetlen reakciótermék keletkezik, amely tartalmazza az összes komponens összes atomját. Az eredményt különálló molekulafajnak tekintik. Ilyen például a nátrium-biszulfit addíciója egy aldehidhez, amely szulfonátot eredményez. Ez éppen úgy tekinthető, mint a különböző molekulák közvetlen kombinációjából származó egyetlen termék, amely a reagáló molekulák összes atomját tartalmazza.
A Lewis-savak és Lewis-bázisok között gyakran képződnek adduktok. Jó példa erre a Lewis-sav borán és a Lewis-bázisok oxigénatomja, a tetrahidrofurán (THF) oxigénatomja közötti adduktképződés: BH3-O(CH2)4 vagy dietil-éter: BH3-O(CH3CH2)2. Számos Lewis-sav és Lewis-bázis gázfázisban vagy nem vizes oldószerben történő, adduktok képződését eredményező reakcióját vizsgálták az ECW-modellben. A trimetil-bór, a trimetil-tin-klorid és a bisz(hexafluoroacetilacetonato)réz(II) olyan Lewis-savak példái, amelyek sztérikus hatást mutató adduktokat képeznek. Például: a trimetil-tin-klorid dietil-éterrel reagálva sztérikus taszítást mutat az Sn metilcsoportjai és az oxigén etilcsoportjai között. Ha azonban a Lewis-bázis tetrahidrofurán, a sztérikus taszítás csökken. Az ECW-modell segítségével mérhetőek ezek a sztérikus hatások.
-
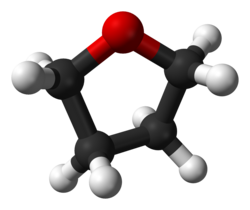
THF molekula
-
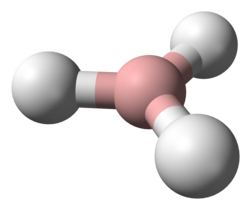
BH3 molekula
-
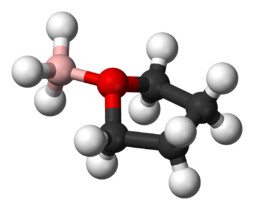
Lewis-addukt BH3 és THF között
Azokat a vegyületeket vagy keverékeket, amelyek sztérikus akadályok miatt nem tudnak adduktot képezni, frusztrált Lewis-pároknak nevezzük.
Az adduktok nem feltétlenül molekuláris jellegűek. Jó példa a szilárdtest-kémiából a CuAlCl4 etilén vagy szén-monoxidjának adduktjai. Ez utóbbi egy kiterjesztett rácsszerkezetű szilárd anyag. Az addukt kialakulásakor egy új, kiterjesztett fázis jön létre, amelyben a gázmolekulák a szerkezeten belül a rézatomok ligandumaként beépülnek (beilleszkednek). Ez a reakció egy bázis és egy Lewis-sav közötti reakciónak is tekinthető, ahol a rézatom az elektronfelvevő szerepben, a gázmolekula pi-elektronjai pedig az elektrondonáló szerepben vannak.


