Más de 200.000 personas se han sometido a una sustitución valvular aórtica transcatéter (TAVR), y cada año aproximadamente 140.000 pacientes reciben una válvula bioprotésica quirúrgica.1,2 A pesar de este volumen creciente, la estrategia óptima de anticoagulación postoperatoria a menudo no está clara. En concreto, hay dos cuestiones que ponen de manifiesto la dificultad en la toma de decisiones para estos escenarios clínicos comunes:
- En los meses iniciales tras la sustitución de la válvula bioprotésica, ¿qué complicaciones intentamos reducir con la anticoagulación?
- ¿Deberíamos proporcionar anticoagulación a todos los pacientes para reducir estas complicaciones? ¿O deberíamos tener un enfoque más selectivo basado en los factores de riesgo?
Riesgos trombóticos tras la sustitución de la válvula bioprotésica
Tradicionalmente, la justificación de la anticoagulación en los primeros meses tras la sustitución quirúrgica de la válvula ha sido mitigar las complicaciones trombóticas, presumiblemente relacionadas con el material de sutura y un anillo de costura que aún no está cubierto de biofilm y endotelizado.3,4 Las posibles complicaciones trombóticas posteriores son tres: eventos tromboembólicos, trombosis manifiesta de la válvula y trombo organizado subclínico que puede perjudicar la función de la válvula a largo plazo. A pesar de la frecuencia del reemplazo de la válvula bioprotésica, los datos relacionados con estas complicaciones son limitados, en parte porque estos eventos son aparentemente infrecuentes.
Un reciente meta-análisis destacó la baja tasa de eventos después del reemplazo de la válvula bioprotésica. En este análisis de 31.740 pacientes, predominantemente con sustitución quirúrgica de la válvula aórtica, se produjeron acontecimientos tromboembólicos tempranos en 145 pacientes (1%) que tomaban antagonistas de la vitamina K y en 262 pacientes (1,5%) que no tomaban antagonistas de la vitamina K (odds ratio 0,96; intervalo de confianza del 95%, 0,60-1,52).5 Si se parte de la hipótesis de que en realidad hay un aumento del 0,5% de las complicaciones tromboembólicas en los primeros meses después de la sustitución quirúrgica de la válvula aórtica en los pacientes que no toman antagonistas de la vitamina K, un ensayo controlado aleatorio con la potencia adecuada requeriría aproximadamente 15.500 pacientes.6 Hasta la fecha, se han realizado 2 ensayos aleatorios, con un total de 268 pacientes.7,8 Dado el reducido número de pacientes, no es sorprendente la falta de una diferencia estadísticamente detectable en los 2 grupos.
A falta de grandes ensayos controlados aleatorios, los médicos deben recurrir a estudios observacionales para obtener información, como el análisis del Registro Nacional Danés de Pacientes.9 En este estudio de 4.075 pacientes con sustituciones valvulares aórticas bioprotésicas, la interrupción de la warfarina se asoció a un aumento de los episodios tromboembólicos y las muertes cardiovasculares entre 1 y 6 meses después de la cirugía. Curiosamente, aunque la tasa de accidentes cerebrovasculares aumentó en los primeros 3 meses en el grupo de tratamiento, el número de accidentes cerebrovasculares entre los 3 y los 6 meses no fue diferente entre los pacientes que continuaron o suspendieron la warfarina, aunque sólo hubo 21 eventos durante este período. Además, no hubo diferencias en las hemorragias entre los 3 meses y el año. Esta observación es contraria a informes anteriores y a la experiencia clínica de que los pacientes que toman warfarina tienen más probabilidades de ser hospitalizados por hemorragias.5 Por lo tanto, las conclusiones de los autores respecto a la mortalidad cardiovascular y los eventos tromboembólicos pueden haber estado relacionadas con un factor de confusión residual. En concreto, es posible que no haya habido diferencias en los episodios hemorrágicos porque los médicos eran menos propensos a iniciar o continuar la anticoagulación en los pacientes de mayor riesgo.
Desgraciadamente, en comparación con los episodios tromboembólicos, los datos publicados proporcionan aún menos información sobre las asociaciones inferenciales para la trombosis de la válvula bioprotésica. Se han notificado pocos acontecimientos, y la mayor parte de la literatura se limita a series de casos y experiencias de un solo centro.10 En consecuencia, la incidencia de la trombosis de la válvula bioprotésica no está bien definida, aunque en un estudio, sólo 8 de 4.568 pacientes con válvulas aórticas bioprotésicas requirieron una reintervención por estenosis aórtica relacionada con el trombo.11 Asimismo, se desconoce en gran medida el papel de la trombosis clínicamente silenciosa y la posible degeneración acelerada de la válvula bioprotésica.
Anticoagulación selectiva tras la sustitución de la válvula bioprotésica
A partir de una magnitud de beneficio poco clara y un riesgo de hemorragia bien aceptado, la anticoagulación universal tras la sustitución de la válvula aórtica bioprotésica es difícil de justificar; esta incertidumbre se refleja en la recomendación de clase IIb de las directrices sobre cardiopatías valvulares del American College of Cardiology y la American Heart Association (ACC/AHA) de 2014.12 Sin embargo, pueden surgir situaciones clínicas específicas en las que la anticoagulación debe considerarse con más fuerza. Por ejemplo, en un reciente estudio de casos y controles que incluyó a 46 pacientes con reoperación por trombosis de la válvula aórtica bioprotésica, un aumento >50% de los gradientes Doppler medios en la ecocardiografía con respecto a los valores iniciales, un aumento del grosor de las cúspides y una movilidad anormal de las cúspides se asociaron a la trombosis de la válvula.13 Por lo tanto, en estos pacientes podría considerarse un ensayo de anticoagulación y ecocardiografía de seguimiento para evaluar los gradientes Doppler,14 aunque no está claro hasta qué punto la función valvular a corto y largo plazo se modifica con la anticoagulación.
Además, los pacientes con una válvula mitral bioprotésica parecen tener un mayor riesgo de sufrir eventos tromboembólicos y trombosis valvular (véase el caso ilustrativo, con las figuras 1-2 y los vídeos 1-2, a continuación). Dado que la sustitución de la válvula mitral bioprotésica es mucho menos frecuente que la sustitución de la válvula aórtica, los datos son aún más limitados. Sin embargo, en un estudio unicéntrico de 216 pacientes con sustitución valvular mitral bioprotésica, 10 (5%) sufrieron un ictus isquémico en un plazo de 6 meses.15 Además, en otro estudio de 149 pacientes consecutivos, 9 (6%) desarrollaron una trombosis de la válvula mitral bioprotésica.16 Por lo tanto, los pacientes con sustitución de la válvula mitral bioprotésica parecen estar en mayor riesgo, y debe considerarse la anticoagulación rutinaria durante 3-6 meses, de nuevo reflejada por la recomendación de clase IIa en las directrices de cardiopatía valvular del ACC/AHA de 2014.12
Caso ilustrativo: trombosis de la válvula mitral bioprotésica
Una mujer de 71 años se presentó con insuficiencia cardíaca 8 meses después de la sustitución de la válvula mitral bioprotésica por estenosis mitral reumática. En el postoperatorio, había sido tratada con cumadina durante 3 meses y continuaba con aspirina. No tenía antecedentes de fibrilación auricular y había estado afebril, y los hemocultivos fueron negativos.
Vídeo 1
Figura 1
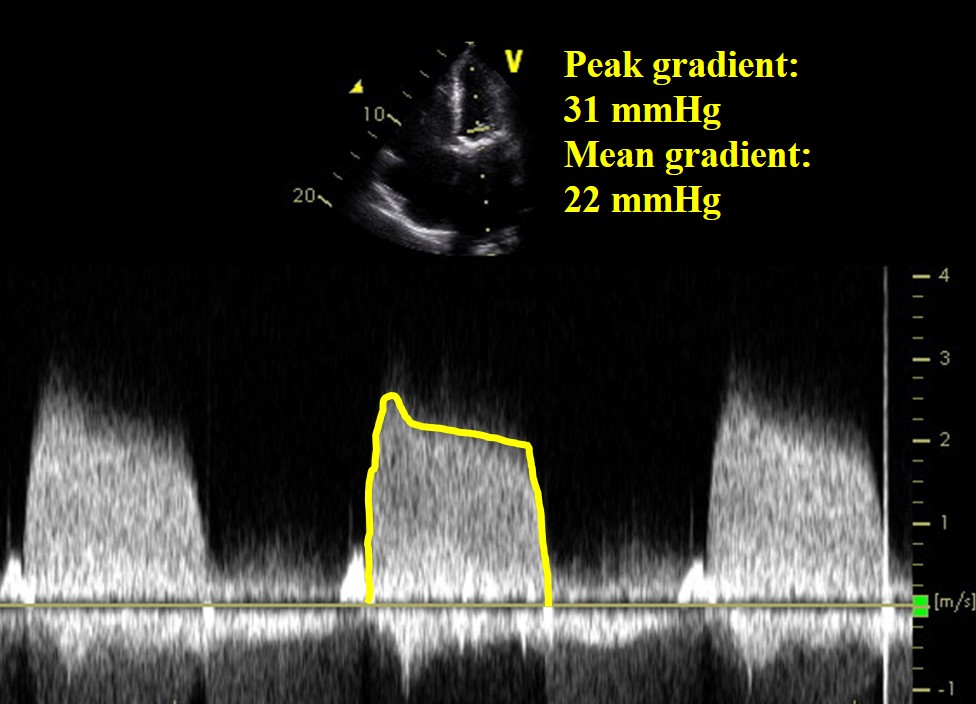
Vídeo 2
Figura 2
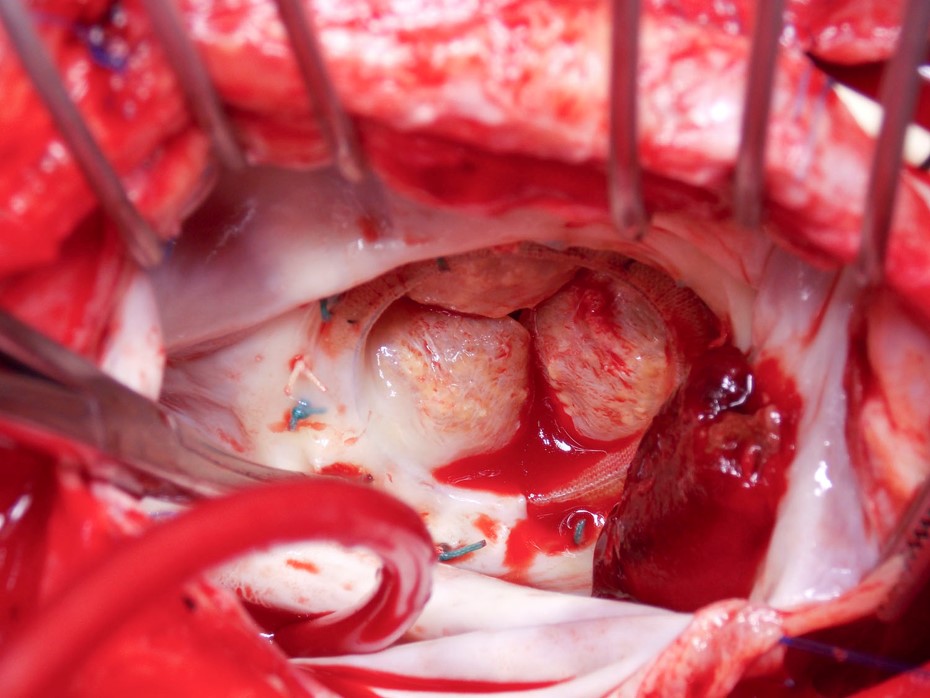
Por último, y quizás lo más controvertido, es si nuestro enfoque de la anticoagulación debe ser diferente para los pacientes que se han sometido a TAVR. La norma inicial ha sido tratar a estos pacientes con aspirina y clopidogrel porque éste fue el enfoque adoptado en los ensayos aleatorios. Más recientemente, con la angiografía por tomografía computarizada (ATC) cuatridimensional guiada por electrocardiografía, se ha descrito una reducción de la movilidad de las valvas de la válvula aórtica bioprotésica y un engrosamiento hipoatenuado de las valvas, lo que implica una trombosis valvular.17,18 A menudo, estos pacientes son asintomáticos y tienen gradientes Doppler normales en la ecocardiografía, lo que sugiere que estos hallazgos pueden ser subclínicos. Es importante destacar que estas anomalías de la ATC pueden resolverse con warfarina, y la falta de anticoagulación inicial está surgiendo como un posible factor de riesgo.19 En la actualidad, sin embargo, estos hallazgos de imagen no tienen una importancia clínica clara.20 Afortunadamente, se está llevando a cabo un ensayo aleatorio, GALILEO (Global Study Comparing a Rivaroxaban-Based Antithrombotic Strategy to an Antiplatelet-Based Strategy After Transcatheter Aortic Valve Replacement to Optimize Clinical Outcomes), que compara el rivaroxabán con el tratamiento antiplaquetario tras el TAVR, y que debería aportar información valiosa.21 Sin embargo, a pesar de que se estima que se han inscrito 1.520 pacientes, es posible que el ensayo no tenga la potencia adecuada para los eventos clínicos.
Conclusiones
En general, en los pacientes con válvulas bioprotésicas, los acontecimientos tromboembólicos tempranos no relacionados con el procedimiento son poco frecuentes. Además, la incidencia de trombosis valvular manifiesta es probablemente baja, y el efecto de la trombosis valvular subaguda sobre la durabilidad de la válvula aún se está definiendo. Dadas estas observaciones, junto con el mayor riesgo de hemorragia con la warfarina, abogamos por un enfoque selectivo de la anticoagulación postoperatoria (figura 3). Para los pacientes con válvulas aórticas bioprotésicas, está indicada la anticoagulación durante 3-6 meses en los pacientes con factores de riesgo establecidos, como la fibrilación auricular. Basándose en la reciente evidencia emergente, debe considerarse la anticoagulación y el seguimiento estrecho en pacientes con hallazgos ecocardiográficos o de ATC anormales, como un aumento inexplicable de los gradientes valvulares por Doppler o un engrosamiento hipoatenuado de las valvas. Por último, aunque se dispone de menos datos, los pacientes con válvulas mitrales bioprotésicas parecen tener un mayor riesgo de complicaciones trombóticas, y se recomienda la anticoagulación sistemática durante 3-6 meses.
Figura 3: Enfoque propuesto para la anticoagulación tras la sustitución de la válvula bioprotésica
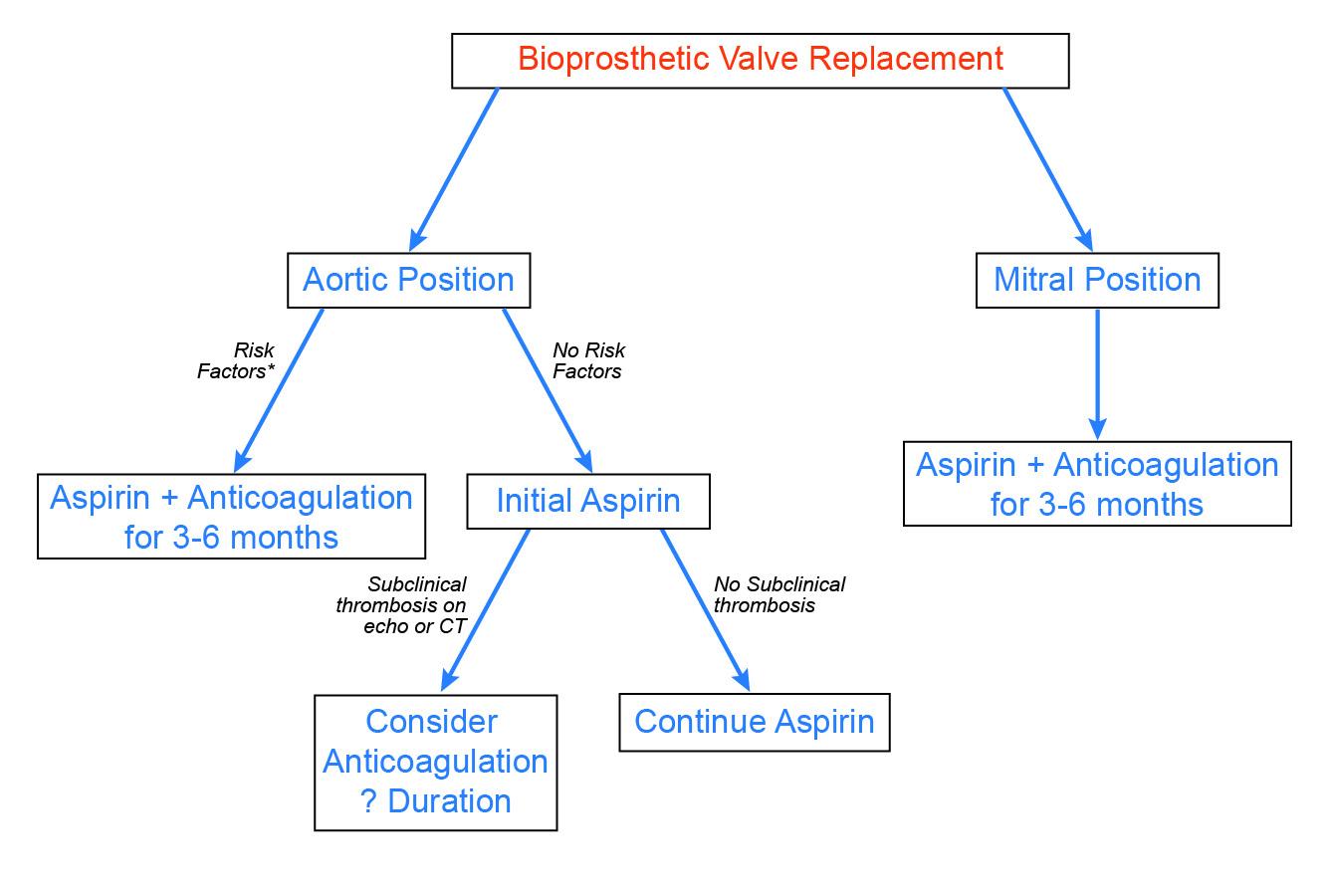
Este artículo contiene material educativo destinado a profesionales de la salud con licencia y está destinado a ser utilizado únicamente con fines educativos e informativos. Aunque el contenido puede versar sobre cuestiones médicas y de salud específicas, no sustituye ni reemplaza el asesoramiento médico personalizado y no está destinado a ser utilizado como única base para tomar decisiones médicas o de salud individualizadas. Los puntos de vista y las opiniones expresadas son los de los autores y editores que contribuyen a la publicación y no representan necesariamente las opiniones del ACC. El material no pretende presentar los únicos, o necesariamente mejores, métodos o procedimientos para las situaciones médicas abordadas, sino que pretende representar un enfoque, punto de vista, declaración u opinión.
- Pibarot P, Dumesnil JG. Válvulas cardíacas protésicas: selección de la prótesis óptima y manejo a largo plazo. Circulation 2009;119:1034-48.
- Mack MJ, Douglas PS, Holmes DR. Shedding More Light on Valve Thrombosis After Transcatheter Aortic Valve Replacement. J Am Coll Cardiol 2016;67:656-8.
- Heras M, Chesebro JH, Fuster V, et al. Alto riesgo de tromboembolismo temprano después del reemplazo de la válvula cardíaca bioprotésica. J Am Coll Caridol 1995;25:1111-9.
- Roudaut R, Serri K, Lafitte S. Thrombosis of prosthetic heart valves: diagnosis and therapeutic considerations. Heart 2007;93:137-42.
- Masri A, Gillinov AM, Johnston DM, et al. Anticoagulación frente a tratamiento antiplaquetario o sin tratamiento en pacientes sometidos a implantación de válvulas bioprotésicas: una revisión sistemática y un metaanálisis. Heart 2017;103:40-80.
- R Core Team (2015). R: Un lenguaje y entorno para la computación estadística. Fundación R para la computación estadística; Viena, Austria. Disponible en: https://www.R-project.org/. (Usando la función power.prop.test α = 0,05 y β = 0,8)
- Aramendi JI, Mestres CA, Martínez-León J, Campos V, Muñoz G, Navas C. Anticoagulación triflusal versus oral para la prevención primaria del tromboembolismo después del reemplazo de la válvula bioprotésica (trac): ensayo prospectivo, aleatorizado y cooperativo. Eur J Cardiothorac Surg 2005;27:854-60.
- Colli A, Mestres CA, Castella M, Gherli T. Comparing warfarin to aspirin (WoA) after aortic valve replacement with the St. Jude Medical Epic heart valve bioprosthesis: results of the WoA Epic pilot trial. J Heart Valve Dis 2007;16:667-71.
- Mérie C, Køber L, Skov Olsen P, et al. Asociación de la duración del tratamiento con warfarina tras el reemplazo de la válvula aórtica bioprotésica con el riesgo de mortalidad, complicaciones tromboembólicas y hemorragias. JAMA 2012;308:2118-25.
- Cremer PC, Rodríguez LL, Griffin BP, et al. Early Bioprosthetic Valve Failure: Mechanistic Insights via Correlation between Echocardiographic and Operative Findings. J Am Soc Echocardiogr 2015;28:1131-48.
- Brown ML, Park SJ, Sundt TM, Schaff HV. Riesgo de trombosis temprana en pacientes con válvulas biológicas en posición aórtica. J Thorac Cardiovasc Surg 2012;144:108-11.
- Nishimura RA, Otto CM, Bonow RO, et al. 2014 AHA/ACC guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol 2014;63:e57-185.
- Egbe AC, Pislaru SV, Pellikka PA, et al. Trombosis de la válvula bioprotésica frente a fallo estructural: Predictores clínicos y ecocardiográficos. J Am Coll Cardiol 2015;66:2285-94.
- Stewart WJ. Trombosis de las válvulas bioprotésicas: ¿Podemos permitirnos ignorarlo? J Am Coll Cardiol 2015;66:2295-7.
- Russo A, Grigioni F, Avierinos JF, et al. Complicaciones tromboembólicas tras la corrección quirúrgica de la regurgitación mitral incidencia, predictores e implicaciones clínicas. J Am Coll Cardiol 2008;51:1203-11.
- Butnaru A, Shaheen J, Tzivoni D, Tauber R, Bitran D, Silberman S. Diagnosis and treatment of early bioprosthetic malfunction in the mitral valve position due to thrombus formation. Am J Cardiol 2013;112:1439-44.
- Makkar RR, Fontana G, Jilaihawi H, et al. Possible Subclinical Leaflet Thrombosis in Bioprosthetic Aortic Valves. N Engj J Med 2015;373:2015-24.
- Pache G, Schoechlin S, Blanke P, et al. Engrosamiento temprano hipoatenuado de las valvas en válvulas cardíacas transcatéter expandibles con balón. Eur Heart J 2016;37:2263-71.
- Hansson NC, Grove EL, Andersen HR, et al. Trombosis de la válvula aórtica transcatéter: incidencia, factores predisponentes e implicaciones clínicas. J Am Coll Cardiol 2016;68:2059-69.
- Laschinger JC, Wu C, Ibrahim NG, Shuren JE. Reducción del movimiento de las hojas en las válvulas aórticas bioprotésicas: la perspectiva de la FDA. N Engj J Med 2015;373:1996-8.
- Estudio global que compara una estrategia antitrombótica basada en rivAroxaban con una estrategia basada en antipLatelet después de la sustitución de válvulas transcatéter para optimizar los resultados clínicos (GALILEO) (sitio web ClinicalTrails.gov). 2016. Disponible en: https://clinicaltrials.gov/ct2/show/NCT02556203. Consultado el 29/11/2016.
Temas clínicos: Manejo de la anticoagulación, Arritmias y PE clínica, Cirugía cardíaca, Insuficiencia cardíaca y miocardiopatías, Angiografía e intervención cardiovascular invasiva, Imagen no invasiva, Cardiopatía valvular, Manejo de la anticoagulación y fibrilación auricular, Fibrilación auricular/Arritmias supraventriculares, Cirugía Aórtica, Cirugía Cardíaca y Arritmias, Cirugía Cardíaca e Insuficiencia Cardíaca, Cirugía Cardíaca y EHV, Insuficiencia Cardíaca Aguda, Intervenciones e Imagen, Intervenciones y Cardiopatía Estructural, Angiografía, Ecocardiografía/Ultrasonido, Imagen Nuclear
Palabras clave: Válvula aórtica, Estenosis de la válvula aórtica, Fibrilación auricular, Aspirina, Bioprótesis, Estudios de casos y controles, Angiografía, Constricción, Patológica, Ecocardiografía, Transesofágica, Electrocardiografía, Insuficiencia cardíaca, Enfermedades de las válvulas cardíacas, Prótesis de la válvula cardíaca, Válvula mitral, Estenosis de la válvula mitral, Reoperación, Factores de riesgo, Accidente cerebrovascular, Suturas, Trombosis, Ticlopidina, Sustitución transcatéter de la válvula aórtica, Vitamina K, Warfarina
< Volver a los listados