Cyclopentan Kemiske egenskaber, anvendelser, produktion
Fysiske og kemiske egenskaber
Cyclopentan, også kendt som “pentamethylen”, er en slags cycloalkan med formlen C5H10. Det har en molekylvægt på 70,13. Det findes som en slags brændbar væske. Det har et smeltepunkt på 94,4 °C, et kogepunkt på 49,3 °C, en relativ massefylde på 0,7460 og et brydningsindeks på 1,4068. Det er opløseligt i alkohol, ether og carbonhydrider og er ikke opløseligt i vand. Cyklopentan er ikke en planar ring og har to konformationer: envelope-konformationer og semi-chair-konformationer. Vinkelen mellem kulstof-kulstof-kulstof-bindingsvinklen er tæt på 109 ° 28 ‘ med en molekylspænding, der ikke er stor, og ringen er relativt stabil. Den har samme kemiske egenskaber som alkaner. Den dødelige koncentration i luften for rotterne var 3,8 × 10-2. Det udviser en rødgul farve ved reaktion med svovlsyre, mens det danner nitrocyklopentan og glutarsyre ved reaktion med salpetersyre. Metode: Det kan fremstilles af petroleumseterdestillat ved højtrykskrakning af cyclohexan i tilstedeværelse af aluminium eller katalytisk hydrogenering af cyclopenten og cyclopentadien. Formål: anvendes hovedsagelig som opløsningsmiddel.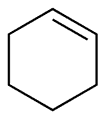

Figur 1 cyklopentanstrukturen.
Cykloalkan
Cycloalkaner er mættede carbonhydrider, hvor kulstofatomerne i molekylet er anbragt i en ring og et tilstrækkeligt antal hydrogenatomer er kombineret. Cycloalkaner, der forekommer i olie, er hovedsagelig cyclopentan og cyclohexan.
Cycloalkaner har et højere smeltepunkt, kogepunkt og relativ massefylde end de tilsvarende retkædede alkaner. Vi kan bruge den naphtheniske aromatiske råolie til at fremstille straight-run-benzin med høj oktan, hvis eksplosionsbeskyttelse er bedre end normal paraffin. Paraffinholdig naphthenisk råolie med lavt svovlindhold er ikke blot let at behandle, men også et fremragende råmateriale til fremstilling af avancerede smøremidler. Petroleum indeholdende relativt mange polycykliske naphtheniske forbindelser med lang sidekæde er et ideelt materiale til smøremidler af høj kvalitet.
Ved stuetemperatur og atmosfærisk tryk er cycloalkan indeholdende fire eller færre kulstofatomer i gasform med dem, der indeholder mere end fire kulstofatomer, der findes i flydende form. Cyclopropan og cyclobutan optræder som gas, cyclopentan til cycloundecan optræder som væske; cyclododecan og derover optræder som fast stof.
Cykloalkanens kemiske natur er relateret til antallet af kulstofatomer, der danner ringen. Det er benævnt tre- og fireleddet ring, som lille ring; den fem-syv-leddet ring som normal ring; den otte-elev-leddet ring som normal ring; den tolv-leddet ring og derover som stor ring. Kerne linjerne af kulstofkerner i små ringe er ikke i overensstemmelse med bindingsorbitalets akse. I cyclopropan er den ring, der dannes af kulstofatomernes kernelinjer, en ligesidet trekant, hvor hver vinkel er 60°, mens vinklen på sp3-hybridorbitalaksen for de enkeltbindinger mellem kulstof og kulstof, der dannes af hvert kulstof, er 104° (se figur 2 nedenfor). Derfor er det ikke lykkedes orbitten at opnå den største grad af overlapning, hvilket forårsager en stor vinkelspænding. Cyclobutan har også vinkelspænding, men er mindre. Dette fører til den lille rings ringe stabilitet, hvilket medfører, at den har samme kemiske egenskab som olefiner, der kan have en ringåbningsadditionsreaktion med mange reagenser. Den anden ring har mindre eller ingen vinkelspænding. Cykloalkan og alkaner har lignende kemiske egenskaber og er mindre tilbøjelige til at have en ringåbningsreaktion, f.eks. en reaktion med hydrogen. Cyclohexan og højere cycloalkan er vanskeligere at gennemgå hydrogenering.
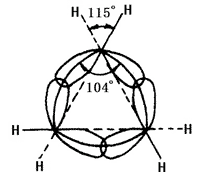
Figur 2 er en skematisk fremstilling af sp3-hybridiseringsorbitaloverlapning i cyclopropan.
Cyclopropan (ved stuetemperatur) og cyclobutan (ved opvarmningsbetingelserne) kan have additionsreaktion med halogen og hydrogenhalogenid.
Den åbne sløjfe opstår mellem de to atomer, der forbinder det mest og mindst antal hydrogen. Additionsreaktionen opfylder den markovske regel. Mens den normale ring, under stimulering af lys eller varme kan have substitutionsreaktion med halogen.
Ved stuetemperatur kan cycloalkan ikke oxideres af kaliumpermanganat.
Cyclopentan, cyclohexan og dets alkylsubstituerede produkter findes i visse petroleumolier. Cycloalkaner kan også syntetiseres ved passende metoder, såsom dihaloalkancyklisering og hydrogenering af aromatiske kulbrinter.
Denne information blev redigeret af Xiaonan fra Chemicalbook (2015-08-17).
Farlig situation
Indtagelse og indånding er moderat giftige. (2) Er brandfarlig med større risiko for forbrænding. Den tilladte koncentration i luft er 600ppm (1720mg/m3) i USA.
Skadelige virkninger og symptomer på forgiftning
Indånding af høje koncentrationer af cyclopentan kan forårsage hæmning af centralnervesystemet, selv om den akutte toksicitet er lav. Symptomer på akut eksponering omfatter først ophidselse, efterfulgt af fremkomsten af balanceforstyrrelser og endog bedøvelse, koma. Der er sjældent tilfælde af død på grund af respirationssvigt. Det er blevet rapporteret, at dyr, der fodres med denne vare, kan få alvorlig diarré, hvilket fører til hjerte-, lunge- og leverkarsammenbrud og hjernedegeneration.
Beskyttelsesforanstaltninger
Det kan bruges til at forbedre produktionsudstyret. Brug hudbeskyttelsescremer eller handsker til at beskytte huden.
Medicinsk pleje
Ved regelmæssig fysisk undersøgelse skal man være opmærksom på den potentielle irritationseffekt af hud og luftveje samt eventuelle komplikationer af nyre og lever.
Transportkrav
Brandfarlig væske af klasse I. Code of Hazard Regulations: 61013. Beholderen skal være mærket med et “brandfarlig væske”-mærke ved transport.
Brandslukningsmiddel
Se “cyclohexan”.
Anbefalede affaldsbortskaffelsesmetoder
Forbrænding;
Kemiske egenskaber
Den fremstår som farveløs væske med et smeltepunkt på-93,9 °C, et kogepunkt på 49,26 °C, en relativ massefylde på 0,7460 (20/4 °C), et brydningsindeks på 1,4068 og et flammepunkt på-37 °C. Det er blandbart med alkohol, ether og andre organiske opløsningsmidler, men er ikke let opløseligt i vand.
Anvendelser
(1) Det kan anvendes som opløsningsmiddel til opløsningspolymerisation af polyisoprengummi og celluloseether. Det kan anvendes som erstatning for Freon som isoleringsmateriale i køleskabe og frysere samt som skummidler til andre hårde PU-skum og kromatografiske analysestandarder.
(2) Anvendes som standardstof til kromatografisk analyse, opløsningsmidler, motorbrændstoffer, azeotropiske destillationsmidler.
Produktionsmetode
Cyklopentan er en bestanddel af petroleumsether i kogepunktsområdet 30-60 °C med et indhold på generelt 5%-10%. Anvend atmosfærisk destillation; ved et refluxforhold på 60:1 og udfør i et tårn med en højde på 8 m; destillation af isopentan og n-pentan; fortsæt fraktionering for at opnå en cyclopentan med en renhed på over 98 %. Cyclopentan kan også fremstilles ved cyclopentanonreduktion eller katalytisk hydrogenering af cyclopentadien.
Farer &Sikkerhedsoplysninger
Kategori Brandfarlige væsker
Toksicitetsklassificering: Lav toksicitet
Akut toksicitet: oral-rat LD50: 11400 mg/kg; oral-mus LD50: 12800 mg/kg
Farlig egenskab af eksplosivstoffer: eksplosivt ved blanding med luft
Brandfarlighed og farlige situationer: brandfarlig i tilfælde af brand, høj temperatur og oxidant med forbrænding, der frigiver irriterende røg
Lagringsegenskaber: Opbevaringsrum: ventileret, lav temperatur og tørt; opbevares sammen med oxidationsmiddel separat
Slukningsmiddel: Slukningsmiddel: Slukningsmiddel: Slukningsmiddel: Slukningsmiddel: Slukningsmiddel: Slukningsmiddel: Slukningsmiddel: Slukningsmiddel: Slukningsmiddel er ikke tilladt: Slukningsmiddel: Tørpulver, kuldioxid, skum, 1211-slukningsmiddel
Arbejdsmiljøstandard: Tørpulver, kuldioxid, skum, 1211-slukningsmiddel: TWA 1720 mg/m3; STEL 2150 mg/kg
Kemiske egenskaber
Farveløs væske med en benzinlignende lugt
Kemiske egenskaber
Cyklopentan er en farveløs væske.
Fysiske egenskaber
Farveløs, mobil, brandfarlig væske med en lugt, der ligner cyclohexan.
Anvendelser
Cyklopentan er et olieprodukt. Det dannes ved katalytisk krakning ved høj temperatur af cyclohexan eller ved reduktion af cyclopentadien. Det forekommer i petroleumsetherfraktioner og i mange kommercielle opløsningsmidler.Det anvendes som opløsningsmiddel til maling, til ekstraktion af voks og fedt og i skoindustrien.
Anvendelser
Som laboratoriereagens; til fremstilling af farmaceutiske produkter; findes i opløsningsmidler og i petroleumsether; drivmiddel til trykudvidelse.
Produktionsmetoder
Cyclopentan forekommer i petroleumsetherfraktioner og fremstilles ved krakning af cyclohexan i nærværelse af aluminiumoxid ved høj temperatur og højt tryk eller ved reduktion af cyclopentadien.
Definition
ChEBI: En cycloalkan, der består af fem kulstofatomer, som hver er bundet med to hydrogener over og under plan. Stamformen i klassen af cyclopentaner.
Generel beskrivelse
En klar farveløs væske med en petroleumlignende lugt. Flammepunkt på -35°F. Mindre tæt end vand og uopløselig i vand. Dampene er tungere end luft.
Luft &Vand Reaktioner
Meget letantændelig. Uopløseligt i vand.
Reaktivitetsprofil
CYCLOPENTAN er uforeneligt med stærke oxidationsmidler såsom klor, brom, fluor. .
Sundhedsfare
Indånding forårsager svimmelhed, kvalme og opkastning; koncentrerede dampe kan forårsage bevidstløshed og kollaps. Damp forårsager let svie i øjnene. Kontakt med væske forårsager irritation af øjnene og kan irritere huden, hvis den får lov til at forblive. Indtagelse forårsager irritation af maven. Aspiration giver alvorlig lungeirritation og hurtigt udviklende lungeødem; ophidselse af centralnervesystemet efterfulgt af depression.
Sundhedsfare
Cyclopentan er et lavt akut giftigt stof. Eksponering i høje koncentrationer kan medføre depression af centralnervesystemet med symptomer på excitabilitet, tab af ligevægt, stupor og koma. Der kan opstå åndedrætssvigt hos rotter efter 30-60 minutters eksponering for 100.000-120.000 ppm i luft. Det er irriterende for de øvre luftveje, hud og øjne. Der findes ingen oplysninger i litteraturen om de kroniske virkninger af langvarig eksponering for cyclopentan.
Brandfare
Adfærd i brand: Beholdere kan eksplodere.
Kemisk reaktivitet
Reaktivitet med vand Ingen reaktion; Reaktivitet med almindelige materialer: Ingen reaktion; Stabilitet under transport: Stabil; Neutraliseringsmidler for syrer og ætsende stoffer: Ikke relevant; Polymerisation: Ikke relevant; Inhibitor af polymerisation: Ikke relevant: Ikke relevant: Polymerisationsinhibitor: Ikke relevant.
Sikkerhedsprofil
Mildt giftig ved indtagelse og indånding. Høje koncentrationer har narkotisk virkning. En meget farlig brandfare, når den udsættes for varme eller flammer; kan reagere med oxidationsmidler. Brug skum, CO2, tørre kemikalier til at bekæmpe brand. Ved opvarmning til nedbrydning afgiver det ætsende røg og dampe.
Potentiel eksponering
Cyclopentan anvendes som opløsningsmiddel.
Kilde
Bestanddel af benzin med høj oktanværdi (citeret, Verschueren, 1983). Harley et al. (2000)analyserede headspace-dampene fra tre kvaliteter blyfri benzin, hvor ethanol var tilsat som erstatning for methyl-tert-butylether. Cyclopentan blev påvist i en identisk koncentration på 1,4 vægtprocent i headspace-dampene for almindelige, mellem- og premiumkvaliteter.
Schauer et al. (1999) rapporterede om cyclopentan i udstødningen fra en dieseldrevet medium-duty lastbil med en emissionsrate på 410 μg/km.
California Phase II reformuleret benzin indeholdt cyclopentan i en koncentration på 4,11 g/kg. Udstødningsemissioner i gasfasen fra benzindrevne biler med og uden katalytiske konvertere var henholdsvis 0,78 og 85,4 mg/km (Schauer et al., 2002).
Miljøets skæbne
Biologisk. Cyclopentan kan oxideres af mikrober til cyclopentanol, som kan oxideres til cyclopentanon (Dugan, 1972).
Photolytisk. Følgende hastighedskonstanter blev rapporteret for reaktionen af oktan og OH-radikaler i atmosfæren: 3,7 x 10-12 cm3/molekyle?sek ved 300 K (Hendry og Kenley, 1979); 5,40x 10-12 cm3/molekyle?sek (Atkinson, 1979); 4,83 x 10-12 cm3/molekyle?sek ved 298 K (DeMore ogBayes, 1999); 6,20 x 10-12, 5,24 x 10-12, og 4.43 x 10-12 cm3/molekyle?sek ved henholdsvis 298, 299 og 300 K (Atkinson, 1985), 5,16 x 10-12 cm3/molekyle?sek ved 298 K (Atkinson, 1990) og 5,02 x 10-12 cm3/mol-sek ved 295 K (Droege og Tilly, 1987).
Kemisk/fysisk. Cyclopentan vil ikke hydrolyseres, fordi det ikke har nogen hydrolyserbar funktionel gruppe. Komplet forbrænding i luft giver kuldioxid og vand.
Ved forhøjede temperaturer sker der brud på ringen, hvorved der dannes ethylen og formodentlig allene og hydrogen (Rice og Murphy, 1942).
Sending
UN1146 Cyclopentan, Fareklasse: 3; Etiketter: 3-Brandfarlig væske.
Rensningsmetoder
Frigør det fra cyclopenten ved to passager gennem en søjle af omhyggeligt tørret og afgaset aktiveret silicagel. Det forekommer i petroleum og er HØJT BRANDFARLIGT.
Inkompatibiliteter
Kan danne en eksplosiv blanding med luft.Kan akkumulere statiske elektriske ladninger og kan forårsage antændelse af dampene. Kontakt med stærke oxidationsmidler kan forårsage brand og eksplosion.
Bortskaffelse af affald
Opløs eller bland materialet med et brændbart opløsningsmiddel og brænd det i en kemisk forbrændingsovn udstyret med efterbrænder og skrubber. Alle føderale, statslige og lokale miljøregler skal overholdes.