Ciclopentan Proprietăți chimice, utilizări, producție
Proprietăți fizice și chimice
Ciclopentanul, cunoscut și sub numele de „pentametilenă”, este un tip de cicloalcan cu formula C5H10. Are o greutate moleculară de 70,13. Există ca un fel de lichid inflamabil. Are un punct de topire de 94,4 °C, un punct de fierbere de 49,3 °C, o densitate relativă de 0,7460 și un indice de refracție de 1,4068. Este solubilă în alcool, eter și hidrocarburi și nu este solubilă în apă. Ciclopentanul nu este un inel planar și are două conformații: conformația înveliș și conformația semicirculară. Unghiul de legătură carbon-carbon-carbon este apropiat de 109 ° 28 ‘, tensiunea moleculară nefiind mare și inelul fiind relativ stabil. Are o proprietate chimică similară cu cea a alcanilor. Concentrația letală în aer pentru șobolani a fost de 3,8 × 10-2. Prezintă o culoare galben-roșie la reacția cu acidul sulfuric fumant, generând în același timp nitrociclopentan și acid glutaric prin reacție cu acidul azotic. Metodă: poate fi obținut din distilate de eter de petrol, prin cracarea la presiune înaltă a ciclohexanului în prezența aluminiului sau prin hidrogenarea catalitică a ciclopentenului și a ciclopentadienei. Scopuri: se utilizează în principal ca solvent.
Figura 1 structura ciclopentanului.
Cicloalcană
Cicloalcanii sunt hidrocarburi saturate în care atomii de carbon din moleculă sunt dispuși într-un inel și în care sunt combinați un număr suficient de atomi de hidrogen. Cicloalcanii prezentați în petrol sunt în principal ciclopentanul și ciclohexanul.
Cicloalcanii au un punct de topire, un punct de fierbere și o densitate relativă mai mari decât alcanii corespunzători cu lanț drept. Putem folosi țițeiul aromatic naftenic pentru a produce benzină de rulare directă cu cifră octanică ridicată, antiexplozia sa fiind mai bună decât parafina normală. Petrolul brut naftenic parafină cu conținut scăzut de sulf nu este doar ușor de prelucrat, ci și o materie primă excelentă pentru producția de lubrifianți avansați. Petrolul care conține relativ mulți compuși naftenici policiclici cu lanț lateral lung este un material ideal pentru lubrifianți de înaltă calitate.
La temperatura camerei și la presiune atmosferică, cicloalcanii care conțin patru sau mai puțini atomi de carbon se află sub formă de gaz, cei care conțin mai mult de patru atomi de carbon existând sub formă lichidă. Ciclopropanul și ciclobutanul apar sub formă de gaz, ciclopentanul până la cicloundecan apare sub formă lichidă; ciclododecanul și mai sus apare sub formă solidă.
Natura chimică a cicloalcanului este legată de numărul de atomi de carbon care formează inelul. Se face referire la inelul cu trei membri și la inelul cu patru membri, ca inel mic; la inelul cu cinci până la șapte membri ca inel normal; la inelul cu opt-unsprezece membri ca inel normal; la inelul cu douăsprezece membri și mai sus ca inel mare. Liniile de nuclee ale nucleelor de carbon din inelele mici nu sunt în concordanță cu axa orbitalului de legătură. În ciclopropan, inelul format de liniile nucleelor atomilor de carbon este un triunghi echilateral, fiecare unghi fiind de 60°, în timp ce unghiul axei orbitalului hibrid sp3 al legăturilor simple carbon-carbon format de fiecare carbon este de 104° (a se vedea figura 2 de mai jos). Prin urmare, orbita nu a reușit să atingă cel mai mare grad de suprapunere, provocând o tensiune unghiulară mare. Ciclobutanul are, de asemenea, tensiune unghiulară, dar fiind mai mică. Acest lucru duce la stabilitatea slabă a inelului mic, cauzând proprietatea sa chimică similară cu cea a olefinelor care pot avea reacție de adiție cu deschidere de inel cu mulți reactivi. Celălalt inel are mai puțin sau deloc tensiune unghiulară. Cicloalcanii și alcanii au proprietăți chimice similare, fiind mai puțin predispuși la reacții de deschidere a inelului, cum ar fi reacția cu hidrogenul. Ciclohexanul și cicloalcanii superiori sunt mai greu de supus hidrogenării.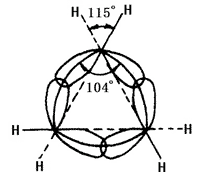
Figura 2 este o reprezentare schematică a suprapunerii orbitalilor de hibridizare sp3 în ciclopropan.
Ciclopropanul (la temperatura camerei) și ciclobutanul (în condiții de încălzire) pot avea reacții de adiție cu halogen și halogenură de hidrogen.
Ciclopropanul (la temperatura camerei) și ciclobutanul (în condiții de încălzire) pot avea reacții de adiție cu halogen și halogenură de hidrogen.
Bucleul deschis apare între cei doi atomi care leagă cel mai mare și cel mai mic număr de hidrogen. Adiția satisface regula markoviană. În timp ce inelul normal, sub stimularea luminii sau a căldurii poate avea reacție de substituție cu halogenul.
La temperatura camerei, cicloalcanul nu poate fi oxidat de permanganatul de potasiu.
Ciclopentanul, ciclohexanul și produsele sale substituite cu alchil sunt prezentate în anumite uleiuri petroliere. Cicloalcanii pot fi, de asemenea, sintetizați prin metode adecvate, cum ar fi ciclizarea dihaloalcanilor și hidrogenarea hidrocarburilor aromatice.
Această informație a fost editată de Xiaonan din Chemicalbook (2015-08-17).
Situație periculoasă
Ingestia și inhalarea sunt moderat toxice. (2) Fiind inflamabil, cu risc mai mare de ardere. Concentrația admisibilă în aer este de 600ppm (1720mg/m3) în Statele Unite.
Efecte nocive și simptome de otrăvire
Inhalarea unor concentrații mari de ciclopentan poate provoca inhibarea sistemului nervos central, deși toxicitatea sa acută este scăzută. Simptomele expunerii acute includ excitare la început, urmată de apariția tulburărilor de echilibru și chiar stupoare, comă. Rare sunt cazurile de deces datorate insuficienței respiratorii. S-a raportat că animalele hrănite cu această marfă pot face diaree severă, ceea ce duce la colaps vascular cardiac, pulmonar și hepatic și la degenerare cerebrală.
Măsuri de protecție
Poate fi folosit pentru îmbunătățirea echipamentului de producție. Folosiți creme de protecție a pielii sau mănuși pentru a proteja pielea.
Îngrijire medicală
La examinarea fizică periodică, acordați atenție efectului potențial de iritare a pielii și a tractului respirator, precum și oricăror complicații ale rinichilor și ficatului.
Condiții de transport
Lichid inflamabil de gradul I. Codul de reglementări privind riscurile: 61013. Recipientul trebuie să fie marcat cu un marcaj „lichid inflamabil” la transport.
Agent de stingere a incendiilor
A se vedea „ciclohexan”.
Metode recomandate de eliminare a deșeurilor
Incinerare;
Proprietăți chimice
Se prezintă sub formă de lichid incolor cu punctul de topire de-93,9 °C, punctul de fierbere de 49,26 ° C, densitatea relativă de 0,7460 (20/4 ° C), indicele de refracție de 1,4068 și punctul de inflamabilitate de-37 °C. Este miscibil cu alcoolul, eterul și alți solvenți organici, nefiind ușor de dizolvat în apă.
Utilizări
(1) Poate fi utilizat ca solvent pentru polimerizarea în soluție a cauciucului de poliizopren și a eterului de celuloză. Poate fi folosit ca substitut al freonului ca material de izolație în frigidere și congelatoare, precum și ca agent de spumare pentru alte spume dure de PU și ca etalon pentru analize cromatografice.
(2) Se folosește ca substanță etalon pentru analize cromatografice, solvenți, combustibili pentru motoare, agenți de distilare azeotropică.
Metoda de obținere
Ciclopentanul este un component al eterului de petrol în intervalul de punct de fierbere de 30-60 °C, conținutul fiind în general de 5%-10%. Se aplică distilarea atmosferică; la un raport de reflux de 60: 1 și se efectuează într-un turn de 8 m înălțime; se distilează mai întâi izopentanul și n-pentanul; se continuă fracționarea pentru a obține un ciclopentan cu o puritate de peste 98%. Ciclopentanul poate fi obținut, de asemenea, prin reducerea ciclopentanonei sau prin hidrogenarea catalitică a ciclopentadienei.
Pericole & Informații privind siguranța
Categoria Lichide inflamabile
Clasificarea toxicității: Toxicitate scăzută
Toxicitate acută: LD50 oral-șobolan: 11400 mg/kg; LD50 oral-șoarece: 12800 mg/kg
Proprietatea periculoasă a explozibililor: fiind exploziv în amestec cu aerul
Inflamabilitate și situații periculoase: fiind inflamabil în caz de incendiu, temperatură ridicată și oxidant, cu combustie care degajă fum iritant
Caracteristici de depozitare: Depozit: ventilat, la temperatură scăzută și uscat; Se depozitează separat cu oxidant
Agent de stingere: Pulbere uscată, dioxid de carbon, spumă, agent de stingere 1211
Standard ocupațional: TWA 1720 mg/m3; STEL 2150 mg/kg
Proprietăți chimice
Lichid incolor cu miros asemănător petrolului
Proprietăți chimice
Ciclopentanul este un lichid incolor.
Proprietăți fizice
Lichid incolor, mobil, inflamabil, cu un miros asemănător cu cel al ciclohexanului.
Utilizări
Ciclopentanul este un produs petrolier. Se formează din cracarea catalitică la temperaturi înalte a ciclohexanului sau prin reducerea ciclopentadienei. Se găsește în fracțiuni de eter de petrol și în mulți solvenți comerciali. este utilizat ca solvent pentru vopsele, în extracția cerii și a grăsimilor și în industria încălțămintei.
Utilizări
Ca reactiv de laborator; la fabricarea produselor farmaceutice; se găsește în solvenți și în eterul de petrol; agent de presurizare a propulsoarelor.
Metode de obținere
Ciclopentanul se găsește în fracțiuni de eter de petrol și estepreparat prin cracarea ciclohexanului în prezența aluminei la temperaturi și presiuni ridicate sau prin reducerea ciclopentadienei.
Definiție
ChEBI: Un cicloalcan care constă din cinci atomi de carbon, fiecare legat cu doi hidrogeni deasupra și dedesubtul planului. Este părintele clasei de ciclopentanuri.
Descriere generală
Lichid limpede și incolor cu miros asemănător cu cel de petrol. Punct de inflamabilitate de -35°F. Mai puțin dens decât apa și insolubil în apă. Vaporii sunt mai grei decât aerul.
Aer & Reacții cu apa
Foarte inflamabil. Insolubil în apă.
Profil de reactivitate
CICLOPENTANUL este incompatibil cu agenții oxidanți puternici, cum ar fi clorul, bromul, fluorul .
Pericol pentru sănătate
Inhalarea provoacă amețeli, greață și vărsături; vaporii concentrați pot provoca pierderea cunoștinței și colapsul. Vaporii provoacă ușoare usturimi ale ochilor. Contactul cu lichidul provoacă iritarea ochilor și poate irita pielea dacă se lasă să rămână. Ingerarea provoacă iritarea stomacului. Aspirația produce iritarea severă a plămânilor și un edem pulmonar cu dezvoltare rapidă; excitare a sistemului nervos central urmată de depresie.
Pericol pentru sănătate
Ciclopentanul este un toxic slab acut. Expunerea la concentrații mari poate produce depresie a sistemului nervos central cu simptome de excitabilitate, pierdere a echilibrului, stupoare și comă. Insuficiența respiratorie poate apărea la șobolani după 30-60 de minute de expunere la 100.000-120.000 ppm în aer. Este un iritant pentru tractul respirator superior, piele și ochi. Nu există informații disponibile în literatura de specialitate cu privire la efectele cronice ale expunerii prelungite la ciclopentan.
Pericol de incendiu
Comportament în caz de incendiu: Containerele pot exploda.
Reactivitate chimică
Reactivitate cu apa Nici o reacție; Reactivitate cu materiale comune: Nici o reacție; Stabilitate în timpul transportului: Stabil; Agenți de neutralizare pentru acizi și substanțe caustice: Nu este relevant; Polimerizare: Nu este relevant; Inhibitor de polimerizare: Nu este relevant.
Profil de siguranță
Ușor toxic prin ingestie și inhalare. Concentrațiile mari au acțiune narcotică. Un risc de incendiu foarte periculos atunci când este expus la căldură sau flacără; poate reacționa cu oxidanții. Pentru combaterea incendiilor, folosiți spumă, CO2, substanțe chimice uscate. Când este încălzit până la descompunere, emite fum și vapori acrișori.
Expunere potențială
Ciclopentanul este utilizat ca solvent.
Sursa
Component al benzinei cu cifră octanică ridicată (citat, Verschueren, 1983). Harley et al. (2000)au analizat vaporii din spațiul de cap a trei calități de benzină fără plumb în care s-a adăugat etanol pentru a înlocui metil terț-butil eterul. Ciclopentanul a fost detectat la o concentrație identică de 1,4 % în greutate în vaporii din spațiul de cap pentru clasele obișnuită, medie și premium.
Schauer et al. (1999) au raportat prezența ciclopentanului în gazele de eșapament ale unui camion diesel de capacitate medie la o rată de emisie de 410 μg/km.
California Phase II benzină reformulată conținea ciclopentan la o concentrație de 4,11g/kg. Ratele de emisie la țeava de eșapament în fază gazoasă a automobilelor alimentate cu benzină cu și fără convertizoare catalitice au fost de 0,78 și, respectiv, 85,4 mg/km (Schauer et al., 2002).
Destinul mediului
Biologic. Ciclopentanul poate fi oxidat de microbi la ciclopentanol, care se poate oxida la ciclopentanonă (Dugan, 1972).
Fotolitic. Au fost raportate următoarele constante de viteză pentru reacția octanului și a radicalilor OH în atmosferă: 3,7 x 10-12 cm3/moleculă?sec la 300 K (Hendry și Kenley, 1979); 5,40x 10-12 cm3/moleculă?sec (Atkinson, 1979); 4,83 x 10-12 cm3/moleculă?sec la 298 K (DeMore șiBayes, 1999); 6,20 x 10-12, 5,24 x 10-12 și 4,20 x 10-12, 5,24 x 10-12, și 4,20 x 10-12 la 298 K (DeMore șiBayes, 1999).43 x 10-12 cm3/mol-sec la 298, 299 și, respectiv, 300 K (Atkinson, 1985), 5,16 x 10-12 cm3/mol-sec la 298 K (Atkinson, 1990) și 5,02x 10-12 cm3/mol-sec la 295 K (Droege și Tilly, 1987).
Chimie/Fizică. Ciclopentanul nu se hidrolizează deoarece nu are nicio grupă funcțională hidrolizabilă. Arderea completă în aer produce dioxid de carbon și apă.
La temperaturi ridicate, are loc ruperea inelului, formându-se etilenă și, probabil, alenăși hidrogen (Rice și Murphy, 1942).
Expediție
UN1146 Ciclopentan, Clasa de pericol: 3; Etichete: 3-Lichid inflamabil.
Metode de purificare
Se eliberează de ciclopenten prin două treceri printr-o coloană de silicagel activat atent uscat și degazat. Se găsește în petrol și este FOARTE INFLAMABIL.
Incompatibilități
Poate forma un amestec exploziv cu aerul. poate acumula sarcini electrice statice și poate provoca aprinderea vaporilor săi. Contactul cu oxidanți puternici poate provoca incendii și explozii.
Eliminarea deșeurilor
Dizolvați sau amestecați materialul cu un solvent combustibil și ardeți-l într-un incinerator chimic echipat cu postcombustie și epurator. Trebuie respectate toate reglementările de mediu federale, de stat și locale.