Ciclopentano Propriedades Químicas,Usos,Produção
Propriedades Físicas e Químicas
Ciclopentano, também conhecido como “pentametileno”, é uma espécie de cicloalcano com a fórmula de C5H10. Tem um peso molecular de 70,13. Existe como uma espécie de líquido inflamável. Tem um ponto de fusão – 94,4 °C, ponto de ebulição de 49,3 °C, densidade relativa de 0,7460 e índice de refração de 1,4068. É solúvel em álcool, éter e hidrocarbonetos e não é solúvel em água. O ciclopentano não é um anel plano e tem duas conformações: as conformações do envelope e as conformações da semicadeira. O ângulo de ligação carbono-carbono é próximo de 109 ° 28 ‘ com a tensão molecular não grande e o anel sendo relativamente estável. Tem uma propriedade química semelhante aos alcanos. A concentração letal no ar para os ratos era de 3,8 × 10-2. Ele exibe cor vermelho-amarelada ao ter reação com ácido sulfúrico fumante enquanto gera nitro ciclopentano e ácido glutárico através de reação com ácido nítrico. Método: pode ser obtido a partir do destilado de éter de petróleo, através do craqueamento a alta pressão do ciclo-hexano na presença de alumínio ou hidrogenação catalítica do ciclopenteno e ciclopentadieno. Finalidades: utilizado principalmente como solvente.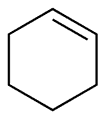
Figure 1 a estrutura do ciclopentano.
Cicloalcano
Cicloalcanos são hidrocarbonetos saturados nos quais os átomos de carbono na molécula estão dispostos em anel e um número suficiente de átomos de hidrogênio são combinados. Cicloalcanos apresentados no petróleo são principalmente ciclopentano e ciclohexano.
Cicloalcanos têm um ponto de fusão, ponto de ebulição e densidade relativa maiores do que os alcanos de cadeia reta correspondentes. Podemos utilizar o óleo cru aromático naftênico para produzir gasolina de cadeia linear de alto octano, sendo a sua antiexplosão melhor do que a parafina normal. O óleo naftênico parafínico de baixo teor de enxofre não só é fácil de processar como também é uma excelente matéria-prima para a produção de lubrificantes avançados. O petróleo contendo relativamente muitos compostos naftênicos policíclicos de cadeia longa é um material ideal para lubrificantes de alta qualidade.
A temperatura ambiente e pressão atmosférica, o cicloalcano contendo quatro ou menos átomos de carbono está na forma gasosa com aqueles contendo mais de quatro carbonos existentes na forma líquida. O ciclopropano e o ciclobutano aparecem como gás, o ciclopentano ao cicloundecano aparece como líquido; o ciclododecano e acima aparece como sólido.
A natureza química do cicloalcano está relacionada com o número de átomos de carbono que formam o anel. É referido como anel de três e quatro membros, como anel pequeno; o anel de cinco a sete membros como anel normal; o anel de oito e onze membros como anel normal; o anel de doze membros e acima como anel grande. As linhas de núcleos de núcleos de carbono em anéis pequenos não são consistentes com o eixo de ligação orbital. Em ciclopropano, o anel formado pelas linhas de núcleos de átomos de carbono é um triângulo equilátero com cada ângulo sendo 60°, enquanto o ângulo do eixo orbital híbrido sp3 de ligações simples carbono-carbono formado por cada 104° de carbono (ver figura 2 abaixo). Portanto, a órbita não conseguiu atingir o maior grau de sobreposição, causando uma grande tensão angular. O ciclobutano também tem tensão angular, mas sendo menor. Isto leva à má estabilidade do anel pequeno, causando sua propriedade química similar às olefinas que podem ter reação de adição de anéis de abertura com muitos reagentes. Outros anéis não têm menos tensão angular. Cicloalcanos e alcanos têm propriedades químicas semelhantes, menos propensos a ter reação de abertura de anéis, como a reação com hidrogênio. Ciclohexano e cicloalcano superior é mais difícil de sofrer hidrogenação.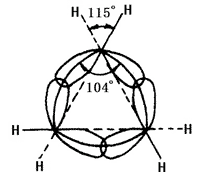
Figure 2 é uma representação esquemática da sobreposição orbital de hibridação sp3 em ciclopropano.
Ciclopropano (à temperatura ambiente) e ciclobutano (nas condições de aquecimento) podem ter reação de adição com halogênio e halogeneto de hidrogênio.
O ciclo aberto ocorre entre os dois átomos conectando o maior e o menor número de hidrogênio. A adição satisfaz a regra de Markovian. Enquanto o anel normal, sob a estimulação da luz ou calor pode ter reação de substituição com o halogênio.
A temperatura ambiente, o cicloalcano não pode ser oxidado por permanganato de potássio.
Ciclopentano, ciclohexano e seus produtos de substituição alquílica são apresentados em certos óleos de petróleo. Cicloalcanos também podem ser sintetizados por métodos adequados, como a ciclagem do dihaloalcano e a hidrogenação dos hidrocarbonetos aromáticos.
Esta informação foi editada por Xiaonan da Chemicalbook (2015-08-17).
Situação perigosa
Ingestão e inalação são moderadamente tóxicas. (2) Sendo inflamáveis com maior risco de combustão. A concentração admissível no ar é de 600ppm (1720mg/m3) nos Estados Unidos.
Efeitos prejudiciais e sintomas de envenenamento
A inalação de altas concentrações de ciclopentano pode causar inibição do sistema nervoso central, embora a sua toxicidade aguda seja baixa. Sintomas de exposição aguda incluem excitação no início, seguida pelo surgimento de distúrbios de equilíbrio, e até mesmo estupor, coma. Raramente há casos de morte devido a insuficiência respiratória. Tem sido relatado que animais alimentados com estes bens podem ter diarréia severa, levando ao colapso vascular do coração, pulmão e fígado e à degeneração cerebral.
Medidas de protecção
Pode ser usado para melhorar o equipamento de produção. Use cremes ou luvas protectoras da pele para proteger a pele.
Cuidados médicos
Ao exame físico regular, preste atenção ao potencial efeito irritante da pele e do tracto respiratório, assim como a quaisquer complicações dos rins e do fígado.
Requisitos de transporte
Líquido inflamável de grau I. Regulamento do Código de Perigos: 61013. O recipiente deve ser marcado com a marca “líquido inflamável” no transporte.
Agente extintor de incêndio
Ver “ciclohexano”.
Métodos recomendados de eliminação de resíduos
Incineração;
Propriedades químicas
Aparece como líquido incolor com um ponto de fusão de -93,9 °C, o ponto de ebulição de 49,26 °C, a densidade relativa de 0,7460 (20/4 °C), o índice de refracção de 1,4068 e o ponto de inflamação de -37 °C. É miscível com álcool, éter e outros solventes orgânicos, não sendo fácil de ser dissolvido em água.
Usos
(1) Pode ser utilizado como solvente para polimerização em solução de borracha de poliisopreno e éter de celulose. Pode ser utilizado como substituto do Freon como material isolante em frigoríficos e congeladores, bem como agentes espumantes para outras espumas duras de PU, e normas de análise cromatográfica.
(2) Utilizado como substância padrão para análise cromatográfica, solventes, combustíveis para motores, agentes de destilação azeotrópicos.
Método de produção
O ciclopentano é um componente do éter de petróleo na faixa de 30-60 °C do ponto de ebulição, sendo o conteúdo geralmente de 5%-10%. Aplicar a destilação atmosférica; a uma razão de refluxo de 60: 1 e realizar a uma torre de 8m de altura; primeiro destilar o isopentano e n-pentano; continuar o fraccionamento para obter um ciclopentano com uma pureza superior a 98%. O ciclopentano também pode ser obtido através da redução da ciclopentanona ou da hidrogenação catalítica do ciclopentadieno.
Perigos &Informações de segurança
Categoria Líquidos inflamáveis
Classificação de toxicidade: Baixa toxicidade
Toxicidade aguda: oral-rato LD50: 11400 mg/kg; oral-rato LD50: 12800 mg/kg
Propriedade precária dos explosivos: ser explosivo em mistura com o ar
Flamabilidade e situações perigosas: ser inflamável em caso de incêndio, alta temperatura e oxidante com combustão libertando fumo irritante
Características de armazenamento: Armazém: ventilado, a baixa temperatura e seco; Armazenar com oxidante separadamente
Agente extintor: Pó seco, dióxido de carbono, espuma, 1211 agente extintor
Padrão de extinção: TWA 1720 mg/m3; STEL 2150 mg/kg
Propriedades Químicas
Líquido incolor com odor a gasolina
Propriedades Químicas
Ciclopentano é um líquido incolor.
Propriedades físicas
Líquido incolor, móvel, inflamável com um odor parecido com o ciclohexano.
Usos
O ciclopentano é um produto petrolífero. É formado a partir do catalisador de alta temperatura do ciclo-hexano ou por redução do ciclopentadieno. Ocorre em eterfrações de petróleo e em muitos solventes comerciais. É utilizado como solvente para tintas, na extração de ceras e gorduras e na indústria de calçados.
Usos
Como reagente de laboratório; na fabricação de produtos farmacêuticos; encontrado em solventes e em éter de petróleo; agente pressurizante de propelente.
Métodos de produção
O ciclopentano ocorre em frações de éter de petróleo e é preparado pelo craqueamento do ciclo-hexano na presença de alumina a alta temperatura e pressão ou pela redução do ciclopentadieno.
Definição
ChEBI: Um cicloalcano que consiste em cinco carbonos cada um colado com dois hidrogênios acima e abaixo do plano. O pai da classe dos ciclopentanos.
Descrição Geral
Um líquido incolor claro com um odor a petróleo. Ponto de fulgor de -35°F. Menos denso que a água e insolúvel na água. Os vapores são mais pesados que o ar.
Air &Reacções na água
Altamente inflamável. Insolúveis em água.
Perfil de reatividade
CICLOPENTANO é incompatível com agentes oxidantes fortes, como cloro, bromo, flúor…
Perigo de saúde
A inalação causa tonturas, náuseas e vómitos; o vapor concentrado pode causar inconsciência e colapso. O vapor causa uma ligeira esperteza dos olhos. O contacto com líquidos causa irritação dos olhos e pode irritar a pele se for permitida a sua permanência. A ingestão causa irritação no estômago. A aspiração produz irritação pulmonar grave e edema pulmonar em rápido desenvolvimento; excitação do sistema nervoso central seguida de depressão.
Perigo para a saúde
O ciclopentano é um tóxico de baixa acidez. Sua exposição em altas concentrações pode produzir depressão do sistema nervoso central com sintomas de excitabilidade, perda de equilíbrio, estupor e coma. A falha respiratória pode ocorrer em ratos de 30-60 minutos de exposição a 100.000-120.000 ppm no ar. É anirritante para o trato respiratório superior, pele e olhos. Não há informações disponíveis na literatura sobre os efeitos crônicos da exposição prolongada ao ciclopentano.
Perigo de Incêndio
Comportamento em Incêndio: Os recipientes podem explodir.
Reactividade química
Reactividade com água Sem reacção; Reactividade com materiais comuns: Sem reacção; Estabilidade durante o transporte: Estável; Agentes Neutralizantes para Ácidos e Cáusticos: Não pertinente; Polimerização: Não pertinente; Inibidor da Polimerização: Não pertinente.
Perfil de Segurança
Ligeiramente tóxico por ingestão e inalação. Altas concentrações têm ação narcótica. Um risco de incêndio muito perigoso quando exposto ao calor ou à chama; pode reagir com oxidantes. Para combater o fogo, usar espuma, CO2, produtos químicos secos. Quando aquecido para decomposição, emite fumos e fumos acre.
Potencial Exposição
O ciclopentano é usado como solvente.
Fonte
Componente da gasolina de alta octanagem (citado, Verschueren, 1983). Harley et al. (2000) analisaram os vapores de headspace de três graus de gasolina sem chumbo, onde o etanol foi adicionado para substituir o éter metilterbutílico. O ciclopentano foi detectado em uma concentração idêntica de 1,4 wt% nos vapores de headspace para graus regulares, médios e premium.
Schauer et al. (1999) reportaram ciclopentano em uma taxa de emissão de atan de exaustão de caminhões movidos a diesel de média potência de 410 μg/km.
Califórnia Fase II reformulada da gasolina continha ciclopentano em uma concentração de 4,11g/kg. As taxas de emissão de gases de escape de automóveis movidos a gasolina com e sem catalisadores foram de 0,78 e 85,4 mg/km, respectivamente (Schauer et al., 2002).
Environmental Fate
Biological. O ciclopentano pode ser oxidado por micróbios a ciclopentanol, que pode oxidar a tociclopentanona (Dugan, 1972).
Fotolítico. As seguintes constantes de taxa foram relatadas para a reação de octanas e OHradicais na atmosfera: 3,7 x 10-12 cm3/molecule?sec a 300 K (Hendry e Kenley, 1979); 5,40 x 10-12 cm3/molecule?sec (Atkinson, 1979); 4,83 x 10-12 cm3/molecule?sec a 298 K (DeMore andBayes, 1999); 6,20 x 10-12, 5,24 x 10-12, e 4.43 x 10-12 cm3/molécula?sec a 298 K, 299, e 300 K,respectivamente (Atkinson, 1985), 5,16 x 10-12 cm3/molécula?sec a 298 K (Atkinson, 1990), e 5,02x 10-12 cm3/mol-sec a 295 K (Droege e Tilly, 1987).
Chemical/Physical. O ciclopentano não irá hidrolisar porque não tem grupo funcional hidrolisável. A combustão completa no ar produz dióxido de carbono e água.
A temperaturas elevadas, ocorre a ruptura do anel formando etileno e presumivelmente alene e hidrogênio (Rice and Murphy, 1942).
Transporte
UN1146 Ciclopentano, Classe de Perigo: 3; Rótulos:3-Líquido inflamável.
Métodos de purificação
Libertar do ciclopenteno por duas passagens através de uma coluna de sílica gel activada cuidadosamente seca e desgaseificada. Ocorre no petróleo e é ALTAMENTE INFLAMÁVEL.
Incompatibilidades
Pode formar mistura explosiva com o ar. Pode acumular cargas elétricas estáticas, e pode causar a ignição de seus vapores. O contacto com oxidantes fortes pode provocar fogo e explosão.
Descarte de resíduos
Dissolver ou misturar o material com um solvente combustível e queimar num incinerador químico equipado com um pós-combustão e um purificador. Todos os regulamentos ambientais federais, estaduais e locais devem ser observados.