Właściwości chemiczne cyklopentanu, zastosowania, produkcja
Właściwości fizyczne i chemiczne
Cyklopentan, znany również jako „pentametylen”, jest rodzajem cykloalkanu o wzorze C5H10. Jego masa cząsteczkowa wynosi 70,13. Występuje jako rodzaj łatwopalnej cieczy. Ma temperaturę topnienia-94,4 °C, temperaturę wrzenia 49,3 °C, gęstość względną 0,7460 i współczynnik załamania światła 1,4068. Jest rozpuszczalny w alkoholu, eterze i węglowodorach, nie rozpuszcza się w wodzie. Cyklopentan nie jest pierścieniem planarnym i ma dwie konformacje: konformacje otoczki i konformacje półłańcuchowe. Kąt wiązania węgiel-węgiel jest zbliżony do 109 ° 28 ’, przy czym napięcie molekularne nie jest duże, a pierścień jest stosunkowo stabilny. Ma podobne właściwości chemiczne jak alkany. Śmiertelne stężenie w powietrzu dla szczurów wynosiło 3,8 × 10-2. Wykazuje czerwono-żółte zabarwienie w reakcji z dymiącym kwasem siarkowym, natomiast w reakcji z kwasem azotowym wytwarza nitrocyklopentan i kwas glutarowy. Metoda: można go otrzymać z destylatu eteru naftowego, poprzez wysokociśnieniowy kraking cykloheksanu w obecności glinu lub katalityczne uwodornienie cyklopentenu i cyklopentadienu. Zastosowanie: głównie stosowany jako rozpuszczalnik.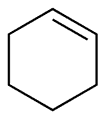
Rysunek 1 struktura cyklopentanu.
Cykloalkany
Cykloalkany to węglowodory nasycone, w których atomy węgla w cząsteczce ułożone są w pierścień i połączona jest z nimi odpowiednia liczba atomów wodoru. Cykloalkany występujące w ropie naftowej to głównie cyklopentan i cykloheksan.
Cykloalkany mają wyższą temperaturę topnienia, temperaturę wrzenia i gęstość względną niż odpowiadające im alkany o prostym łańcuchu. Możemy wykorzystać naftenową ropę aromatyczną do produkcji wysokooktanowej benzyny o prostym przebiegu, której właściwości przeciwwybuchowe są lepsze niż w przypadku zwykłej parafiny. Niska zawartość siarki parafinowa naftenowa ropa naftowa, jest nie tylko łatwa w obróbce, ale również jest doskonałym surowcem do produkcji zaawansowanych środków smarnych. Ropa naftowa zawierająca stosunkowo dużo wielopierścieniowych związków naftenowych o długim łańcuchu bocznym jest idealnym materiałem do produkcji wysokiej jakości smarów.
W temperaturze pokojowej i pod ciśnieniem atmosferycznym, cykloalkan zawierający cztery lub mniej atomów węgla jest w postaci gazu z tymi zawierającymi więcej niż cztery węgle istniejące w postaci ciekłej. Cyklopropan i cyklobutan występują jako gaz, cyklopentan do cykloundekanu występuje jako ciecz; cyklododekan i powyżej występuje jako ciało stałe.
Charakter chemiczny cykloalkanu jest związany z liczbą atomów węgla tworzących pierścień. Jest on określony trzy-członowy pierścień i cztery-członowy pierścień, jako mały pierścień; pięć do siedmiu-członowy pierścień jako normalny pierścień; osiem-eleven pierścień jako normalny pierścień; dwanaście-członowy pierścień i powyżej jako duży pierścień. Linie jąder atomów węgla w małych pierścieniach nie są zgodne z osią orbitali wiążących. W cyklopropan, pierścień utworzony przez linie jąder atomów węgla jest trójkąt równoboczny z każdym kątem 60 °, podczas gdy kąt osi orbitalu hybrydowego sp3 wiązań pojedynczych węgiel-węgiel utworzonych przez każdego węgla 104 ° (patrz rysunek 2 poniżej). W związku z tym, orbital nie udało się osiągnąć największy stopień nakładania się, powodując duże napięcie kątowe. Cyklobutan również ma napięcie kątowe, ale jest mniejsze. Prowadzi to do słabej stabilności małego pierścienia, powodując jego podobne właściwości chemiczne do olefin, które mogą mieć reakcję addycji z otwarciem pierścienia z wieloma reagentami. Inne pierścienie mają mniejsze lub żadne napięcie kątowe. Cykloalkany i alkany mają podobne właściwości chemiczne, mniej podatne na reakcje otwierania pierścieni, takie jak reakcja z wodorem. Cykloheksan i wyższe cykloalkany trudniej ulegają uwodornieniu.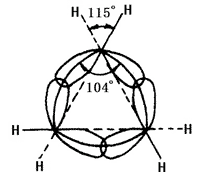
Rysunek 2 jest schematycznym przedstawieniem nakładania się orbitali hybrydyzacji sp3 w cyklopropanie.
Cykloheksan (w temperaturze pokojowej) i cyklobutan (w warunkach ogrzewania) mogą mieć reakcję addycji z halogenem i halogenkiem wodoru.
Pętla otwarta zachodzi pomiędzy dwoma atomami łączącymi największą i najmniejszą liczbę wodoru. Dodanie spełnia regułę Markovian. Podczas gdy normalny pierścień, pod wpływem światła lub ciepła może mieć reakcji substytucji z halogen.
W temperaturze pokojowej, cykloalkan nie może być utlenione przez nadmanganian potasu.
Cyklopentan, cykloheksan i jego alkilowe podstawione produkty są przedstawione w niektórych olejów ropy naftowej. Cykloalkany mogą być również syntetyzowane odpowiednimi metodami, takimi jak cyklizacja dihaloalkanów i uwodornienie węglowodorów aromatycznych.
Ta informacja została zredagowana przez Xiaonan z Chemicalbook (2015-08-17).
Sytuacja niebezpieczna
Połknięcie i wdychanie są umiarkowanie toksyczne. (2) Będąc łatwopalnym z większym ryzykiem spalania. Dopuszczalne stężenie w powietrzu wynosi 600ppm (1720mg/m3) w Stanach Zjednoczonych.
Skutki uboczne i objawy zatrucia
Wdychanie wysokich stężeń cyklopentanu może powodować zahamowanie ośrodkowego układu nerwowego, chociaż jego ostra toksyczność jest niska. Objawy ostrego narażenia obejmują początkowo podniecenie, następnie pojawiają się zaburzenia równowagi, a nawet stupor, śpiączka. Rzadko zdarzają się przypadki śmierci z powodu niewydolności oddechowej. Odnotowano, że zwierzęta karmione tym towarem mogą dostać ciężkiej biegunki, co prowadzi do zapaści naczyniowej serca, płuc i wątroby oraz degeneracji mózgu.
Środki ochronne
Może być stosowany do poprawy urządzeń produkcyjnych. Stosować kremy lub rękawice ochronne do ochrony skóry.
Opieka medyczna
Przy regularnym badaniu fizykalnym zwracać uwagę na potencjalne działanie drażniące na skórę i drogi oddechowe, jak również na wszelkie powikłania ze strony nerek i wątroby.
Wymagania transportowe
Ciecz łatwopalna klasy I. Kodeks przepisów o zagrożeniach: 61013. Podczas transportu pojemnik powinien być oznaczony znakiem „ciecz łatwopalna”.
Środek gaśniczy
Patrz „cykloheksan”.
Zalecane metody unieszkodliwiania odpadów
Spalanie;
Właściwości chemiczne
Występuje jako bezbarwna ciecz o temperaturze topnienia-93,9 °C, temperaturze wrzenia 49,26 °C, gęstości względnej 0,7460 (20/4 °C), współczynniku załamania światła 1,4068 i temperaturze zapłonu-37 °C. Jest mieszalny z alkoholem, eterem i innymi rozpuszczalnikami organicznymi, nie jest łatwy do rozpuszczenia w wodzie.
(2) Stosowany jako substancja wzorcowa do analizy chromatograficznej, rozpuszczalniki, paliwa silnikowe, środki do destylacji azeotropowej.
Metoda produkcji
Cyklopentan jest składnikiem eteru naftowego w zakresie temperatury wrzenia 30-60 °C, a jego zawartość wynosi zazwyczaj 5%-10%. Stosuje się destylację atmosferyczną; przy stosunku refluksu 60: 1 i przeprowadza się w wieży o wysokości 8 m; najpierw destyluje się izopentan i n-pentan; kontynuuje się frakcjonowanie w celu otrzymania cyklopentanu o czystości powyżej 98%. Cyklopentan można również otrzymać przez redukcję cyklopentanonu lub katalityczne uwodornienie cyklopentadienu.
Zagrożenia &Informacje dotyczące bezpieczeństwa
Kategoria Ciecze łatwopalne
Klasyfikacja toksyczności: Niska toksyczność
Toksyczność ostra: doustnie-szczur LD50: 11400 mg/kg; doustnie-mysia LD50: 12800 mg/kg
Niebezpieczne właściwości materiałów wybuchowych: wybuchowy po zmieszaniu z powietrzem
Palność i sytuacje niebezpieczne: łatwopalny w przypadku pożaru, wysokiej temperatury i utleniacza ze spalaniem wydzielającym drażniący dym
Charakterystyka magazynowania: Magazyn: wentylowany, w niskiej temperaturze i suchy; Przechowywać oddzielnie z utleniaczem
Środki gaśnicze: Suchy proszek, dwutlenek węgla, piana, środek gaśniczy 1211
Norma zawodowa: TWA 1720 mg/m3; STEL 2150 mg/kg
Właściwości chemiczne
bezbarwna ciecz o zapachu zbliżonym do benzyny
Właściwości chemiczne
Cyklopentan jest bezbarwną cieczą.
Właściwości fizyczne
Bezbarwna, ruchliwa, łatwopalna ciecz o zapachu przypominającym cykloheksan.
Zastosowanie
Cyklopentan jest produktem naftowym. Powstaje z wysokotemperaturowego katalitycznego krakingu cykloheksanu lub w wyniku redukcji cyklopentadienu. Występuje w frakcjach eteru naftowego i w wielu rozpuszczalnikach handlowych. Jest stosowany jako rozpuszczalnik do farb, w ekstrakcji wosku i tłuszczu oraz w przemyśle obuwniczym.
Zastosowanie
Jako odczynnik laboratoryjny; w produkcji farmaceutyków; występuje w rozpuszczalnikach i w eterze naftowym; czynnik zwiększający ciśnienie gazów pędnych.
Metody produkcji
Cyklopentan występuje we frakcjach eteru naftowego i jest otrzymywany przez kraking cykloheksanu w obecności tlenku glinu w wysokiej temperaturze i pod wysokim ciśnieniem lub przez redukcję cyklopentadienu.
Definicja
ChEBI: Cykloalkan, który składa się z pięciu węgli, z których każdy jest związany z dwoma hydrogenami powyżej i poniżej płaszczyzny. Rodzic klasy cyklopentanów.
powietrze &woda Reakcje
Wysoce łatwopalny. Nierozpuszczalny w wodzie.
Profil reaktywności
CYKLOPENTAN jest niekompatybilny z silnymi utleniaczami, takimi jak chlor, brom, fluor….
Zagrożenie dla zdrowia
Wdychanie powoduje zawroty głowy, nudności i wymioty; stężone pary mogą powodować utratę przytomności i zapaść. Opary powodują lekkie łzawienie oczu. Kontakt z cieczą powoduje podrażnienie oczu i może podrażnić skórę, jeśli pozwoli się jej pozostać. Połknięcie powoduje podrażnienie żołądka. Aspiracja powoduje poważne podrażnienie płuc i szybko rozwijający się obrzęk płuc; pobudzenie ośrodkowego układu nerwowego, po którym następuje depresja.
Zagrożenie dla zdrowia
Cyklopentan jest substancją o niskiej toksyczności ostrej. Narażenie na jego działanie w wysokich stężeniach może powodować depresję ośrodkowego układu nerwowego z objawami pobudliwości, utraty równowagi, osłupienia i śpiączki. Niewydolność oddechowa może wystąpić u szczurów od 30-60 minut ekspozycji na 100,000-120,000 ppm w powietrzu. Działa drażniąco na górne drogi oddechowe, skórę i oczy. W literaturze brak jest informacji na temat chronicznych skutków długotrwałego narażenia na cyklopentan.
Zagrożenie pożarowe
Zachowanie w ogniu: Pojemniki mogą eksplodować.
Reaktywność chemiczna
Reaktywność z wodą Brak reakcji; Reaktywność z materiałami powszechnego użytku: Brak reakcji; Stabilność podczas transportu: Stabilny; Środki neutralizujące dla kwasów i substancji żrących: Nie dotyczy; Polimeryzacja: Nie dotyczy; Inhibitor polimeryzacji: Nie dotyczy.
Profil bezpieczeństwa
Działa łagodnie toksycznie po połknięciu i przez drogi oddechowe. Wysokie stężenia mają działanie narkotyczne. Bardzo niebezpieczne zagrożenie pożarowe w kontakcie z ciepłem lub płomieniem; może reagować z utleniaczami. Do gaszenia pożaru należy używać piany, CO2, suchej substancji chemicznej. Po podgrzaniu do rozkładu wydziela ostry dym i opary.
Potencjalne narażenie
Cyklopentan jest stosowany jako rozpuszczalnik.
Źródło
Składnik benzyny wysokooktanowej (cytowany, Verschueren, 1983). Harley et al. (2000) przeanalizowali opary w przestrzeni nadfazowej trzech gatunków benzyny bezołowiowej, do której dodano etanol w celu zastąpienia eteru metylo-tert-butylowego. Cyklopentan został wykryty w identycznym stężeniu 1,4 % mas. w oparach przestrzeni nadlotniskowej dla klas zwykłej, średniej i premium.
Schauer et al. (1999) zgłosili obecność cyklopentanu w spalinach samochodu ciężarowego o średniej ładowności z silnikiem wysokoprężnym przy poziomie emisji 410 μg/km.
Benzyna reformułowana fazy II w Kalifornii zawierała cyklopentan w stężeniu 4,11g/kg. Wskaźniki emisji z rury wydechowej samochodów zasilanych benzyną z katalizatorem i bez katalizatora wynosiły odpowiednio 0,78 i 85,4 mg/km (Schauer i in., 2002).
Postać w środowisku
Biologiczne. Cyklopentan może być utleniany przez mikroby do cyklopentanolu, który może utleniać tocyklopentanon (Dugan, 1972).
Fotolityczne. Podano następujące stałe szybkości dla reakcji oktanu i rodników OH w atmosferze: 3.7 x 10-12 cm3/molekule?sek w temperaturze 300 K (Hendry i Kenley, 1979); 5.40x 10-12 cm3/molekule?sek (Atkinson, 1979); 4.83 x 10-12 cm3/molekule?sek w temperaturze 298 K (DeMore iBayes, 1999); 6.20 x 10-12, 5.24 x 10-12, i 4.43 x 10-12 cm3/molekuł-sek w 298, 299, i 300 K, odpowiednio (Atkinson, 1985), 5.16 x 10-12 cm3/molekuł-sek w 298 K (Atkinson, 1990), i 5.02x 10-12 cm3/mol-sek w 295 K (Droege i Tilly, 1987).
Chemiczne/fizyczne. Cyklopentan nie będzie hydrolizować, ponieważ nie ma hydrolizowalnej grupy funkcyjnej. Całkowite spalanie w powietrzu daje dwutlenek węgla i wodę.
W podwyższonej temperaturze następuje rozerwanie pierścienia, tworząc etylen i przypuszczalnie alen oraz wodór (Rice i Murphy, 1942).
Wysyłka
UN1146 Cyklopentan, Klasa zagrożenia: 3; Oznakowanie:3 – ciecz łatwopalna.
Metody oczyszczania
Uwolnić go od cyklopentenu przez dwukrotne przejście przez kolumnę starannie wysuszonego i odgazowanego aktywnego żelu krzemionkowego. Występuje w ropie naftowej i jest wysoce łatwopalna.