Abstract
Syöpä syntyy kontrolloimattoman solukasvun tai epänormaalin solunjakautumisen DNA-vaurion yhteydessä. Karsinogeenit ovat tekijöitä, jotka aiheuttavat DNA-mutaatioita ja niiden tiedetään aiheuttavan syöpää kehossamme tekemällä muutoksia geenitasolla. Geneettinen alttius on myös tärkeä syövän kehittymisessä yhdessä sellaisten tekijöiden kanssa kuin huonot elinolosuhteet. Lisäksi kaikilla näillä ympäristötekijöillä, kuten röntgensäteillä, gammasäteillä, radioaktiivisista materiaaleista peräisin olevalla säteilyllä, aniliinityyppisillä väriaineilla, savukkeilla, vapailla radikaaleilla, asbestilla, piidioksidipölyllä, ilman pilaantumisella, elintarvikelisäaineilla, erilaisilla lääkkeillä, joillakin hajuvesissä käytetyillä kemikaaleilla, syöpää aiheuttavilla viruksilla ja bakteereilla on tärkeä rooli syövän synnyssä, ja ne myötävaikuttavat osaltaan syövän ilmaantuvuuden lisääntymiseen. Syövän aiheuttavia ympäristötekijöitä on ilmassa, vedessä, maaperässä ja elintarvikkeissa, joita tarvitsemme elämiseen. Näin ollen ihmiset saavat syövän altistuttuaan syöpää aiheuttaville tekijöille ympäristössä, jossa he elävät. Syöpä on vaikeasti hoidettava sairaus ja heikentää syöpää sairastavien elämänlaatua. Ympäristötekijöiden vaikutusten tutkiminen syöpään ja syövän kehittymisen ehkäiseminen syövän aiheuttavia tekijöitä määrittelemällä ovat tästä näkökulmasta erittäin tärkeitä.
Avainsanat
Ympäristö, syöpää aiheuttavat aineet, syöpä, syöpä, DNA, mutaatio
Esittely
Syöpä, joka on toiseksi yleisin kuolinsyy, on sairausryhmä, johon liittyy solujen epänormaali kasvu, jolla on potentiaalia tunkeutua muualle elimistöön tai levitä muihin kehonosiin . GLOBOCANin mukaan maailmassa oli vuonna 2012 noin 14,1 miljoonaa uutta syöpätapausta, 8,2 miljoonaa syöpäkuolemaa ja 32,6 miljoonaa ihmistä, jotka elivät syövän kanssa viiden vuoden kuluessa diagnoosista. Toisaalta arvioidaan, että Yhdysvalloissa diagnosoidaan 1 685 210 uutta syöpätapausta ja 595 690 ihmistä kuolee tautiin vuonna 2016. Näin ollen tarvitaan kiireellisesti uutta hoitostrategiaa syöpään liittyvien kuolemantapausten vähentämiseksi.
Syöpä on monitekijäinen sairaus. Useimmat geneettiset tekijät ja ympäristötekijät, kuten virukset, bakteerit, säteily sekä ruokailutottumukset ja kemikaalit, lisäävät riskiä sairastua syöpään (kuva 1). Kaikista syövistä 10-15 %:n uskotaan liittyvän perinnöllisyyteen, kun taas loput, 85-90 % syövistä, juontavat juurensa ympäristöön ja elintapoihin. Tiedetään, että noin 25-30 prosenttia tupakasta, 30-35 prosenttia ruokavaliosta, 15-20 prosenttia infektioista ja loput prosenttia muista tekijöistä, kuten säteilystä, stressistä, fyysisestä aktiivisuudesta, ympäristön epäpuhtauksista jne. aiheutuu syöpäkuolleisuutta . Geneettisten tekijöiden osalta mutaatiot useissa geeneissä, kuten onkogeeneissä, kasvainsuppressorigeeneissä ja DNA:n korjausgeeneissä, voivat johtaa syövän syntyyn pikemminkin kuin yksittäinen geeni. Nämä geenit aiheuttavat syöpää kolmen tärkeimmän biologisen reitin kautta, jotka normaalisti säätelevät kudoksen homeostaasia ja solujen kasvua. Tätä varten tämän tutkimuksen tavoitteena oli keskustella geneettisten tekijöiden vuorovaikutuksesta erilaisten ympäristötekijöiden kanssa, mukaan lukien ruokavalio, elintavat, aineenvaihdunnan muutokset ja erilaiset ympäristöaltistukset.
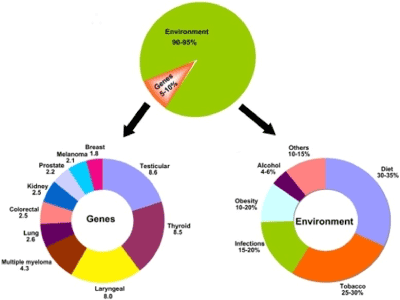
Kuva 1. Geenien ja ympäristön rooli syövän kehittymisessä .
Syövän ja genetiikan välinen suhde
Perimäperäisillä geneettisillä tekijöillä on tärkeä rooli syövän kehittymisessä. Kriittisten geenien, kuten kasvainsuppressorigeenien, onkogeenien ja DNA:n korjaukseen osallistuvien geenien mutaatio johtaa geneettiseen epävakauteen ja syövän kehittymiseen. Useita perinnöllisiin syöpiin liittyviä geenejä on tunnistettu leukemiassa, tietyissä lapsuuden kasvaimissa, paksusuolen ja erityisesti rinta- ja munasarjasyövässä. . Esimerkiksi rintasyöpägeeni 1:n sukusolumutaatiot ovat altistava geneettinen tekijä 15-45 prosentissa perinnöllisistä rintasyövistä. Naisilla mutaation kantajilla on 60-80 prosentin elinikäinen riski sairastua rintasyöpään ja 20-40 prosentin elinikäinen riski sairastua munasarjasyöpään . Lisäksi mutaatiot APC-geenissä tai DNA:n korjausgeeneissä johtavat kahteen erityyppiseen perinnölliseen paksusuolisyöpään, familiaaliseen adenomatoottiseen polypoosiin ja perinnölliseen ei-polypoosiseen kolorektaalisyöpään .
Syövän ja syöpää aiheuttavien aineiden välinen suhde
Ympäristötekijöillä, kuten röntgensäteillä, gammasäteillä, radioaktiivisten materiaalien lähettämällä säteilyllä, aniliinityyppisillä väriaineilla, savukkeilla, vapailla radikaaleilla, asbestilla, piidioksidipölyllä, ilmansaasteilla, elintarvikkeiden lisäaineilla, erilaisilla lääkkeillä, joillakin hajuvesien kemikaaleilla, syöpää aiheuttavilla viruksilla ja bakteereilla, on suuri merkitys syövän riskiin. .
Säteily
Säteily luokitellaan kahteen perusluokkaan, ionisoimattomaan ja ionisoivaan säteilyyn. Ionisoivalla säteilyllä tarkoitetaan röntgensäteilyä, joka muodostaa sähköisesti varattuja hiukkasia tai ioneja . Röntgen- ja gammasäteilyä käytetään erityisesti lääketieteellisessä kuvantamisessa . Tietokonetomografia on radiologinen menetelmä, joka tuottaa kolmiulotteisen kuvan eri sairauksien diagnosoimiseksi . Useissa tutkimuksissa on kuvattu, että diagnostiset röntgensäteet aiheuttavat mutaatioita ja jopa 10 prosenttia invasiivisista syövistä liittyy säteilyaltistukseen . Tämän huolen osalta on vuosikymmenien ajan seurattu suuria kohortteja potilaita, joita on hoidettu sädehoidolla kohdunkaulan syövän, rintasyövän, Hodgkinin lymfooman, kivessyövän ja lapsuusiän syövän vuoksi. Lisääntynyt seulonta säteilyaltistuksessa tiedetään syövän ilmaantuvuuden riskistä. Tältä osin biologinen vaikutus voi muuttua säteilyn ekvivalenttiannoksen mukaan .
Raskasmetallit
Altistuminen erilaisille kemikaaleille ja raskasmetalleille riippuen altistuneesta annoksesta, genetiikasta, ihmisten immuuniresistenssistä ja yleisestä terveydentilasta, iästä, ravitsemuksen tasosta on yhdistetty eri syöpien riskiin, mukaan lukien rintasyöpä, haima-, keuhko- ja sappirakkosyöpä jne. Kun metallit pääsevät elimistöön ilman, ruoan, veden tai ihon kautta, ne vaikuttavat entsymaattisesti ja genotoksisesti eri elimiin. Joidenkin raskasmetallien, kuten arseenin, kadmiumin, kromin, nikkelin ja sinkin tiedetään kehittävän syöpää. Ne sitoutuvat elintärkeisiin solukomponentteihin, kuten rakenneproteiineihin, entsyymeihin ja nukleiinihappoihin . Esimerkiksi kadmiumin vaikutus keuhko- ja eturauhassyöpään on todettu . Sinkin toksikologiset vaikutukset määritettiin koe-eläimillä . Lisäksi tietyille metalliyhdisteille altistumisen ja rintasyövän riskin välillä saattaa olla yhteys . Tarvitaan kuitenkin kiireellisesti koe-eläintutkimuksia ja epidemiologisia tutkimuksia, jotka liittyvät metalleihin ja syöpään.
Savuke
Savukkeen savun sisältämät kemikaalit aiheuttavat DNA-vaurioita ja ovat lisänneet erilaisten syöpien, erityisesti primaarisen keuhkosyövän riskiä . Tiedetään, että lähes yhdeksän kymmenestä keuhkosyövästä johtuu tupakanpoltosta. Savukkeet aiheuttavat noin 1,5 miljoonaa keuhkosyöpäkuolemaa vuodessa ja määrän arvioidaan nousevan lähes 2 miljoonaan vuodessa 2020- tai 2030-luvulla .
Ruoka ja ravitsemus
Ruokavaliotekijät on yhdistetty 30 %:iin syöpätapauksista länsimaissa. Itse asiassa ruokavalion tekeminen on tupakan jälkeen toisena tekijänä ehkäistävissä olevan syövän aiheuttajana. Ruokavalion vaikutuksia syöpäriskiin kehitysmaissa on pidetty noin 20 % . Toisaalta joillakin lisäaineiden osilla on syöpää aiheuttavia vaikutuksia. Esimerkiksi maksasyöpää aiheuttavien synteettisten lisäaineiden kaltaiset dulce, cinnamyyliantranilaatti ja tiourea on havaittu joissakin kokeissa, ja siksi näiden aineiden käyttö elintarvikkeissa on kielletty. Joitakin aineita, kuten nitriittisuoloja, natriumnitriittiä tai kaliumnitriittiä, on kuitenkin käytetty siitä huolimatta, että ne lisäävät syöpäriskiä. Lihavalmisteet, kuten makkarat, sisältävät näitä aineita antibakteerisina ja väriaineina. Tämäntyyppiset lihajalosteet lisäävät suolistosyövän riskiä 21 prosentilla . Valitettavasti sokerin ja suolan, jotka ovat kaksi tärkeintä elintarviketta, liiallinen kulutus aiheuttaa lihavuutta ja insuliinin lisääntymistä, joten näiden aineiden korkeampi määrä lisää epäsuorasti syöpäriskiä. Lisäksi aflatoksiineja esiintyy maapähkinöissä, palkokasveissa, öljykasveissa ja viljoissa, ja ne lisäävät hepatosellulaarisen syövän riskiä .
Vapaat radikaalit ja ROS
Vapaat radikaalit ja ROS on yhdistetty lisääntyneeseen syöpäriskiin . Erityisesti vapaat radikaalit aiheuttavat syöpää ja ateroskleroosisairauksia. Vapaat radikaalit johtavat syövän syntyyn ja edistämiseen kromosomivirheiden ja onkogeenien aktivoitumisen kautta. Toisaalta ROS:illa, kuten superoksidi-anionilla, vetyperoksidilla, hydroksyyliradikaalilla ja typpioksidilla sekä niiden biologisilla aineenvaihduntatuotteilla on myös tärkeä rooli karsinogeneesissä. ROS:t aiheuttavat DNA-vaurioita, kuten kaksoissäikeiden katkeamisia, emäsmuutoksia ja DNA-proteiinien ristisidoksia.
Liikenneilman pilaantuminen
Moottoriajoneuvoista, teollisuusprosesseista, sähköntuotannosta, kotitalouksien kiinteiden polttoaineiden poltosta ja muista lähteistä peräisin olevat päästöt saastuttavat ilmaa kaikkialla maailmassa ja vaikuttavat maailmanlaajuisesti. Ilmansaasteiden kemialliset ja fysikaaliset ominaisuudet voivat vaihdella saastelähteiden, ilmaston ja meteorologian mukaan. Ilmansaasteiden tiettyjen kemikaalien tiedetään kuitenkin olevan ihmiselle syöpää aiheuttavia. Vuonna 1971 laadittiin Yhdysvaltojen Clean Air Act -laki, jossa otsoni, hiukkaset, rikkidioksidi, typpidioksidi, hiilimonoksidi ja lyijy määriteltiin ilman epäpuhtauksiksi. Lisäksi on määritelty 189 myrkyllistä ja vaarallista ilman epäpuhtautta. Hiljattain arvioitiin, että altistuminen ilmassa oleville pienhiukkasille aiheutti vuonna 2010 maailmanlaajuisesti 3,2 miljoonaa ennenaikaista kuolemantapausta, jotka johtuivat suurelta osin sydän- ja verisuonitaudeista, ja 223 000 kuolemantapausta keuhkosyövästä.
Nämä ilmansaasteet aiheuttavat akuutteja sairauksia, kuten oksentelua, kroonisia sairauksia, kuten syöpää, sekä immunologisia, neurologisia, lisääntymis- ja kehityspoliittisia tauteja ja hengityselinsairauksia. Altistuminen näille kemikaaleille lisää keuhkopussin ja vatsakalvon kasvainten riskiä ja keuhkosyövän ilmaantuvuutta .
Onkogeeniset virukset
Onkovirukset tai kasvainvirukset ovat yleisnimitys viruksille. Tätä termiä alettiin käyttää 1950-60-luvuilla osoittamaan akuuttia muuntumista. Nykyään sillä tarkoitetaan mitä tahansa DNA- tai RNA-genomia sisältävää virusta ja siten se on synonyymi ”kasvainvirukselle” tai ”syöpävirukselle”. Suurin osa viruksista ei kuitenkaan aiheuta syöpää ihmisille tai eläimille . Onkovirukset, kuten hepatiittivirukset , ihmisen papilloomavirukset , Kaposin sarkooma-assosioitunut herpesvirus , ihmisen T-lymphotrooppinen virus ja Epstein-Barr-virus on yhdistetty syöpäriskiin . On arvioitu, että virusinfektiot aiheuttavat 15-20 prosenttia kaikista ihmisen syövistä. Näin ollen näitä syöpiä voidaan ehkäistä rokottamalla ja ne voidaan havaita yksinkertaisella verikokeella ja hoitaa viruslääkkeillä.
Keskustelu
Uudet syöpätutkimusalueet keskittyvät epäpuhtauksien mahdollisiin vuorovaikutussuhteisiin keskenään ja geneettisten tekijöiden kanssa. Syövän tarkkaa syytä tai syitä ei ole tarkkaan tiedetty. Kuitenkin tietyt geenit, jotka taipuvat syöpään, ovat vuorovaikutuksessa joidenkin ympäristötekijöiden, kuten virusten, säteilylle altistumisen, erilaisten kemikaalien ja saasteiden kanssa ja liittyvät syöpäriskin lisääntymiseen. Syöpää aiheuttavat aineet vaikuttavat vahingoittamalla DNA:ta, häiritsemällä hormoneja, tulehduttamalla kudoksia tai kytkemällä geenejä päälle tai pois päältä . Toisaalta on olemassa huomattavaa näyttöä siitä, että kahden eri altisteen yhteisvaikutus voi aiheuttaa joitakin syöpiä. Esimerkiksi asbesti tehostaa tupakansavun karsinogeenisuutta, joten keuhkosyöpätapauksia oli erityisen paljon ihmisillä, jotka tupakoivat ja altistuivat asbestille työpaikoillaan . Näin ollen ympäristöä käytetään usein laajasti lääketieteellisessä kirjallisuudessa, ja tiedetään, että ympäristötekijät ovat lisänneet syöpäriskiä . Näin ollen tarvitaan lisää yksityiskohtaisia tutkimuksia, jotta voidaan määrittää ympäristötekijöiden tarkat vaikutukset syövän kehittymiseen.
Johtopäätös
Ihmiset voivat välttää joitakin syöpää aiheuttavia altistumisia, kuten tupakansavua ja auringonsäteitä. Muita ympäristöriskitekijöitä, kuten ilman, veden ja ruoan epäpuhtauksia, ei kuitenkaan voida estää, koska ne koostuvat normaalista elämästä. Tiedetään, että ympäristötekijät voivat aiheuttaa tai edistää syövän kehittymistä. Tarvitaan kuitenkin yksityiskohtaisempia tutkimuksia terveysvaikutuksen tarkan syyn määrittämiseksi. Kun on tehty suuri määrä tutkimuksia, voidaan todellisen syöpäriskin ja ympäristöriskitekijöiden välinen yhteys saada selvemmäksi.
- Futreal PA, Kasprzyk A, Birney E, Mullikin JC, Wooster R, et al. (2001) Cancer and genomics. Nature 409: 850-852.
- Stratton MR, Campbell PJ, Futreal PA (2009) The cancer genome. Nature 458: 719-724.
- Williams GM (2001) Kemiallisen karsinogeneesin mekanismit ja soveltaminen ihmisen syöpäriskin arviointiin. Toxicology 166: 3-10.
- Williams G M (1979) Review of in vitro test systems using DNA damage and repair for screening of chemical carcinogens. J Assoc Official Anal Chemists 62: 857-863.
- Williams G M (1985) Genotoxic and epigenetic carcinogens, In: F. Homburger (toim.), Safety Evaluation and Regulation of Chemicals 2 (Kemikaalien turvallisuuden arviointi ja sääntely). Impact of Regulations-Improvement of Methods, Basel: Karger: 251-256.
- Williams G M (1987) DNA reaktiiviset ja epigeneettiset karsinogeenit, In: J.C. Barrett, (toim.), Mechanisms of Environmental Carcinogenesis, Vol 1: Role of Genetic and Epigenetic Changes, Boca Raton, FL: CRC Press, Inc:113-127.
- Williams GM (1987) Definition of a human cancer hazard. In: Nongenotoxic Mechanisms in Carcinogenesis. New York: Banbury Report 25, Cold Spring Harbor Laboratory: 367-380.
- Williams GM (1992) DNA-reaktiiviset ja epigeneettiset karsinogeenit. Exp Toxicol Pathol 44: 457-464.
- ”Tag: Early diagnosis of cancer”, https://sanjivharibhakti.wordpress.com/tag/early-diagnosis-of-cancer/ (Accessed: Mar 11, 2017).
- Yokus B, Ülker DU (2012) Kanser Biyokimyasi. Dicle Üniv Vet Fak Derg 1: 7-18.
- Aksoy U, Eltem R, Meyvaci KB, Altindisli A, Karabat S (2007) Five-year survey of ochratoxin A in processed sultanas from Turkey. Food Addit Contam 24: 292-296.
- Lobo V, Patil A, Phatak A, Chandra N (2010) Free radicals, antioxidants and functional foods: Impact on human health. Pharmacogn Rev 4: 118-126.
- Bougie O, Weberpals JI (2011) Clinical Considerations of BRCA1 – and BRCA2 -Mutation Carriers: A Review. Int J Surg Oncol 2011: 374012.
- King MC, Marks JH, Mandell JB (2003) BRCA1:n ja BRCA2:n perinnöllisten mutaatioiden aiheuttamat rinta- ja munasarjasyövän riskit. Science 302: 643-646.
- Antoniou A, Pharoah PD, Narod S, Risch HA, Eyfjord JE, et al. (2003) Keskimääräiset rinta- ja munasarjasyövän riskit, jotka liittyvät BRCA1- tai BRCA2-mutaatioihin, jotka on havaittu tapaussarjoissa, joita ei ole valittu sukuhistorian perusteella: 22 tutkimuksen yhdistetty analyysi. Am J Hum Genet 72: 1117-1130.
- Vogelstein B, Kinzler KW (1993) Syövän monivaiheisuus. Trends Genet 9: 138-141.
- Dauda S (2011) Dicle Üniversitesi Tip Fakültesi Biyofizik Anabilim Dalinda ”Iyonlastirmayan Elektromanyetik Alanlar Ve Ihsan Sagligi” Üzerine Yapilmis Arastirma Sonuçlarinin Degerlendirilmesi ÇEVRE ve Halk Sagligi Için Emanet 2011, Elektromanyetik Alanlar ve Etkileri Sempozyumu 7 – 8 Ekim, Istanbul: 233-237.
- Elektromanyetik Kirlilik ve Saglik. Kent ve Elektromanyetik Dalga Kirliligi Sempozyumu Bildiri Kitabi, Antalya, 2010; 15-22.
- 2007 Recommendations of the International Commission on Radiological Protection (Users Edition)” ICRP Publication 103. Ann ICRP 37: 1-332.
- Radiation protection in Medicine (Säteilysuojelu lääketieteessä) ICRP Publication 105. Ann ICRP 37: 1-63.
- Säteilysuojelu, röntgensäteet. http://www.arpansa.gov.au/radiationprotection/ Basics/xrays.cfm (Viitattu: 29. toukokuuta 2016).
- Huang BS, Law MWM, Khong PL (2009) Whole-Body PET/CT Scanning: Estimation of Radiation Dose and Cancer Risk. Radiology 251: 166-174.
- National Toxicology Program, U.S. Department of Health and Human Services, Eleventh Edition of the Report on Carcinogens, 31. tammikuuta 2005.
- Dedic S, Pranjic N (2009) Lung cancer risk from exposure to diagnostic x- rays. Health Med 3: 307-313.
- Herfarth H, Palmer L (2009) Risk of Radiation and Choice of Imaging. Dig Dis 27: 278-284.
- Heyes GJ, Mill AJ, Charles MW (2009) Mammography-oncogenecity at low doses. J Radiol Protect 29: A123-A132.
- Gilbert ES (2009) Säteilyyn liittyvä kiinteiden syöpien riski näyttää säilyvän läpi elämän. Int J Radiation Biol 85: 467-482.
- Dawson P, Punwani S (2009) The thyroid dose burden in medical imaging: A re-examination. Eur J Radiol 69: 74-79.
- Wakeford R (2008) Childhood leukemia following medical diagnostic exposure to ionizing radiation in utero or after birth. Radiat Prot Dosimetry 132: 166-174.
- Myles P, Evans S, Lophatananon A, Dimitropoulou P, Easton D, et al. (2008) Diagnostiset säteilytoimenpiteet ja eturauhassyövän riski. Br J Cancer 98: 1852-1856.
- Gilbert ES (2009) Ionizing Radiation and Cancer Risks: What Have We Learned From Epidemiology? Int J Radiat Biol 85: 467-482.
- Chhabra D, Oda K, Jagannath P, Utsunomiya H, Takekoshi S, et al. (2012) Chronic Heavy Metal Exposure and Gallbladder Cancer Risk in India, a Comparative Study with Japan. Asian Pac J Cancer Prev 13: 187-190.
- Antwi SO, Eckert EC, Sabaque CV, Leof ER, Hawthorne KM, et al. (2015) Altistuminen ympäristökemikaaleille ja raskasmetalleille sekä haimasyöpäriski. Cancer Causes Control 26: 1583-1591.
- Verougstraete V, Lison D, Hotz P (2003) Cadmium, Lung and Prostate Cancer: A Systematic Review of Recent Epidemiological Data. J Toxicol Environ Health B Crit Rev 6: 227-256.
- Vural H (1993) Agir metal iyonlarinin gidalarda olusturdugu kirlilikler. Çevre Dergisi 8: 3-8.
- Florea M, Büsselberg D (2011) Metals and Breast Cancer: Riskitekijöitä vai parantavia tekijöitä? J Toxicol 8: 1-8.
- Proctor NR (2012) Savukkeiden keuhkosyöpäyhteyden löytämisen historia: todistusperinteet, yritysten kieltäminen, maailmanlaajuinen tulli. Tob Control 21: 87-91.
- Key TJ, Schatzkin A, Willett WC, Allen NE, Spencer EA, et al. (2004) Diet, nutrition and the prevention of cancer. Public Health Nut 7: 187-200.
- Czene K, Lichtenstein P, Hemminki K (2002) Environmental and heritable causes of cancer among 9.6 million individuals in the Swedish Family-Cancer Database. Int J Cancer 99: 260-266.
- Anand P, Kunnumakara AB, Sundaram C, Harikumar KB, Tharakan ST, et al. (2008) Syöpä on ennaltaehkäistävissä oleva sairaus, joka edellyttää merkittäviä elämäntapamuutoksia. Pharm Res 25: 2097-2116.
- Boffetta P, Nyberg F (2003) Ympäristötekijöiden vaikutus syöpäriskiin. Br Med Bull 68: 71-94.
- Irigaray P, Newby JA, Clapp R, Hardell L, Howard V, et al. (2007) Lifestyle-related factors and environmental agents causing cancer: an overview. Biomed Pharmacother 61: 640-658.
- Kushi LH, Doyle C, McCullough M, Rock CL, Demark-Wahnefried W, et al. (2006) American Cancer Society Guidelines on Nutrition and Physical Activity for Cancer Prevention: Reducing the Risk of Cancer with Healthy Food Choices and Physical Activity. CA Cancer J Clin 56: 254-281.
- Hussain SP, Hofseth LJ, Harris CC (2003) Radical causes of cancer. Nat Rev Cancer 3: 276-285.
- Burrows M (2009) The Clean Air Act: Citizen Suits: Citizen Suits, Attorneys’ Fees and the Separate Public Interest Requirement. Envtl Aff 36.
- Air pollution and cancer. https://www.iarc.fr/en/publications/books/sp161/ Air Pollutionand Cancer16.pdf (viitattu 18.5.2016).
- Brown RC1, Hoskins JA, Miller K, Mossman BT (1990) Pathogenetic mechanisms of asbestos and other mineral fibres. Mol Aspects Med 11: 325-349.
- Peto J, Seidman H, Selikoff IJ (1982) Mesotelioomakuolleisuus asbestityöntekijöillä: Implications for models of carcinogenesis and risk assessment. Br J Cancer 45: 124-132.
- Maghissi AA, Seiler MC (1989) Radonin jälkeläisille altistumisen lisääntyminen passiivisen tupakoinnin seurauksena. Environ Int 15: 261-264.
- Kunz E, Sevc J, Placek V, Horácek J (1979) Ihmisen keuhkosyöpä suhteessa säteilyaltistuksen eri aikajakaumiin. Health Phys 36: 699-706.
- Onkovirüs. https://tr.wikipedia.org/wiki/Onkovir%C3%BCs (viitattu 20.5.2016).
- Margaret EM, Munger K (2007) Viruses associated with human cancervol. Biochim Biophys Acta 1782: 127-150.
- Miten monta syöpää ympäristö aiheuttaa? http://www.scientificamerican.com/ article/how-many-cancers-are-caused-by-the-environment/ (viitattu 13.5.2016).
- L. Tomatis (1990) Cancer: Causes, occurrence and control. IARC Scientific Publications, 100. Kansainvälinen syöväntutkimuskeskus, Lyon.