Yli 200 000 henkilölle on tehty transkatetrinen aorttaläpän vaihto (TAVR), ja vuosittain noin 140 000 potilaalle asennetaan kirurginen bioproteettinen läppä.1,2 Tästä kasvavasta määrästä huolimatta optimaalinen postoperatiivinen antikoagulaatiostrategia on usein epäselvä. Erityisesti kaksi kysymystä korostaa päätöksenteon vaikeutta näissä yleisissä kliinisissä skenaarioissa:
- Mitä komplikaatioita yritämme vähentää antikoagulaatiolla bioproteettisen läpän vaihdon jälkeisinä ensimmäisinä kuukausina?
- Pitäisikö antikoagulaatiota antaa kaikille potilaille näiden komplikaatioiden vähentämiseksi? Vai pitäisikö meillä olla valikoivampi lähestymistapa, joka perustuu riskitekijöihin?
Tromboosiriskit bioproteettisen läpän vaihdon jälkeen
Traditionaalisesti antikoagulaation perusteena kirurgisen läpänvaihdon jälkeisinä ensimmäisinä kuukausina on ollut vähentää tromboottisia komplikaatioita, jotka liittyvät oletettavasti ommelmateriaaleihin ja ompelurenkaaseen, joka ei ole vielä peittynyt biofilmiin ja endotelisoitunut3,4 . Mahdollisia myöhempiä tromboottisia komplikaatioita on kolme: tromboemboliset tapahtumat, läpän avoin tromboosi ja subkliininen järjestäytynyt trombi, joka voi heikentää läpän pitkäaikaista toimintaa. Bioproteettisen läpän vaihdon yleisyydestä huolimatta näihin komplikaatioihin liittyvät tiedot ovat vähäisiä, osittain siksi, että nämä tapahtumat ovat näennäisesti harvinaisia.
Tuoreessa meta-analyysissä korostettiin pientä tapahtumamäärää bioproteettisen läpän vaihdon jälkeen. Tässä analyysissä, johon osallistui 31 740 potilasta, joille oli tehty pääasiassa kirurginen aorttaläpän tekonivelleikkaus, varhaisia tromboembolisia tapahtumia esiintyi 145 potilaalla (1 %), jotka käyttivät K-vitamiiniantagonisteja, ja 262 potilaalla (1,5 %), jotka eivät käyttäneet K-vitamiiniantagonisteja (odds ratio 0,96; 95 %:n luottamusväli, 0,60-1,52).5 Jos oletamme, että K-vitamiiniantagonisteja käyttämättömillä potilailla tromboembolisten komplikaatioiden määrä lisääntyy 0,5 % kirurgisen aorttaläpän vaihdon jälkeisinä ensimmäisinä kuukausina 0,5 %:lla, tarvittaisiin noin 15 500 potilasta riittävän tehokasta satunnaistettua ja kontrolloitua tutkimusta varten.6 Tähän mennessä on tehty kaksi satunnaistettua tutkimusta, joihin osallistui yhteensä 268 potilasta.7,8 Kun otetaan huomioon potilaiden pieni määrä, ei ole yllättävää, ettei tilastollisesti havaittavaa eroa näissä kahdessa ryhmässä ole.
Suurten satunnaistettujen kontrolloitujen tutkimusten puuttuessa lääkäreiden on turvauduttava havainnointitutkimuksiin, kuten Tanskan kansallisen potilasrekisterin analyysiin.9 Tässä tutkimuksessa, johon osallistui 4075 potilasta, joille oli asennettu bioproteettinen aorttaläppä, varfariinin lopettamiseen liittyi lisääntyneitä tromboembolisia tapahtumia ja sydän- ja verisuonitautien aiheuttamia kuolemantapauksia kuolintapauksia 1-6 kuukautta leikkauksen jälkeen. Mielenkiintoista oli, että vaikka aivohalvausten määrä lisääntyi kolmen ensimmäisen kuukauden aikana hoitoryhmässä, aivohalvausten määrä kolmen ja kuuden kuukauden välisenä aikana ei eronnut varfariinia jatkaneiden tai lopettaneiden potilaiden välillä, vaikka tapahtumia oli tänä aikana vain 21. Myöskään verenvuototapahtumissa ei ollut eroa 3 kuukauden ja 1 vuoden välillä. Tämä havainto on ristiriidassa aiempien raporttien ja kliinisen kokemuksen kanssa, joiden mukaan varfariinipotilaat joutuvat todennäköisemmin sairaalahoitoon verenvuodon vuoksi.5 Näin ollen kirjoittajien johtopäätökset kardiovaskulaarisesta kuolleisuudesta ja tromboembolisista tapahtumista ovat saattaneet liittyä jäljellä olevaan sekoittavaan tekijään. Erityisesti verenvuototapahtumissa ei ehkä ollut eroa, koska lääkärit aloittivat tai jatkoivat antikoagulaatiota epätodennäköisemmin suurimman riskin potilailla.
Valitettavasti tromboembolisiin tapahtumiin verrattuna julkaistut tiedot antavat vieläkin vähemmän tietoa bioproteettisen läpän tromboosia koskevista päätelmäyhteyksistä. Tapahtumia on raportoitu vain vähän, ja suurin osa kirjallisuudesta rajoittuu tapaussarjoihin ja yhden keskuksen kokemuksiin.10 Näin ollen bioproteettisen läpän tromboosin ilmaantuvuus ei ole tarkkaan määritelty, vaikka eräässä tutkimuksessa vain 8 potilasta 4568 bioproteettisella aorttaläpällä varustetusta potilaasta tarvitsi uusintaleikkauksen trombiin liittyvän aorttastenoosin vuoksi.11 Samoin kliinisesti piilevän tromboosin ja mahdollisen nopeutuneen bioproteettisen läpän rappeutumisen merkitys on suurelta osin tuntematon.
Selektiivinen antikoagulaatio bioproteettisen läpän vaihdon jälkeen
Epäselvän hyödyn suuruuden ja hyvin hyväksytyn verenvuotoriskin perusteella yleistä antikoagulaatiota bioproteettisen aorttaläpän vaihdon jälkeen on vaikea perustella; tämä epävarmuus näkyy American College of Cardiologyn ja American Heart Associationin (ACC/AHA:n) vuoden 2014 sydämen läppävika- ja sydänsairauksia koskevien ohjeiden suosituksessa, joka kuuluu luokkaan IIb.12 Saattaa kuitenkin esiintyä erityisiä kliinisiä tilanteita, joissa antikoagulaatiota olisi harkittava voimakkaammin. Esimerkiksi äskettäin tehdyssä tapaus-verrokkitutkimuksessa, johon osallistui 46 potilasta, joille oli tehty uusintaleikkaus bioproteettisen aorttaläpän tromboosin vuoksi, keskimääräisen Doppler-gradientin lisääntyminen >50 % kaikukardiografiassa lähtötilanteeseen verrattuna, suurentunut ulokepaksuus ja ulokkeen epänormaali liikkuvuus liittyivät kaikki läpän tromboosiin.13 Sen vuoksi näillä potilailla voitaisiin harkita koeajoa, jossa annettaisiin antikoagulaatiota ja seurantakäynnillä tehtävää kaikukardiografiaa, jolla arvioitaisiin doppler-gradienttia,14 vaikka onkin epäselvää, missä määrin antikoagulaatio muuttaisi läpän lyhyen aikavälin ja pitkäkestoisen toiminnan vaikutusta.
Potilailla, joilla on bioproteettinen mitraaliläppä, näyttää lisäksi olevan suurempi riski tromboembolisiin tapahtumiin ja läppätromboosiin (ks. alla oleva havainnollistava tapaus, jossa on kuvat 1-2 ja videot 1-2). Koska bioproteettisen mitraaliläpän vaihto on paljon harvinaisempaa kuin aorttaläpän vaihto, tietoja on vielä vähemmän. Yhden keskuksen tutkimuksessa, johon osallistui 216 potilasta, joille oli tehty bioproteettinen mitraaliläpän tekonivelleikkaus, 10 (5 %) sai iskeemisen aivohalvauksen kuuden kuukauden kuluessa.15 Toisessa tutkimuksessa, johon osallistui 149 peräkkäistä potilasta, 9 (6 %) sai bioproteettisen mitraaliläpän tromboosin16 . Näin ollen bioproteettisen mitraaliläpän tekonivelleikkauksen saaneilla potilailla näyttää olevan suurempi riski, ja rutiininomaista antikoagulaatiota olisi harkittava 3-6 kuukauden ajan, mikä heijastuu jälleen luokan IIa suositukseen ACC/AHA:n sydänläppien sairauksia koskevissa vuoden 2014 ohjeissa.12
Kuvaileva tapaus: Bioproteettisen mitraaliläpän tromboosi
71-vuotias nainen sai sydämen vajaatoiminnan kahdeksan kuukautta sen jälkeen, kun hänelle oli vaihdettu bioproteettisen mitraaliläpän tekonivelleikkaus, jonka syynä oli ollut mitraalisen mitraaliläpän reumaattinen stenoosi. Leikkauksen jälkeen häntä oli hoidettu kumadiinilla 3 kuukauden ajan ja hän jatkoi aspiriinin käyttöä. Hänellä ei ollut aiemmin ollut eteisvärinää ja hän oli ollut kuumeeton, ja veriviljelyt olivat negatiivisia.
Video 1
Kuva 1
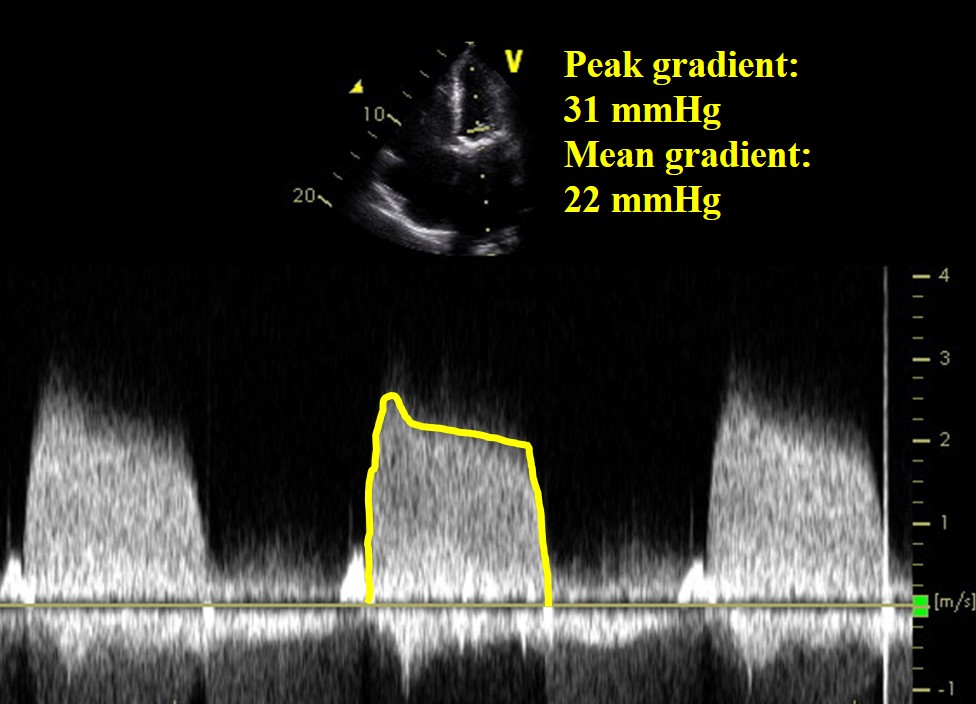
Video 2
Kuva 2
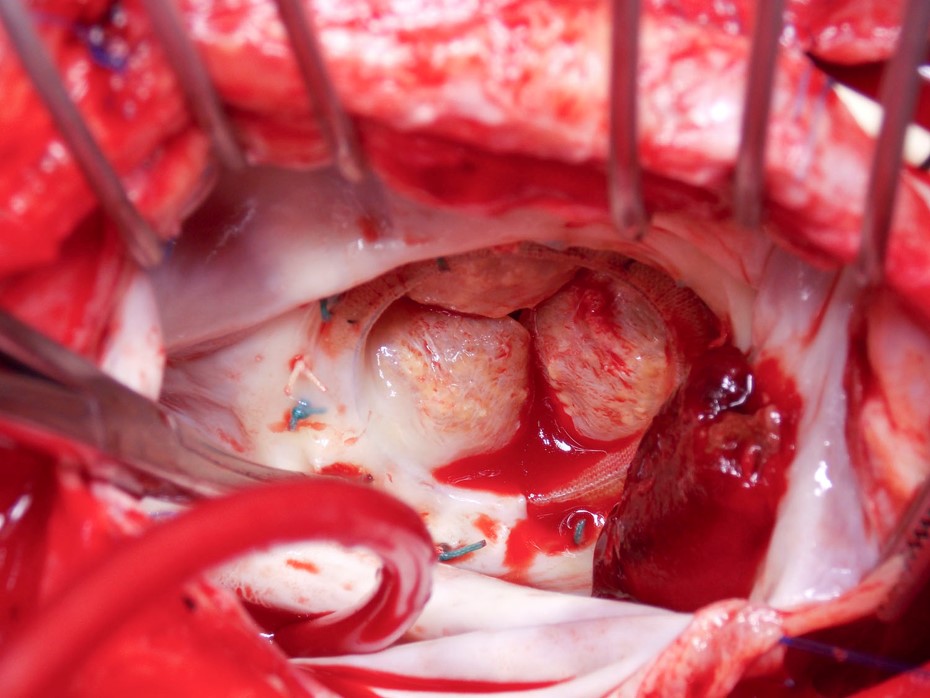
Viimeiseksi ja ehkä kiistanalaisimmaksi kysymykseksi nousee se, pitäisikö lähestymistapamme antikoagulaatiohoitoon olla erilainen niiden potilaiden osalta, joille on tehty TAVR. Aluksi oletuksena on ollut, että näitä potilaita hoidetaan aspiriinilla ja klopidogreelillä, koska tämä oli satunnaistetuissa tutkimuksissa käytetty lähestymistapa. Viime aikoina on kuvattu elektrokardiografian avulla tehdyssä neliulotteisessa tietokonetomografia-angiografiassa (CTA), että bioproteettisen aorttaläpän läpän liikkuvuus on heikentynyt ja että läpän paksuuntuminen on hypoattenuoitunut, mikä viittaa läpän tromboosiin.17,18 Usein nämä potilaat ovat oireettomia, ja heidän dopplergradienttinsa on kaikukardiografiassa normaali, minkä vuoksi nämä löydökset saattavat olla subkliinisiä. On tärkeää, että nämä CTA-poikkeavuudet saattavat korjaantua varfariinilla, ja antikoagulaation puuttuminen alun perin on nousemassa mahdolliseksi riskitekijäksi.19 Tällä hetkellä näiden kuvantamislöydösten kliininen merkitys on kuitenkin epäselvä20. Onneksi on meneillään satunnaistettu tutkimus GALILEO (Global Study Comparing a Rivaroxaban-Based Antithrombotic Strategy to an Antiplatelet-Based Strategy After Transcatheter Aortic Valve Replacement to Optimize Clinical Outcomes), jossa verrataan rivaroksabaania trombosyyttien estohoitoon TAVR-hoidon jälkeen, ja sen pitäisi antaa arvokasta tietoa.21 Vaikka tutkimukseen on arviolta osallistunut 1520 potilasta, tutkimuksessa ei ehkä ole riittävästi tehoa kliinisten tapahtumien määrittämiseksi.
Johtopäätökset
Kaiken kaikkiaan potilailla, joilla on bioproteesiläpät, varhaiset ei-proseduraaliset tromboemboliset tapahtumat ovat harvinaisia. Lisäksi avoimen läppätromboosin esiintyvyys on todennäköisesti vähäinen, ja subakuutin läppätromboosin vaikutus läpän kestävyyteen on vasta määrittelyssä. Kun otetaan huomioon nämä havainnot ja varfariinin aiheuttama lisääntynyt verenvuotoriski, suosittelemme valikoivaa lähestymistapaa leikkauksen jälkeiseen antikoagulaatiohoitoon (kuva 3). Bioproteettisilla aorttaläpillä varustettujen potilaiden antikoagulaatio 3-6 kuukauden ajan on aiheellista potilaille, joilla on vakiintuneita riskitekijöitä, kuten eteisvärinä. Viimeaikaisten uusien todisteiden perusteella antikoagulaatiota ja tiivistä seurantaa olisi harkittava potilailla, joilla on epänormaaleja kaikukardiografisia tai CTA-löydöksiä, kuten selittämätön Doppler-läpän gradientin nousu tai hypoattenuoitunut läpän paksuuntuminen. Vaikka tietoja on saatavilla vähemmän, bioproteettisilla mitraaliläpillä varustetuilla potilailla näyttää olevan suurempi tromboottisten komplikaatioiden riski, ja rutiininomaista antikoagulaatiota suositellaan 3-6 kuukauden ajan.
Kuvio 3: Ehdotettu lähestymistapa antikoagulaatioon bioproteettisen läpänvaihdon jälkeen
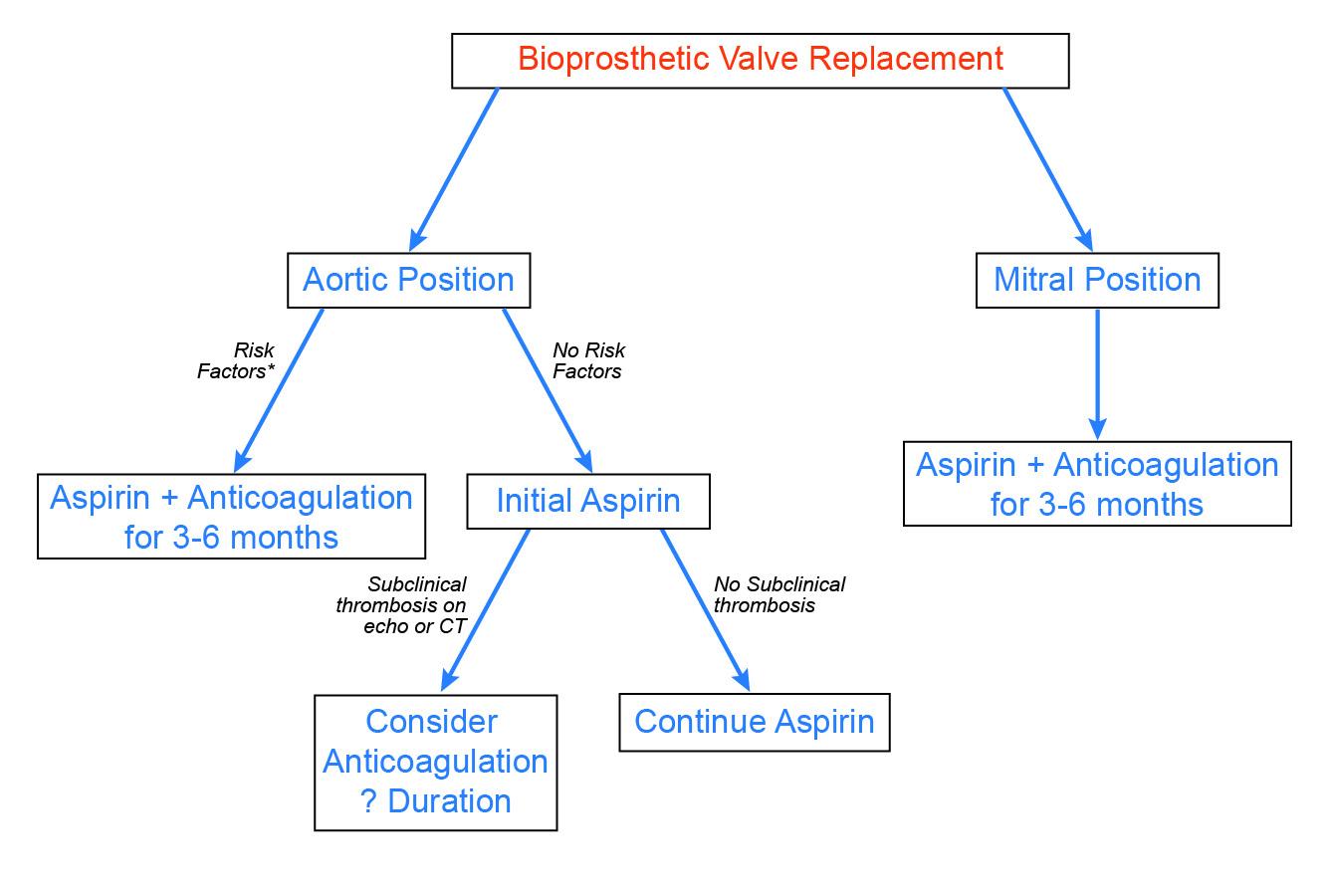
Tämä artikkeli sisältää opetusmateriaalia, joka on tarkoitettu luvan saaneille terveydenhuollon ammattilaisille, ja se on tarkoitettu käytettäväksi yksinomaan koulutus- ja tiedotustarkoituksiin. Vaikka sisältö voi koskea tiettyjä lääketieteellisiä ja terveydenhoitoon liittyviä kysymyksiä, se ei korvaa tai korvaa henkilökohtaista lääketieteellistä neuvontaa, eikä sitä ole tarkoitettu käytettäväksi ainoana perustana yksilöllisten lääketieteellisten tai terveyteen liittyvien päätösten tekemiselle. Esitetyt näkemykset ja mielipiteet ovat kirjoittajien ja toimittajien omia eivätkä välttämättä edusta ACC:n näkemyksiä. Aineiston tarkoituksena ei ole esittää ainoita tai välttämättä parhaita menetelmiä tai menettelyjä käsiteltyihin lääketieteellisiin tilanteisiin, vaan pikemminkin edustaa lähestymistapaa, näkemystä, lausuntoa tai mielipidettä.
- Pibarot P, Dumesnil JG. Sydänproteesit: optimaalisen proteesin valinta ja pitkäaikaishoito. Circulation 2009;119:1034-48.
- Mack MJ, Douglas PS, Holmes DR. Shedding More Lighting on Valve Thrombosis After Transcatheter Aortic Valve Replacement. J Am Coll Cardiol 2016;67:656-8.
- Heras M, Chesebro JH, Fuster V, et al. High risk of thromboemboli early after bioprosthetic cardiac valve replacement. J Am Coll Caridol 1995;25:1111-9.
- Roudaut R, Serri K, Lafitte S. Thrombosis of prosthetic heart valves: diagnosis and therapeutic considerations. Heart 2007;93:137-42.
- Masri A, Gillinov AM, Johnston DM, et al. Antikoagulaatio vs. trombosyyttien estohoito tai ei hoitoa potilailla, joille tehdään bioproteettisen läpän implantointi: systemaattinen katsaus ja meta-analyysi. Heart 2017;103:40-80.
- R Core Team (2015). R: A language and environment for statistical computing. R Foundation for Statistical Computing; Wien, Itävalta. Saatavilla osoitteessa: https://www.R-project.org/. (Käyttämällä funktiota power.prop.test α = 0.05 ja β = 0.8)
- Aramendi JI, Mestres CA, Martinez-León J, Campos V, Muñoz G, Navas C. Triflusaalinen versus oraalinen antikoagulaatio tromboembolian primaaripreventiossa bioproteettisen läpän vaihdon jälkeen (trac): prospektiivinen, satunnaistettu, yhteistoiminnallinen tutkimus. Eur J Cardiothorac Surg 2005;27:854-60.
- Colli A, Mestres CA, Castella M, Gherli T. Vertailu varfariinin ja aspiriinin välillä (WoA) aorttaläpän vaihdon jälkeen St. Jude Medical Epic sydänläpän bioproteesilla: WoA Epic pilottitutkimuksen tulokset. J Heart Valve Dis 2007;16:667-71.
- Mérie C, Køber L, Skov Olsen P, et al. Assosiaatio varfariinihoidon kestosta bioproteettisen aorttaläpän vaihdon jälkeen kuolleisuuden, tromboembolisten komplikaatioiden ja verenvuotojen riskiin. JAMA 2012;308:2118-25.
- Cremer PC, Rodriguez LL, Griffin BP, et al. Early Bioprosthetic Valve Failure: Mechanistic Insights via Correlation between Echocardiographic and Operative Findings. J Am Soc Echocardiogr 2015;28:1131-48.
- Brown ML, Park SJ, Sundt TM, Schaff HV. Varhainen tromboosiriski potilailla, joilla on biologiset läpät aortan asennossa. J Thorac Cardiovasc Surg 2012;144:108-11.
- Nishimura RA, Otto CM, Bonow RO, et al. 2014 AHA/ACC guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol 2014;63:e57-185.
- Egbe AC, Pislaru SV, Pellikka PA, et al. Bioprosthetic Valve Thrombosis Versus Structural Failure: Clinical and Echocardiographic Predictors. J Am Coll Cardiol 2015;66:2285-94.
- Stewart WJ. Bioproteettisten läppien tromboosi: Can We Afford to Ignore It? J Am Coll Cardiol 2015;66:2295-7.
- Russo A, Grigioni F, Avierinos JF, et al. Thromboembolic complications after surgical correction of mitral regurgitation incidence, predictors, and clinical implications. J Am Coll Cardiol 2008;51:1203-11.
- Butnaru A, Shaheen J, Tzivoni D, Tauber R, Bitran D, Silberman S. Diagnosis and treatment of early bioprosthetic malfunction in the mitral valve position due to thrombus formation. Am J Cardiol 2013;112:1439-44.
- Makkar RR, Fontana G, Jilaihawi H, et al. Possible Subclinical Leaflet Thrombosis in Bioprosthetic Aortic Valves. N Engj J Med 2015;373:2015-24.
- Pache G, Schoechlin S, Blanke P, et al. Early hypo-attenuated leaflet thickening in balloon-expandable transcatheter aortic heart valves. Eur Heart J 2016;37:2263-71.
- Hansson NC, Grove EL, Andersen HR, et al. Transcatheter Aortic Valve Thrombosis: Incidence, Predisposing Factors, and Clinical Implications. J Am Coll Cardiol 2016;68:2059-69.
- Laschinger JC, Wu C, Ibrahim NG, Shuren JE. Reduced Leaflet Motion in Bioprosthetic Aortic Valves–The FDA Perspective. N Engj J Med 2015;373:1996-8.
- Global Study Comparing a rivAroxaban-based Antithrombotic Strategy to an antipLatelet-based Strategy After Transcatheter aortIc vaLve rEplacement to Optimize Clinical Outcomes (GALILEO) (Global Study Comparing a rivAroxaban-based Antithrombotic Strategy to an antipLatelet-based Strategy After Transcatheter aortIc vaLve rEplacement to Optimize Clinical Outcomes (GALILEO) (KliinisetTrails.gov-verkkosivusto). 2016. Saatavilla osoitteessa: https://clinicaltrials.gov/ct2/show/NCT02556203. Accessed 11/29/2016.
Kliiniset aiheet: Antikoagulaation hoito, rytmihäiriöt ja kliininen EP, sydänkirurgia, sydämen vajaatoiminta ja kardiomyopatiat, invasiivinen kardiovaskulaarinen angiografia ja interventio, noninvasiivinen kuvantaminen, sydämen läppäviat, antikoagulaation hoito ja eteisvärinä, eteisvärinä / supraventrikulaariset rytmihäiriöt, Aortan leikkaus, Sydänkirurgia ja rytmihäiriöt, Sydänkirurgia ja sydämen vajaatoiminta, Sydänkirurgia ja VHD, Akuutti sydämen vajaatoiminta, Toimenpiteet ja kuvantaminen, Toimenpiteet ja rakenteelliset sydänsairaudet, Angiografia, kaikukardiografia/ultraääni, ydinkuvantaminen
Sanoja: Avainsanat: Aorttaläppä, aorttaläpän ahtauma, eteisvärinä, aspiriini, bioproteesi, tapaus-kontrollitutkimukset, angiografia, ahtauma, patologinen, kaikukardiografia, transesofageaalinen, elektrokardiografia, sydämen vajaatoiminta, sydänläppien sairaudet, Sydänläppäproteesi, Mitraaliläppä, Mitraaliläpän ahtauma, Reoperaatio, Riskitekijät, Aivohalvaus, Ompeleet, Tromboosi, Tiklopidiini, Transkatetrinen aorttaläpän vaihto, K-vitamiini, varfariini
< Takaisin listauksiin