Adduktio (latinan sanasta adductus, ”kohti vedetty” vaihtoehtoisesti supistuma sanasta ”additiotuote”) on kahden tai useamman erillisen molekyylin suoran yhteenliittämisen tuote, jonka tuloksena syntyy yksi reaktiotuote, joka sisältää kaikkien komponenttien kaikki atomit. Tulosta pidetään erillisenä molekyylilajina. Esimerkkeinä voidaan mainita natriumbisulfiitin lisäys aldehydiin, jolloin saadaan sulfonaatti. Sitä voidaan pitää vain yhtenä eri molekyylien suoran yhdistymisen tuloksena syntyvänä tuotteena, joka sisältää kaikki reagoivien molekyylien atomit.
Lewishappojen ja -emästen välille muodostuu usein addukteja. Hyvä esimerkki on adduktien muodostuminen Lewis-hapon booraanin ja Lewis-baseissa olevan happiatomin, tetrahydrofuraanin (THF), välille: BH3-O(CH2)4 tai dietyylieetteri: BH3-O(CH3CH2)2. ECW-mallilla on tutkittu monia kaasufaasissa tai muissa kuin vesiliuottimissa reagoivia Lewis-happoja ja -emäksiä, jotka muodostavat addukteja. Trimetyyliboron, trimetyylitinakloridi ja bis(heksafluoroasetyyliasetonato)kupari(II) ovat esimerkkejä Lewis-hapoista, jotka muodostavat addukteja, joilla on steriinejä vaikutuksia. Esimerkiksi: trimetyylitinakloridi reagoidessaan dietyylieetterin kanssa osoittaa steriittistä hylkimistä Sn:n metyyliryhmien ja hapen etyyliryhmien välillä. Mutta kun Lewisin emäs on tetrahydrofuraani, steerinen repulsio vähenee. ECW-mallilla voidaan mitata näitä staattisia vaikutuksia.
-
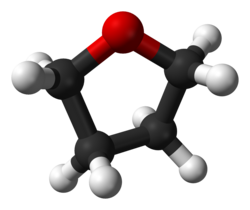
THF-molekyyli
-
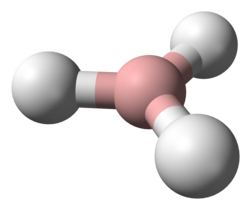
BH3-molekyyli
-
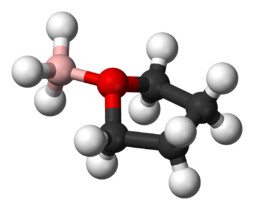
BH3:n ja THF:n välinen Lewis-addukti
Yhdisteitä tai seoksia, jotka eivät pysty muodostamaan adduktiota steerisen esteen vuoksi, kutsutaan turhautuneiksi Lewis-pareiksi.
Adduktiot eivät välttämättä ole luonteeltaan molekyylisiä. Hyvä esimerkki kiinteän olomuodon kemiasta ovat CuAlCl4:n eteenin tai hiilimonoksidin adduktit. Jälkimmäinen on kiinteä aine, jolla on laajennettu ristikkorakenne. Adduktin muodostuessa muodostuu uusi laajennettu faasi, jossa kaasumolekyylit ovat rakenteessa olevien kupariatomien ligandeina. Tätä reaktiota voidaan pitää myös emäksen ja Lewisin hapon välisenä reaktiona, jossa kupariatomi on elektronia vastaanottavassa roolissa ja kaasumolekyylin pii-elektronit elektronia luovuttavassa roolissa.


