Hauptunterschied – sterische vs. torsionale Dehnung
Die Dehnung ist die Abstoßung zwischen Bindungselektronen eines Moleküls. Die Anordnung eines Moleküls hängt von der Dehnung ab, da die Bindungselektronenpaare so angeordnet sind, dass die Dehnung minimiert wird. Es gibt drei Haupttypen von Dehnungen, die in einem Molekül vorkommen können. Es handelt sich um die Winkeldehnung, die Torsionsdehnung und die sterische Dehnung. Die Winkeldehnung tritt auf, wenn die Bindungswinkel der tatsächlichen Moleküle von denen idealer Moleküle abweichen. Die Torsionsspannung entsteht, wenn ein Molekül um eine Bindung gedreht wird. Sterische Dehnung entsteht, wenn sich zwei oder mehr sperrige Gruppen einander nähern. Der Hauptunterschied zwischen sterischer und torsionaler Dehnung besteht darin, dass die sterische Dehnung nicht durch Rotation des Moleküls um eine Bindung verringert werden kann, während die torsionale Dehnung durch Rotation des Moleküls um eine Bindung verringert werden kann.
Behandelte Schlüsselbereiche
1. Was ist Sterische Dehnung
– Definition, Erklärung mit Beispielen
2. Was ist Torsionsdehnung
– Definition, Erklärung mit Beispielen
3. Was ist der Unterschied zwischen Sterischer und Torsionsdehnung
– Vergleich der Hauptunterschiede
Schlüsselbegriffe: Winkelspannung, Bindungselektronenpaar, sterische Spannung, Torsionsspannung

Was ist sterische Spannung
Die sterische Spannung ist die Abstoßung zwischen zwei Atomen oder Gruppen von Atomen, wenn der Abstand zwischen ihnen verringert wird. Dies wird auch als sterische Hinderung bezeichnet. Die sterische Spannung ist sehr wichtig, um die Anordnung eines Moleküls zu bestimmen, da jedes Molekül so angeordnet ist, dass die sterische Spannung minimiert wird. Wenn die sterische Spannung minimiert ist, wird die potenzielle Energie des Moleküls verringert. Da Materie stabil ist, wenn sie ein niedrigeres Energieniveau hat, macht das niedrigere Energieniveau eines Moleküls dieses zu einem stabilen Molekül.
Das Konzept der sterischen Spannung ist sehr wichtig für die Vorhersage der Produkte einer chemischen Reaktion. Das liegt daran, dass Atomgruppen so an ein Kohlenstoffatom gebunden sind, dass das sterische Hindernis minimiert wird. Daher entsteht bei einer chemischen Reaktion ein Molekülgemisch, das stabile und instabile Produkte enthält. Der Hauptbestandteil dieses Gemischs wird jedoch immer das stabile Produkt mit der geringsten sterischen Hinderung sein.

Abbildung 1: Sterische Spannung in organischen Verbindungen
Wie in der obigen Abbildung zu sehen ist, erhöht sich die potentielle Energie eines Moleküls je nach der sterischen Spannung, die es aufweist. Wenn sich der Abstand zwischen zwei Methylgruppen verringert, erhöht sich die potentielle Energie.
Abbildung 2: Die sterische Belastung nimmt zu, wenn sperrige Gruppen vorhanden sind
Die obige Abbildung zeigt, dass die sterische Belastung zunimmt, wenn sperrige Gruppen vorhanden sind. Stärker sterisch gehinderte Moleküle haben eine höhere potentielle Energie im Vergleich zu weniger sterisch gehinderten Molekülen. Daher sind weniger sterisch gehinderte Moleküle stabiler.
Was ist Torsionsspannung
Torsionsspannung ist die Abstoßung, die zwischen Atomen oder Atomgruppen entsteht, wenn ein Molekül um eine Sigma-Bindung gedreht wird. Dies ist die Abstoßung, die beobachtet werden kann, wenn Bindungselektronen aneinander vorbeigehen. Diese Art der Belastung ist wichtig für die Bestimmung der stabilen Konformationen organischer Verbindungen. Diese Konformationen können durch Newman-Projektionen dargestellt werden. Die Newman-Projektion eines Moleküls ist die Konformation dieses Moleküls, wenn man von vorne nach hinten durch die C-C-Bindung blickt.
Die Torsionsspannung entsteht, wenn der Flächenwinkel der sperrigen Gruppen klein ist. Der Flächenwinkel ist der Winkel zwischen zwei Bindungen von zwei verschiedenen Kohlenstoffatomen in einer Newman-Projektion. Wenn der Flächenwinkel groß ist, ist die Torsionsspannung gering.
Newman-Projektionen gibt es in zwei Arten, als gestaffelte Konformation und als eklipsierte Konformation. Die eclipsed Konformation zeigt eine höhere Torsionsspannung als die staggered Konformation.
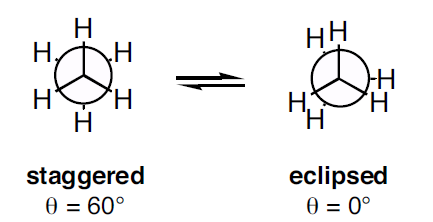
Abbildung 3: Zwei Arten von Newman-Projektionen
Wie in der obigen Abbildung gezeigt, zeigt die staggered Konformation einen Flächenwinkel von 60o und die eclipsed Konformation einen Flächenwinkel von 0o. Wenn das Molekül jedoch gedreht wird, ändert sich die Konformation. Die Torsionsspannung in der gestaffelten Konformation ist geringer als die der eklipsierten Konformation. Wenn das Molekül gedreht wird, kann die eclipsed Konformation in die staggered Konformation übergehen; dadurch wird die Torsionsspannung reduziert.
Unterschied zwischen sterischer und torsionaler Spannung
Definition
Sterische Spannung: Sterische Spannung ist die Abstoßung zwischen zwei Atomen oder Gruppen von Atomen, wenn der Abstand zwischen ihnen verringert wird.
Torsionsspannung: Torsionsspannung ist die Abstoßung, die zwischen Atomen oder Atomgruppen entsteht, wenn ein Molekül um eine Sigma-Bindung gedreht wird.
Rotation des Moleküls
Sterische Spannung: Sterische Dehnung kann nicht durch Rotation des Moleküls um eine Sigma-Bindung verringert werden.
Torsionsdehnung: Die Torsionsspannung kann durch Rotation des Moleküls um eine Sigma-Bindung verringert werden.
Ursache für die Spannung
Sterische Spannung: Sterische Dehnung tritt auf, wenn der Abstand zwischen sperrigen Gruppen eines Moleküls verringert wird.
Torsionsdehnung: Torsionsspannung tritt auf, wenn Bindungselektronen aneinander vorbeigehen, wenn das Molekül rotiert.
Schlussfolgerung
Die Spannung eines Moleküls ist die Abstoßung zwischen Bindungselektronen oder Einzelelektronenpaaren, die in diesem Molekül vorhanden sind. Diese Abstoßung bewirkt, dass die potentielle Energie eines Moleküls erhöht wird. Dadurch wird das Molekül instabil. Die sterische Spannung eines Moleküls wird durch die in einem Molekül vorhandenen sperrigen Gruppen und den Abstand zwischen diesen sperrigen Gruppen bestimmt. Die Newman-Projektion ist eine einfache Struktur, die die Anordnung von Atomen oder Gruppen von Atomen in einem organischen Molekül zeigt. Sie kann verwendet werden, um die Torsionsspannung eines Moleküls zu bestimmen. Der Hauptunterschied zwischen sterischer und torsionaler Dehnung besteht darin, dass die sterische Dehnung nicht durch Rotation des Moleküls um eine Bindung verringert werden kann, während die torsionale Dehnung durch Rotation des Moleküls um eine Bindung verringert werden kann.
1. „Torsional Strain“. OChemPal, Available here. Accessed 28 Aug. 2017.
2. „Strain (Chemistry).“ Wikipedia, Wikimedia Foundation, 25. Juli 2017, Available here. Accessed 28 Aug. 2017.
3. „Dihedral Angle.“ OChemPal, Available here. Accessed 28 Aug. 2017.
Image Courtesy:
1. „Napthalene phenanthraene methyl-methyl strai“ By DMacks – Own work (Public Domain) via Commons Wikimedia
2. „Steric hindrance disp“ By Mwolf37 – Own work (CC BY-SA 3.0) via Commons Wikimedia
3. „Escalonada e eclipsada“ By Pauloquimico – Own work (CC BY-SA 3.0) via Commons Wikimedia
![]()