Über 200.000 Menschen haben sich einem Transkatheter-Aortenklappenersatz (TAVR) unterzogen, und jedes Jahr erhalten etwa 140.000 Patienten eine chirurgische bioprothetische Klappe.1,2 Trotz dieser steigenden Zahl ist die optimale postoperative Antikoagulationsstrategie oft unklar. Insbesondere zwei Fragen unterstreichen die Schwierigkeit bei der Entscheidungsfindung für diese häufigen klinischen Szenarien:
- Welche Komplikationen versuchen wir in den ersten Monaten nach dem bioprothetischen Klappenersatz mit einer Antikoagulation zu reduzieren?
- Sollten alle Patienten eine Antikoagulation erhalten, um diese Komplikationen zu reduzieren? Oder sollten wir einen selektiveren Ansatz auf der Grundlage von Risikofaktoren verfolgen?
Thromboserisiken nach bioprothetischem Klappenersatz
Traditionell besteht die Begründung für die Antikoagulation in den ersten Monaten nach dem chirurgischen Klappenersatz darin, thrombotische Komplikationen zu verhindern, die vermutlich mit dem Nahtmaterial und einem noch nicht mit Biofilm überzogenen und endothelialisierten Nähring zusammenhängen.3,4 Die möglichen thrombotischen Folgekomplikationen sind dreifach: thromboembolische Ereignisse, offene Thrombose der Klappe und subklinische organisierte Thromben, die die langfristige Funktion der Klappe beeinträchtigen können. Trotz der Häufigkeit des bioprothetischen Klappenersatzes sind die Daten zu diesen Komplikationen begrenzt, zum Teil, weil diese Ereignisse scheinbar selten sind.
Eine kürzlich durchgeführte Meta-Analyse unterstrich die niedrige Ereignisrate nach bioprothetischem Klappenersatz. In dieser Analyse von 31.740 Patienten, überwiegend mit chirurgischem Aortenklappenersatz, traten frühe thromboembolische Ereignisse bei 145 Patienten (1 %), die Vitamin-K-Antagonisten einnahmen, und 262 Patienten (1,5 %), die keine Vitamin-K-Antagonisten einnahmen, auf (Odds Ratio 0,96; 95 % Konfidenzintervall, 0,60-1,52).5 Wenn wir davon ausgehen, dass die Zahl der thromboembolischen Komplikationen in den ersten Monaten nach einem chirurgischen Aortenklappenersatz bei Patienten, die keine Vitamin-K-Antagonisten einnehmen, tatsächlich um 0,5 % ansteigt, dann wären für eine entsprechend aussagekräftige randomisierte kontrollierte Studie etwa 15.500 Patienten erforderlich.6 Bislang wurden 2 randomisierte Studien mit insgesamt 268 Patienten durchgeführt.7,8 Angesichts der geringen Patientenzahl ist das Fehlen eines statistisch nachweisbaren Unterschieds zwischen den beiden Gruppen nicht überraschend.
In Ermangelung großer randomisierter kontrollierter Studien müssen Kliniker auf Beobachtungsstudien zurückgreifen, um Erkenntnisse zu gewinnen, wie z. B. die Analyse des dänischen nationalen Patientenregisters.9 In dieser Studie mit 4 075 Patienten mit bioprothetischem Aortenklappenersatz war das Absetzen von Warfarin mit einer Zunahme thromboembolischer Ereignisse und kardiovaskulärer Todesfälle 1-6 Monate nach dem Eingriff verbunden. Interessanterweise war zwar die Schlaganfallrate in den ersten drei Monaten in der Behandlungsgruppe erhöht, die Zahl der Schlaganfälle zwischen drei und sechs Monaten unterschied sich jedoch nicht zwischen den Patienten, die das Warfarin fortführten oder absetzten, obwohl es in diesem Zeitraum nur 21 Ereignisse gab. Auch bei den Blutungsereignissen gab es keinen Unterschied zwischen 3 Monaten und 1 Jahr. Diese Beobachtung steht im Widerspruch zu früheren Berichten und klinischen Erfahrungen, wonach Patienten unter Warfarin häufiger wegen Blutungen ins Krankenhaus eingeliefert werden.5 Die Schlussfolgerungen der Autoren in Bezug auf die kardiovaskuläre Sterblichkeit und thromboembolische Ereignisse könnten daher auf ein Rest-Confounding zurückzuführen sein. Insbesondere könnte es keinen Unterschied bei den Blutungsereignissen gegeben haben, weil die Kliniker bei den Hochrisikopatienten seltener eine Antikoagulation einleiteten oder fortsetzten.
Im Vergleich zu den thromboembolischen Ereignissen geben die veröffentlichten Daten leider noch weniger Aufschluss über die Zusammenhänge bei bioprothetischen Klappenthrombosen. Es wurden nur wenige Ereignisse berichtet, und die meiste Literatur beschränkt sich auf Fallserien und Erfahrungen einzelner Zentren.10 Folglich ist die Inzidenz der bioprothetischen Klappenthrombose nicht genau definiert, obwohl in einer Studie nur 8 von 4.568 Patienten mit bioprothetischen Aortenklappen eine Reoperation wegen einer thrombusbedingten Aortenstenose benötigten.11 Ebenso ist die Rolle der klinisch stummen Thrombose und einer möglichen beschleunigten bioprothetischen Klappendegeneration weitgehend unbekannt.
Selektive Antikoagulation nach bioprothetischem Klappenersatz
Basierend auf einem unklaren Ausmaß des Nutzens und einem gut akzeptierten Blutungsrisiko ist eine universelle Antikoagulation nach bioprothetischem Aortenklappenersatz schwer zu rechtfertigen; diese Unsicherheit spiegelt sich in der Klasse IIb-Empfehlung in den Leitlinien für Herzklappenerkrankungen des American College of Cardiology und der American Heart Association (ACC/AHA) von 2014 wider.12 Es können jedoch spezifische klinische Situationen auftreten, in denen eine Antikoagulation stärker in Betracht gezogen werden sollte. In einer kürzlich durchgeführten Fall-Kontroll-Studie mit 46 Patienten, die wegen einer Thrombose der bioprothetischen Aortenklappe reoperiert wurden, waren beispielsweise ein Anstieg >50 % des mittleren Doppler-Gradienten in der Echokardiographie gegenüber dem Ausgangswert, eine erhöhte Höckerdicke und eine abnormale Höckermobilität mit einer Klappenthrombose assoziiert.13 Daher könnte bei diesen Patienten eine Antikoagulationsstudie und eine Nachuntersuchung der Echokardiographie zur Beurteilung der Doppler-Gradienten in Betracht gezogen werden,14 obwohl unklar ist, inwieweit die kurz- und langfristige Klappenfunktion durch die Antikoagulation verändert wird.
Außerdem scheinen Patienten mit einer bioprothetischen Mitralklappe ein höheres Risiko für thromboembolische Ereignisse und Klappenthrombosen zu haben (siehe den illustrativen Fall mit den Abbildungen 1-2 und Videos 1-2 unten). Da der bioprothetische Mitralklappenersatz viel seltener ist als der Aortenklappenersatz, sind die Daten noch begrenzter. In einer Studie an einem einzigen Zentrum mit 216 Patienten mit bioprothetischem Mitralklappenersatz erlitten jedoch 10 (5 %) innerhalb von 6 Monaten einen ischämischen Schlaganfall.15 In einer anderen Studie mit 149 konsekutiven Patienten entwickelten 9 (6 %) eine bioprothetische Mitralklappenthrombose.16 Daher scheinen Patienten mit bioprothetischem Mitralklappenersatz einem höheren Risiko ausgesetzt zu sein, und eine routinemäßige Antikoagulation sollte für 3-6 Monate in Betracht gezogen werden, was sich auch in der Klasse IIa-Empfehlung der ACC/AHA-Leitlinien für Herzklappenerkrankungen von 2014 widerspiegelt.12
Illustrativer Fall: Bioprothetische Mitralklappenthrombose
Eine 71-jährige Frau stellte sich 8 Monate nach einem bioprothetischen Mitralklappenersatz wegen einer rheumatischen Mitralstenose mit Herzversagen vor. Postoperativ war sie 3 Monate lang mit Cumadin behandelt worden und nahm weiterhin Aspirin ein. Sie hatte kein Vorhofflimmern in der Anamnese, war fieberfrei und die Blutkulturen waren negativ.
Video 1
Abbildung 1
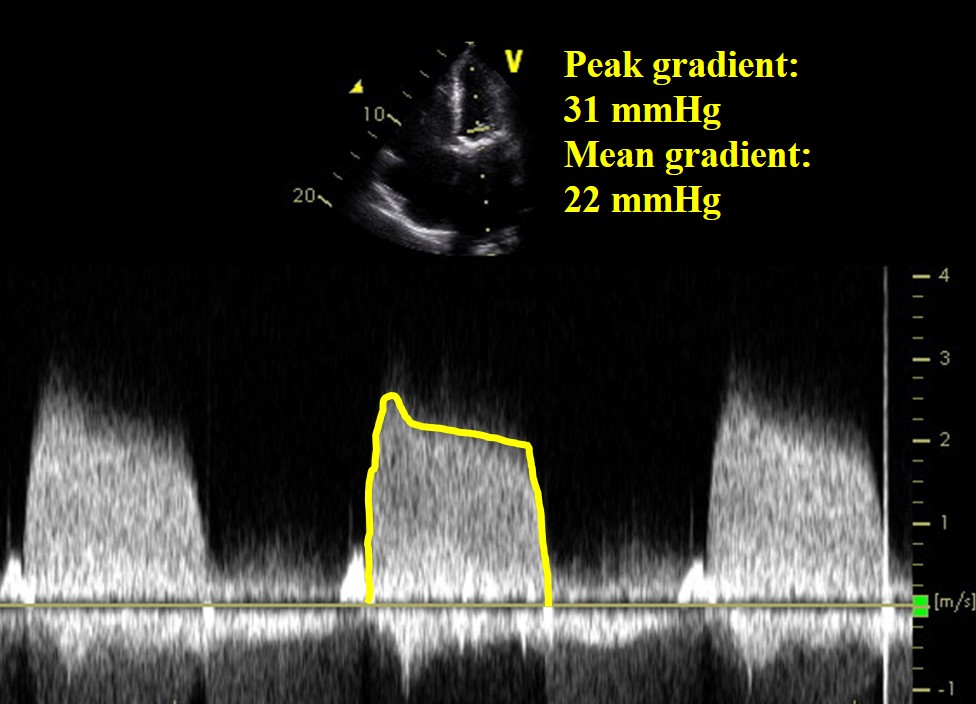
Video 2
Abbildung 2
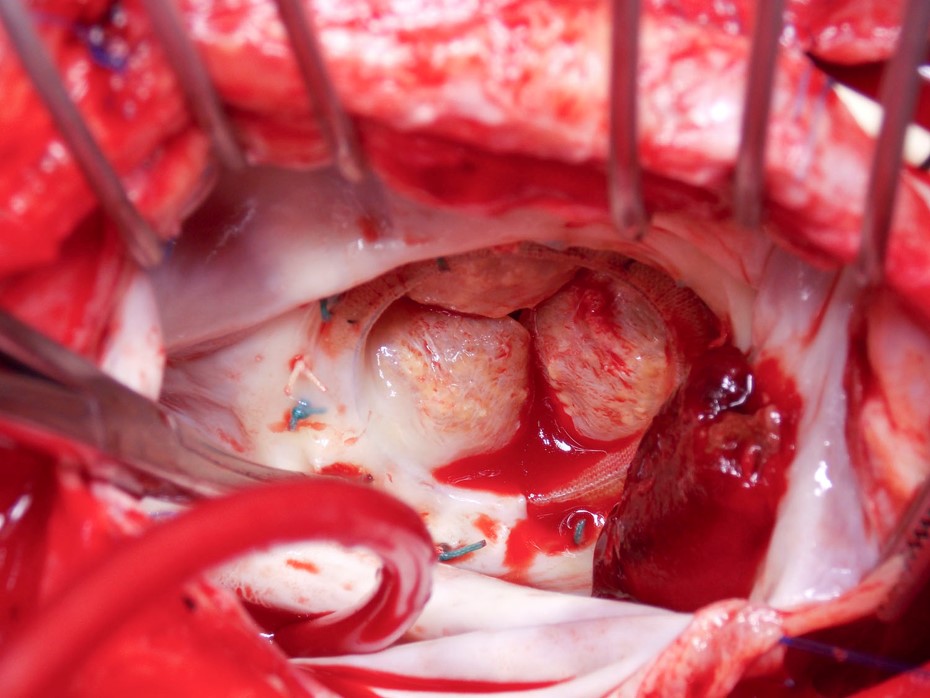
Schließlich und vielleicht am umstrittensten ist die Frage, ob wir bei Patienten, die sich einer TAVR unterzogen haben, anders mit der Antikoagulation umgehen sollten. Ursprünglich wurden diese Patienten standardmäßig mit Aspirin und Clopidogrel behandelt, weil dies der Ansatz war, der in den randomisierten Studien verfolgt wurde. In jüngerer Zeit wurden mit der elektrokardiographisch gesteuerten vierdimensionalen Computertomographie-Angiographie (CTA) eine verringerte Beweglichkeit der bioprothetischen Aortenklappenflügel und eine hypoabgeschwächte Verdickung der Flügel beschrieben, was auf eine Klappen-Thrombose hindeutet.17,18 Häufig sind diese Patienten asymptomatisch und haben normale Doppler-Gradienten in der Echokardiographie, was darauf hindeutet, dass diese Befunde subklinisch sein könnten. Wichtig ist, dass sich diese CTA-Anomalien unter Warfarin zurückbilden können, und eine fehlende anfängliche Antikoagulation erweist sich als möglicher Risikofaktor.19 Derzeit sind diese bildgebenden Befunde jedoch von unklarer klinischer Bedeutung.20 Glücklicherweise läuft derzeit eine randomisierte Studie, GALILEO (Global Study Comparing a Rivaroxaban-Based Antithrombotic Strategy to an Antiplatelet-Based Strategy After Transcatheter Aortic Valve Replacement to Optimize Clinical Outcomes), in der Rivaroxaban mit einer Thrombozytenaggregationshemmer-Therapie nach TAVR verglichen wird und die wertvolle Erkenntnisse liefern dürfte.21 Trotz einer geschätzten Teilnehmerzahl von 1.520 Patienten ist die Studie jedoch möglicherweise nicht ausreichend auf klinische Ereignisse ausgerichtet.
Schlussfolgerungen
Insgesamt sind bei Patienten mit bioprothetischen Klappen frühe nicht-prozedurale thromboembolische Ereignisse selten. Darüber hinaus ist die Inzidenz offener Klappenthrombosen wahrscheinlich gering, und die Auswirkungen subakuter Klappenthrombosen auf die Haltbarkeit der Klappen sind noch nicht geklärt. In Anbetracht dieser Beobachtungen und des erhöhten Blutungsrisikos bei Warfarin befürworten wir eine selektive Vorgehensweise bei der postoperativen Antikoagulation (Abbildung 3). Bei Patienten mit bioprothetischen Aortenklappen ist eine Antikoagulation für 3-6 Monate bei Patienten mit etablierten Risikofaktoren wie Vorhofflimmern angezeigt. Auf der Grundlage neuerer Erkenntnisse sollten eine Antikoagulation und eine engmaschige Überwachung bei Patienten mit abnormen echokardiographischen oder CTA-Befunden, wie z. B. einem unerklärlichen Anstieg des Doppler-Klappengradienten oder einer hypoabgeschwächten Verdickung des Klappenblattes, in Betracht gezogen werden. Obwohl weniger Daten vorliegen, scheinen Patienten mit bioprothetischen Mitralklappen ein höheres Risiko für thrombotische Komplikationen zu haben, und eine routinemäßige Antikoagulation für 3-6 Monate wird empfohlen.
Abbildung 3: Vorgeschlagenes Konzept für die Antikoagulation nach bioprothetischem Klappenersatz
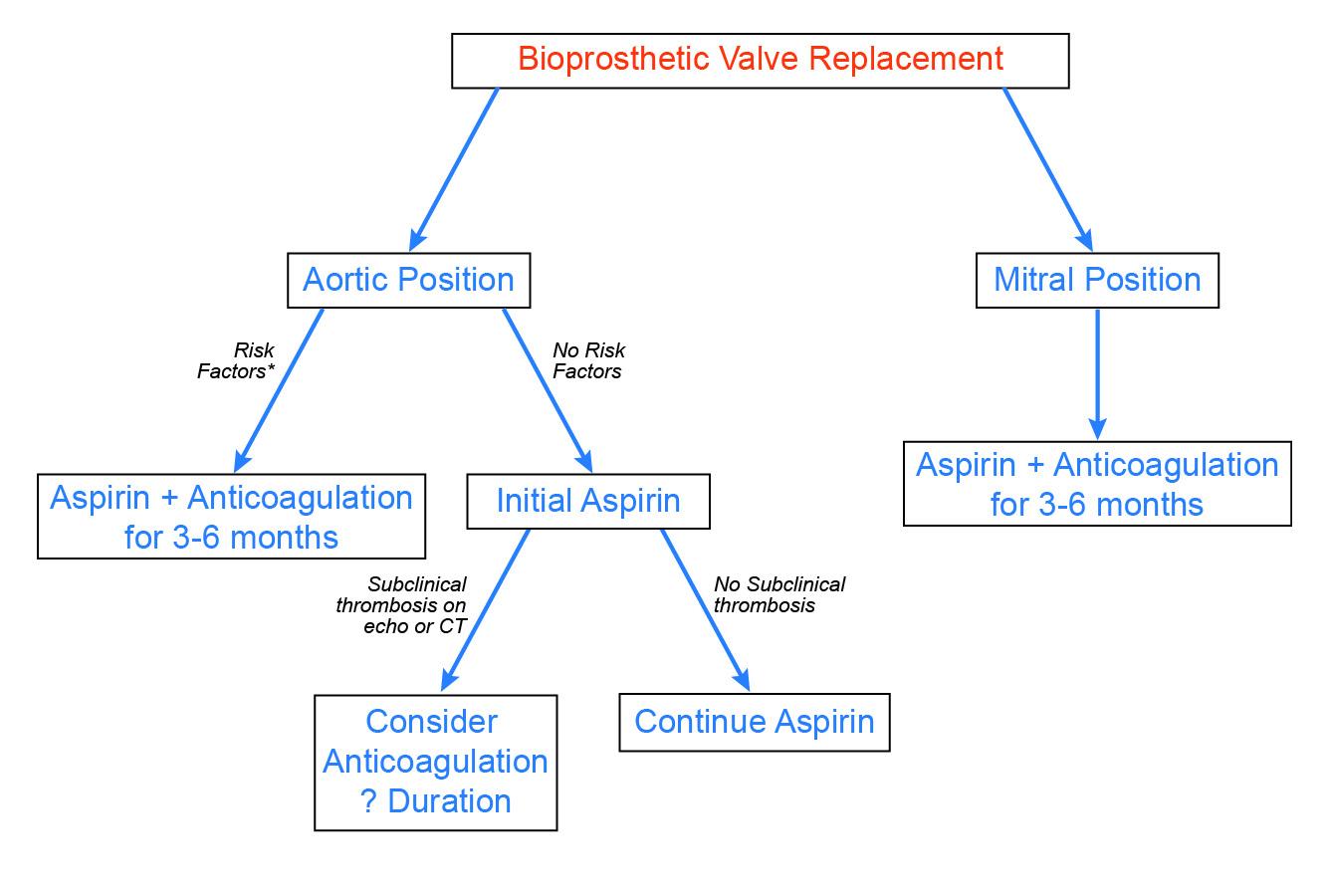
Dieser Artikel enthält Aufklärungsmaterial, das für zugelassenes medizinisches Fachpersonal bestimmt ist und ausschließlich zu Aufklärungs- und Informationszwecken verwendet werden soll. Auch wenn sich der Inhalt auf bestimmte medizinische und gesundheitliche Themen bezieht, ist er kein Ersatz für eine persönliche medizinische Beratung und soll nicht als alleinige Grundlage für individuelle medizinische oder gesundheitsbezogene Entscheidungen dienen. Die Ansichten und Meinungen, die hier zum Ausdruck gebracht werden, sind die der Autoren und Redakteure und geben nicht unbedingt die Ansichten des ACC wieder. Das Material soll nicht die einzigen oder notwendigerweise besten Methoden oder Verfahren für die angesprochenen medizinischen Situationen darstellen, sondern soll vielmehr einen Ansatz, eine Ansicht, eine Aussage oder eine Meinung repräsentieren.
- Pibarot P, Dumesnil JG. Herzklappenprothesen: Auswahl der optimalen Prothese und Langzeitmanagement. Circulation 2009;119:1034-48.
- Mack MJ, Douglas PS, Holmes DR. Shedding More Light on Valve Thrombosis After Transcatheter Aortic Valve Replacement. J Am Coll Cardiol 2016;67:656-8.
- Heras M, Chesebro JH, Fuster V, et al. High risk of thromboemboli early after bioprosthetic cardiac valve replacement. J Am Coll Caridol 1995;25:1111-9.
- Roudaut R, Serri K, Lafitte S. Thrombosis of prosthetic heart valves: diagnosis and therapeutic considerations. Heart 2007;93:137-42.
- Masri A, Gillinov AM, Johnston DM, et al. Antikoagulation versus Thrombozytenaggregationshemmer oder keine Therapie bei Patienten, die sich einer bioprothetischen Klappenimplantation unterziehen: eine systematische Überprüfung und Meta-Analyse. Heart 2017;103:40-80.
- R Core Team (2015). R: A language and environment for statistical computing. R Foundation for Statistical Computing; Wien, Österreich. Verfügbar unter: https://www.R-project.org/. (Using function power.prop.test α = 0.05 and β = 0.8)
- Aramendi JI, Mestres CA, Martinez-León J, Campos V, Muñoz G, Navas C. Triflusal versus oral anticoagulation for primary prevention of thromboembolism after bioprosthetic valve replacement (trac): prospective, randomized, co-operative trial. Eur J Cardiothorac Surg 2005;27:854-60.
- Colli A, Mestres CA, Castella M, Gherli T. Comparing warfarin to aspirin (WoA) after aortic valve replacement with the St. Jude Medical Epic heart valve bioprosthesis: results of the WoA Epic pilot trial. J Heart Valve Dis 2007;16:667-71.
- Mérie C, Køber L, Skov Olsen P, et al. Association of warfarin therapy duration after bioprosthetic aortic valve replacement with risk of mortality, thromboembolic complications, and bleeding. JAMA 2012;308:2118-25.
- Cremer PC, Rodriguez LL, Griffin BP, et al. Early Bioprosthetic Valve Failure: Mechanistic Insights via Correlation between Echocardiographic and Operative Findings. J Am Soc Echocardiogr 2015;28:1131-48.
- Brown ML, Park SJ, Sundt TM, Schaff HV. Frühes Thromboserisiko bei Patienten mit biologischen Klappen in Aortenposition. J Thorac Cardiovasc Surg 2012;144:108-11.
- Nishimura RA, Otto CM, Bonow RO, et al. 2014 AHA/ACC guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol 2014;63:e57-185.
- Egbe AC, Pislaru SV, Pellikka PA, et al. Bioprosthetic Valve Thrombosis Versus Structural Failure: Clinical and Echocardiographic Predictors. J Am Coll Cardiol 2015;66:2285-94.
- Stewart WJ. Thrombosis of Bioprosthetic Valves: Can We Afford to Ignore It? J Am Coll Cardiol 2015;66:2295-7.
- Russo A, Grigioni F, Avierinos JF, et al. Thromboembolic complications after surgical correction of mitral regurgitation incidence, predictors, and clinical implications. J Am Coll Cardiol 2008;51:1203-11.
- Butnaru A, Shaheen J, Tzivoni D, Tauber R, Bitran D, Silberman S. Diagnosis and treatment of early bioprosthetic malfunction in the mitral valve position due to thrombus formation. Am J Cardiol 2013;112:1439-44.
- Makkar RR, Fontana G, Jilaihawi H, et al. Possible Subclinical Leaflet Thrombosis in Bioprosthetic Aortic Valves. N Engj J Med 2015;373:2015-24.
- Pache G, Schoechlin S, Blanke P, et al. Early hypo-attenuated leaflet thickening in ballonexpandable transcatheter aortic heart valves. Eur Heart J 2016;37:2263-71.
- Hansson NC, Grove EL, Andersen HR, et al. Transcatheter Aortic Valve Thrombosis: Incidence, Predisposing Factors, and Clinical Implications. J Am Coll Cardiol 2016;68:2059-69.
- Laschinger JC, Wu C, Ibrahim NG, Shuren JE. Reduced Leaflet Motion in Bioprosthetic Aortic Valves–The FDA Perspective. N Engj J Med 2015;373:1996-8.
- Global Study Comparing a rivAroxaban-based Antithrombotic Strategy to an antipLatelet-based Strategy After Transcatheter aortIc vaLve rEplacement to Optimize Clinical Outcomes (GALILEO) (ClinicalTrails.gov website). 2016. Available at: https://clinicaltrials.gov/ct2/show/NCT02556203. Accessed 11/29/2016.
Klinische Themen: Antikoagulationsmanagement, Arrhythmien und klinische EP, Herzchirurgie, Herzinsuffizienz und Kardiomyopathien, invasive kardiovaskuläre Angiographie und Intervention, nicht-invasive Bildgebung, Herzklappenerkrankung, Antikoagulationsmanagement und Vorhofflimmern, Vorhofflimmern/supraventrikuläre Arrhythmien, Aortenchirurgie, Herzchirurgie und Arrhythmien, Herzchirurgie und Herzinsuffizienz, Herzchirurgie und VHD, Akute Herzinsuffizienz, Interventionen und Bildgebung, Interventionen und strukturelle Herzerkrankungen, Angiographie, Echokardiographie/Ultraschall, Kernspintomographie
Schlüsselwörter: Aortenklappe, Aortenklappenstenose, Vorhofflimmern, Aspirin, Bioprothese, Fall-Kontroll-Studien, Angiographie, Verengung, pathologisch, Echokardiographie, transösophageal, Elektrokardiographie, Herzinsuffizienz, Herzklappenerkrankungen, Herzklappenprothese, Mitralklappe, Mitralklappenstenose, Reoperation, Risikofaktoren, Schlaganfall, Nähte, Thrombose, Ticlopidin, Transkatheter-Aortenklappenersatz, Vitamin K, Warfarin
< Zurück zu den Einträgen