Ein Addukt (vom lateinischen adductus, „hingezogen“, alternativ eine Verkürzung von „Additionsprodukt“) ist ein Produkt einer direkten Addition von zwei oder mehr verschiedenen Molekülen, das zu einem einzigen Reaktionsprodukt führt, das alle Atome aller Komponenten enthält. Das resultierende Produkt wird als eigenständige Molekülart betrachtet. Beispiele hierfür sind die Addition von Natriumbisulfit an einen Aldehyd zur Bildung eines Sulfonats. Es kann nur als ein einziges Produkt betrachtet werden, das aus der direkten Kombination verschiedener Moleküle entsteht und alle Atome der reagierenden Moleküle enthält.
Addukte bilden sich häufig zwischen Lewis-Säuren und Lewis-Basen. Ein gutes Beispiel ist die Bildung von Addukten zwischen der Lewis-Säure Boran und dem Sauerstoffatom in der Lewis-Base Tetrahydrofuran (THF): BH3-O(CH2)4 oder Diethylether: BH3-O(CH3CH2)2. Viele Lewis-Säuren und Lewis-Basen, die in der Gasphase oder in nichtwässrigen Lösungsmitteln unter Bildung von Addukten reagieren, wurden mit dem ECW-Modell untersucht. Trimethylboron, Trimethylzinnchlorid und Bis(hexafluoroacetylacetonato)kupfer(II) sind Beispiele für Lewis-Säuren, die Addukte bilden, die sterische Effekte aufweisen. Ein Beispiel: Trimethylzinnchlorid zeigt bei der Reaktion mit Diethylether eine sterische Abstoßung zwischen den Methylgruppen am Sn und den Ethylgruppen am Sauerstoff. Wenn die Lewis-Base jedoch Tetrahydrofuran ist, ist die sterische Abstoßung geringer. Das ECW-Modell kann ein Maß für diese sterischen Effekte liefern.
-
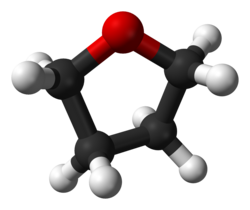
THF-Molekül
-
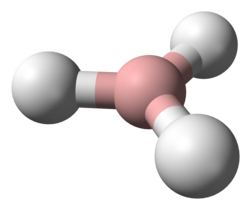
BH3-Molekül
-
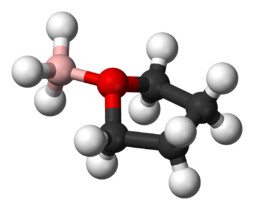
Lewis-Addukt zwischen BH3 und THF
Verbindungen oder Gemische, die aufgrund sterischer Hinderung kein Addukt bilden können, werden als frustrierte Lewis-Paare bezeichnet.
Addukte sind nicht unbedingt molekularer Natur. Ein gutes Beispiel aus der Festkörperchemie sind die Addukte von Ethylen oder Kohlenmonoxid an CuAlCl4. Letzteres ist ein Festkörper mit einer ausgedehnten Gitterstruktur. Bei der Bildung des Addukts bildet sich eine neue ausgedehnte Phase, in der die Gasmoleküle als Liganden der Kupferatome in die Struktur eingebaut (eingefügt) sind. Diese Reaktion kann auch als Reaktion zwischen einer Base und einer Lewis-Säure betrachtet werden, wobei das Kupferatom die Elektronen aufnimmt und die pi-Elektronen des Gasmoleküls die Elektronen abgibt.


